摘要:下列各组的三种溶液.只用酚酞试液.便能鉴别出来的( ) A. H2SO4 HCl NaCl B. HCl Ba(OH)2 KOH C. H2SO4 NaOH KOH D. HCl NaCl NaOH
网址:http://m.1010jiajiao.com/timu3_id_100781[举报]
下列各组的三种溶液,只用酚酞试液(组内物质可互相混合),便能鉴别出来的( )
A、 H2SO4 HCl NaCl B、 HCl Ba(OH)2 KOH
C、 H2SO4 NaOH KOH D、 HCl NaCl NaOH
查看习题详情和答案>>21、NaNO2(亚硝酸钠)、NaCl和物质M (不含结晶水)的溶解度曲线如图1所示,请根据图象和有关信息回答下列问题:
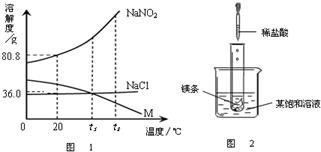
(1)t2℃时,NaNO2、NaCl和M的溶解度由大到小的顺序是
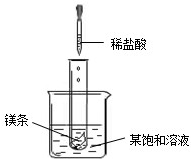
(2)如图2所示,当往试管中加入5mL稀盐酸时,试管内立刻产生大量气泡,同时放热使烧杯中饱和溶液变浑浊(不考虑水分蒸发).请判断:该饱和溶液中的溶质是
(3)分别将NaNO2、NaCl和M的饱和溶液从t2℃降温到t1℃时,三种溶液中溶质的质量分数由大到小的顺序是
(4)NaNO2有毒,其外观和咸味与食盐很相似,因此要防止因误食NaNO2而发生中毒事故.为了区别NaNO2、NaCl固体,某化学兴趣小组同学查阅资料获得如下信息:NaNO2的水溶液呈碱性,NaCl的水溶液呈中性;NaNO2熔点为271℃,NaCl熔点为801℃.
①小明同学设计的鉴别实验方案如下:
20℃时分别取NaNO2、NaCl各5.0g于两只小烧杯中,分别加入10mL水(水的密度近似看作1g/cm3),用玻璃棒充分搅拌后观察.你认为此方案是否可行
②该小组其他同学又设计出与小明不同的实验方案,并获得成功.你认为该方案可能是
查看习题详情和答案>>

(1)t2℃时,NaNO2、NaCl和M的溶解度由大到小的顺序是
NaNO2>NaCl>M
.(2)如图2所示,当往试管中加入5mL稀盐酸时,试管内立刻产生大量气泡,同时放热使烧杯中饱和溶液变浑浊(不考虑水分蒸发).请判断:该饱和溶液中的溶质是
M
.(填“NaNO2”或“NaCl”或“M”)(3)分别将NaNO2、NaCl和M的饱和溶液从t2℃降温到t1℃时,三种溶液中溶质的质量分数由大到小的顺序是
NaNO2>NaCl>M
.(4)NaNO2有毒,其外观和咸味与食盐很相似,因此要防止因误食NaNO2而发生中毒事故.为了区别NaNO2、NaCl固体,某化学兴趣小组同学查阅资料获得如下信息:NaNO2的水溶液呈碱性,NaCl的水溶液呈中性;NaNO2熔点为271℃,NaCl熔点为801℃.
①小明同学设计的鉴别实验方案如下:
20℃时分别取NaNO2、NaCl各5.0g于两只小烧杯中,分别加入10mL水(水的密度近似看作1g/cm3),用玻璃棒充分搅拌后观察.你认为此方案是否可行
可行
(填“可行”或“不可行”).②该小组其他同学又设计出与小明不同的实验方案,并获得成功.你认为该方案可能是
别取少量样品于试管中,加水溶解,滴加无色酚酞试液,变红者为NaNO2,不变者为NaCl
(只填写一种方案并简单叙述). (2009?连云港) NaNO2(亚硝酸钠)、NaCl和物质M (不含结晶水)的溶解度曲线如图所示,请根据图象和有关信息回答下列问题:
(2009?连云港) NaNO2(亚硝酸钠)、NaCl和物质M (不含结晶水)的溶解度曲线如图所示,请根据图象和有关信息回答下列问题:(1)t2℃时,NaNO2、NaCl和M的溶解度由大到小的顺序是
NaNO2>NaCl>M
NaNO2>NaCl>M
.(2)如图所示,当往试管中加入5mL稀盐酸时,试管内立刻产生大量气泡,同时放热使烧杯中饱和溶液变浑浊(不考虑水分蒸发).请判断:该饱和溶液中的溶质是NaNO2、NaCl和M中的
M
M
(3)分别将NaNO2、NaCl和M的饱和溶液从t2℃降温到t1℃时,三种溶液中溶质的质量分由大到小的顺序是
NaNO2>NaCl>M
NaNO2>NaCl>M
.(4)NaNO2有毒,其外观和咸味与食盐很相似,因此要防止因误食NaNO2而发生中毒事故.为了区别NaNO2、NaCl固体,某化学兴趣小组同学查阅资料获得如下信息:NaNO2的水溶液呈碱性,NaCl的水溶液呈中性;NaNO2熔点为271℃,NaCl熔点为801℃.
①小明同学设计的鉴别实验方案如下:
20℃时分别取NaNO2、NaCl各5.0g于两只小烧杯中,分别加入10mL水(水的密度近似看作1g/cm3),用玻璃棒充分搅拌后观察.你认为此方案是否可行
可行
可行
(填“可行”或“不可行”).②该小组其他同学又设计出与小明不同的实验方案,并获得成功.你认为该方案可能是
分别取少量的NaNO2、NaCl固体于两支试管中,用酒精灯加热,熔化者为NaNO2,不熔者为NaCl(或分别取少量样品于试管中,加水溶解,滴加无色酚酞试液,变红者为NaNO2,不变者为NaCl)(或其他合理答案)
分别取少量的NaNO2、NaCl固体于两支试管中,用酒精灯加热,熔化者为NaNO2,不熔者为NaCl(或分别取少量样品于试管中,加水溶解,滴加无色酚酞试液,变红者为NaNO2,不变者为NaCl)(或其他合理答案)
(只填写一种方案并简单叙述).小王同学对化学充满了兴趣,喜欢做各种实验.有一次他和其它同学对镁进行了一些研究:
【Ⅰ】他们用砂纸打磨掉表面灰黑色的物质,将其放入水中,未看到有明显的现象,改用酒精灯加热后,观察到表面有大量气泡,经验是氢气.他们又向溶液中滴加无色酚酞试液,发现酚酞变成红色,说明有
【Ⅱ】该小组成员开始研究镁带表面的灰黑色物质,小王大胆提出了三个假设:
假设1该物质是MgO;假设2该物质是Mg(OH)2;假设3镁可能会象铜一样生成碱式碳酸镁.
但其它同这立即否定了他的假设1和2,因为根据所学的知识MgO,Mg(OH)2都是
【III】他们在取镁带表面灰黑色样品时感到比较困难,索性将表面发黑的镁带全部磨成粉末,放入干燥的硬质试管中加热,一段时间后,镁粉突然出现红热燃烧起来,反应停止后有少量黑色物质A粘在试管壁上,这黑色物质A中混有什么?他们查资料筛选出几条有价值的信息:
(1)2Mg+CO2=2MgO+C; (2)C+2H2SO4(浓)=CO2↑+SO2↑+H2O;(3)SO2+Ca(OH)2=CaSO3↓(白)+H2O.
试分析A物质为
【Ⅳ】为验证碳和浓硫酸反应的三种产物,应将气体通过下列三种试剂(假设每步均完全)即:
气体→
(现象依次为)
【V】该兴趣小组的同学进一步又查出胃药碱式碳酸镁有多种不同的组成,如Mg2(OH)2CO3、Mg4(OH)2(CO3)3、Mg5(OH)2(CO3)4等.小红同学为确定碱式碳酸镁的组成,设计如图所示的实验:
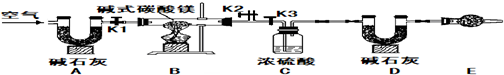
实验步骤(1)按图组装置后,首先进行的操作是
实验步骤(2)称取样品31g,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量为87.6g,装碱石灰的U型管D的质量为74.7g.
实验步骤(3)打开活塞
实验步骤(4)关闭活塞
实验步骤(5)打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,称得洗气瓶C的质量为89.4g,U型管D的质量为87.9g,则该碱式碳酸镁的化学式为
【Ⅵ】小明认为其化学式可用Mgx(OH)2(CO3)y表示,根据化合价规律,x和y的关系是
小明设计了两套方案(忽略装置中原来的气体)
方案I:只测定分解后生成的水,连接方案是A→C→B,则C中盛放的药品是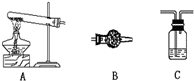
方案II:只测定分解生成的CO2的质量,连接方案是A→C→B→C,则B中的药品是
请你设计出更简单的实验方法
若取样品7.88克,方案I测得生成水0.36g,方案II测得生成CO2 3.52g,请你选择实验数据,通过计算得出碱式碳酸镁的化学式.
查看习题详情和答案>>
【Ⅰ】他们用砂纸打磨掉表面灰黑色的物质,将其放入水中,未看到有明显的现象,改用酒精灯加热后,观察到表面有大量气泡,经验是氢气.他们又向溶液中滴加无色酚酞试液,发现酚酞变成红色,说明有
OH-
OH-
产生.该实验表明化学反应的发生和速率与温度
温度
有关,许多物质的反应速度
反应速度
随温度的升高而增大.【Ⅱ】该小组成员开始研究镁带表面的灰黑色物质,小王大胆提出了三个假设:
假设1该物质是MgO;假设2该物质是Mg(OH)2;假设3镁可能会象铜一样生成碱式碳酸镁.
但其它同这立即否定了他的假设1和2,因为根据所学的知识MgO,Mg(OH)2都是
白
白
色固体.对于假设3,他们设计了如下方案| 实验方案 | 实验现象 | 实验结论 |
| 证明有CO32- | ||
| 取样于试管,加热 | 证明有氢元素 |
(1)2Mg+CO2=2MgO+C; (2)C+2H2SO4(浓)=CO2↑+SO2↑+H2O;(3)SO2+Ca(OH)2=CaSO3↓(白)+H2O.
试分析A物质为
C
C
,根据上述信息,他们又设计了下列实验,帮助他们完成实验报告:| 实验方案 | 实验现象 | 实验结论 |
| 取反应后试管内样品,先滴加过量的 稀硫酸 稀硫酸 |
固体部分溶解 | |
| 再 加热 加热 (填一具体的实验操作) |
黑色固体全部溶解 |
气体→
无水硫酸铜
无水硫酸铜
→高锰酸钾溶液
高锰酸钾溶液
→澄清石灰水
澄清石灰水
;(现象依次为)
白色固体变蓝
白色固体变蓝
、紫红色褪去
紫红色褪去
、澄清石灰水变浑浊
澄清石灰水变浑浊
【V】该兴趣小组的同学进一步又查出胃药碱式碳酸镁有多种不同的组成,如Mg2(OH)2CO3、Mg4(OH)2(CO3)3、Mg5(OH)2(CO3)4等.小红同学为确定碱式碳酸镁的组成,设计如图所示的实验:

实验步骤(1)按图组装置后,首先进行的操作是
检查装置的气密性
检查装置的气密性
.E处干燥管内盛放的药品是碱石灰
碱石灰
,其作用是防止空气中的水蒸气进入装置
防止空气中的水蒸气进入装置
.实验步骤(2)称取样品31g,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量为87.6g,装碱石灰的U型管D的质量为74.7g.
实验步骤(3)打开活塞
K1K2
K1K2
,关闭K3
K3
,缓慢鼓入空气数分钟.实验步骤(4)关闭活塞
K1K2
K1K2
,打开K3
K3
,点燃酒精灯加热至不再产生气体为止.实验步骤(5)打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,称得洗气瓶C的质量为89.4g,U型管D的质量为87.9g,则该碱式碳酸镁的化学式为
Mg4(OH)2CO3
Mg4(OH)2CO3
.【Ⅵ】小明认为其化学式可用Mgx(OH)2(CO3)y表示,根据化合价规律,x和y的关系是
x=y+1
x=y+1
,写出该物质分解的方程式:Mgx(OH)2(CO3)y
xMgO+H2O+yCO2↑
| ||
Mgx(OH)2(CO3)y
xMgO+H2O+yCO2↑
| ||
小明设计了两套方案(忽略装置中原来的气体)
方案I:只测定分解后生成的水,连接方案是A→C→B,则C中盛放的药品是
浓硫酸
浓硫酸
,B中盛放的药品是氯化钙固体
氯化钙固体

方案II:只测定分解生成的CO2的质量,连接方案是A→C→B→C,则B中的药品是
碱石灰
碱石灰
,最后连接的C中的药品是氢氧化钠溶液
氢氧化钠溶液
请你设计出更简单的实验方法
加热碱式碳酸镁称量反应前后固体质量
加热碱式碳酸镁称量反应前后固体质量
.若取样品7.88克,方案I测得生成水0.36g,方案II测得生成CO2 3.52g,请你选择实验数据,通过计算得出碱式碳酸镁的化学式.
小王同学对化学充满了兴趣,喜欢做各种实验.有一次他和其它同学对镁进行了一些研究:
【Ⅰ】他们用砂纸打磨掉表面灰黑色的物质,将其放入水中,未看到有明显的现象,改用酒精灯加热后,观察到表面有大量气泡,经验是氢气.他们又向溶液中滴加无色酚酞试液,发现酚酞变成红色,说明有______产生.该实验表明化学反应的发生和速率与______有关,许多物质的______随温度的升高而增大.
【Ⅱ】该小组成员开始研究镁带表面的灰黑色物质,小王大胆提出了三个假设:
假设1该物质是MgO;假设2该物质是Mg(OH)2;假设3镁可能会象铜一样生成碱式碳酸镁.
但其它同这立即否定了他的假设1和2,因为根据所学的知识MgO,Mg(OH)2都是______色固体.对于假设3,他们设计了如下方案
| 实验方案 | 实验现象 | 实验结论 |
| 证明有CO32- | ||
| 取样于试管,加热 | 证明有氢元素 |
(1)2Mg+CO2=2MgO+C; (2)C+2H2SO4(浓)=CO2↑+SO2↑+H2O;(3)SO2+Ca(OH)2=CaSO3↓(白)+H2O.
试分析A物质为______,根据上述信息,他们又设计了下列实验,帮助他们完成实验报告:
| 实验方案 | 实验现象 | 实验结论 |
| 取反应后试管内样品,先滴加过量的______ | 固体部分溶解 | |
| 再______ (填一具体的实验操作) | 黑色固体全部溶解 |
气体→______→______→______;
(现象依次为)______、______、______
【V】该兴趣小组的同学进一步又查出胃药碱式碳酸镁有多种不同的组成,如Mg2(OH)2CO3、Mg4(OH)2(CO3)3、Mg5(OH)2(CO3)4等.小红同学为确定碱式碳酸镁的组成,设计如图所示的实验:

实验步骤(1)按图组装置后,首先进行的操作是______.E处干燥管内盛放的药品是______,其作用是______.
实验步骤(2)称取样品31g,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量为87.6g,装碱石灰的U型管D的质量为74.7g.
实验步骤(3)打开活塞______,关闭______,缓慢鼓入空气数分钟.
实验步骤(4)关闭活塞______,打开______,点燃酒精灯加热至不再产生气体为止.
实验步骤(5)打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,称得洗气瓶C的质量为89.4g,U型管D的质量为87.9g,则该碱式碳酸镁的化学式为______.
【Ⅵ】小明认为其化学式可用Mgx(OH)2(CO3)y表示,根据化合价规律,x和y的关系是______,写出该物质分解的方程式:______
小明设计了两套方案(忽略装置中原来的气体)
方案I:只测定分解后生成的水,连接方案是A→C→B,则C中盛放的药品是______,B中盛放的药品是______

方案II:只测定分解生成的CO2的质量,连接方案是A→C→B→C,则B中的药品是______,最后连接的C中的药品是______
请你设计出更简单的实验方法______.
若取样品7.88克,方案I测得生成水0.36g,方案II测得生成CO2 3.52g,请你选择实验数据,通过计算得出碱式碳酸镁的化学式. 查看习题详情和答案>>