摘要:点燃镁粉或镁条可以产生耀眼的强光.写出该反应的化学方程式 .但厚度超过0.318cm的镁片却难以燃烧.为什么? .
网址:http://m.1010jiajiao.com/timu3_id_100524[举报]
点燃镁粉或镁条可以产生耀眼的强光,写出该反应的化学方程式___________________。但厚度超过0.318cm的镁片却难以燃烧,为什么?_________________________ 。
查看习题详情和答案>>
 甲、乙、丙三同学在学完了第二单元后,对测定空气中氧气含量的实验非常感兴趣,想探究能否用其它物质来代替红磷完成该实验.他们选取了以下几种物质:铁丝、硫粉、木炭、镁条(镁是一种金属).凭已有知识他们进行了讨论:
甲、乙、丙三同学在学完了第二单元后,对测定空气中氧气含量的实验非常感兴趣,想探究能否用其它物质来代替红磷完成该实验.他们选取了以下几种物质:铁丝、硫粉、木炭、镁条(镁是一种金属).凭已有知识他们进行了讨论:(1)甲同学首先认为不能用铁丝代替红磷.他的理由是
铁丝在空气中不能燃烧
铁丝在空气中不能燃烧
.(2)乙同学认为也不能用硫粉、木炭代替红磷.他的理由是
产生的气体占据了消耗掉的氧气的空间,压强不变
产生的气体占据了消耗掉的氧气的空间,压强不变
.(3)丙同学在认真思考乙同学的理由后认为,如果要用木炭来代替红磷而且实验要获得成功必须作一点小小的改进,他预先在集气瓶中装了一种物质,结果他实验成功了,你认为他预先在集气瓶中装的物质是
氢氧化钠溶液
氢氧化钠溶液
.(4)对于镁条三同学凭已有的知识无法判断,他们于是进行了如下的探究:
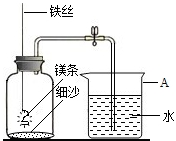
他们用如图所示装置和光亮镁条进行实验,将镁条点燃后迅速放入瓶中燃烧,观察到镁条发出耀眼的白光,有白色粉末状物质产生,冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%(实验过程中所有操作都是正确的)
(5)冷却后水能进入集气瓶中的原因是
消耗了瓶内的气体,使压强变小,外界大气压将水压入瓶中
消耗了瓶内的气体,使压强变小,外界大气压将水压入瓶中
为了让实验取得成功,该同学进行实验时的第一步是检查装置的气密性
检查装置的气密性
.在进行实验时,为了使镁条变得光亮他应进行的操作是用砂纸打磨
用砂纸打磨
.(6)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多超过其容积的五分之一,现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气.问题:氮气为什么减少呢?假设一:氮气与瓶内其它物质反应而减少.假设二:
氮气与镁条反应而减少
氮气与镁条反应而减少
. 通过以上实验你认为能否用镁条代替红磷测定空气中氧气含量(填:“能”或“不能”)不能
不能
.(7)根据他们的讨论和本探究实验实验,你认为选择测定空气中氧气含量实验的药品应满足的条件是
能把氧气反应掉
能把氧气反应掉
、不能与空气中的其它成分反应
不能与空气中的其它成分反应
、不生成新的气体杂质
不生成新的气体杂质
.甲、乙、丙三同学在学完了第二单元后,对测定空气中氧气含量的实验非常感兴趣,想探究能否用其它物质来代替红磷完成该实验.他们选取了以下几种物质:铁丝、硫粉、木炭、镁条(镁是一种金属).凭已有知识他们进行了讨论: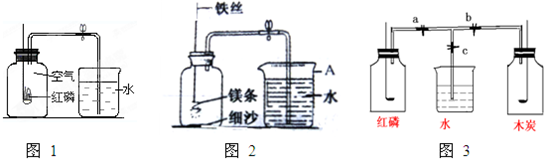
(1)甲同学首先认为不能用铁丝代替红磷.他的理由是
(2)乙同学认为也不能用硫粉、木炭代替红磷.他的理由是
(3)丙同学在认真思考乙同学的理由后认为:如果要用木炭来代替红磷而且实验要获得成功必须作一点小小的改进,他预先在集气瓶中装了一种物质,结果他实验成功了,你认为他预先在集气瓶中装的物质是
(4)对于镁条三同学凭已有的知识无法判断,他们于是进行了如下的探究:
他们用如图2所示装置和光亮镁条进行实验,将镁条点燃后迅速放入瓶中燃烧,观察到镁条发出耀眼的白光,有白色粉末状物质产生,冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%(实验过程中所有操作都是正确的)
冷却后水能进入集气瓶中的原因是
(5)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多超过其容积的五分之一,现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气.问题:氮气为什么减少呢?假设一:氮气与瓶内其它物质反应而减少.假设二:
(6)已知空气中氧气的体积分数为21%,小兰同学用如图3装置进行验证,实验后发现测得的氧气体积分数小于
,请你帮她分析造成这种结果的可能原因(至少答两点):
(7)关闭止水夹a、b、c,使过量的红磷和木炭分别在盛有空气的等容积的甲、乙两瓶中同时燃烧,如图所示,试回答:
①燃烧停止并冷却,若打开止水夹a、c后观察到的现象是
②若打开止水夹b、c后观察到的现象是
③若打开止水夹a、b、c后观察到的现象是
查看习题详情和答案>>

(1)甲同学首先认为不能用铁丝代替红磷.他的理由是
铁丝在空气中不能燃烧
铁丝在空气中不能燃烧
.(2)乙同学认为也不能用硫粉、木炭代替红磷.他的理由是
产生的气体占据了消耗掉的氧气的空间,压强不变
产生的气体占据了消耗掉的氧气的空间,压强不变
.(3)丙同学在认真思考乙同学的理由后认为:如果要用木炭来代替红磷而且实验要获得成功必须作一点小小的改进,他预先在集气瓶中装了一种物质,结果他实验成功了,你认为他预先在集气瓶中装的物质是
氢氧化钠溶液
氢氧化钠溶液
.(4)对于镁条三同学凭已有的知识无法判断,他们于是进行了如下的探究:
他们用如图2所示装置和光亮镁条进行实验,将镁条点燃后迅速放入瓶中燃烧,观察到镁条发出耀眼的白光,有白色粉末状物质产生,冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶容积的70%(实验过程中所有操作都是正确的)
冷却后水能进入集气瓶中的原因是
消耗了瓶内的气体,使压强变小,外界大气压将水压入瓶中
消耗了瓶内的气体,使压强变小,外界大气压将水压入瓶中
为了让实验取得成功,该同学进行实验时的第一步是检查装置的气密性
检查装置的气密性
.在进行实验时,为了使镁条变得光亮他应进行的操作是用砂纸打磨
用砂纸打磨
.(5)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多超过其容积的五分之一,现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气.问题:氮气为什么减少呢?假设一:氮气与瓶内其它物质反应而减少.假设二:
氮气与镁条反应而减少
氮气与镁条反应而减少
. 通过以上实验你认为能否用镁条代替红磷测定空气中氧气含量(填:“能”或“不能”)不能
不能
(6)已知空气中氧气的体积分数为21%,小兰同学用如图3装置进行验证,实验后发现测得的氧气体积分数小于
| 1 | 5 |
气密性不好
气密性不好
,红磷量不足.
红磷量不足.
(7)关闭止水夹a、b、c,使过量的红磷和木炭分别在盛有空气的等容积的甲、乙两瓶中同时燃烧,如图所示,试回答:
①燃烧停止并冷却,若打开止水夹a、c后观察到的现象是
水进入左瓶中
水进入左瓶中
;②若打开止水夹b、c后观察到的现象是
水不会进入右瓶中
水不会进入右瓶中
;③若打开止水夹a、b、c后观察到的现象是
水进入两个集气瓶中
水进入两个集气瓶中
,原因是气体总体积减小,压强变小
气体总体积减小,压强变小
.