湖南省雅礼中学2009届高三第六次月考试卷
理科综合
雅礼中学理科综合组
本试卷分第I卷(选择题)和第II卷(非选择题)两部分。共300分。考试时间150分钟
第I卷(选择题 共126分)
注意事项:
1.答题前,考生务必将自己的姓名、准考证号填在试题卷的答题卡上,并认真核对号码。
2.每小题选出答案后,用2B铅笔把答题卡上对应的答案标号涂黑。如果需要改动,用橡皮擦干净后,再选涂其它答案标号。答在试题卷上答案视为无效。
可能用到的相对原子质量:
Na
一、选择题(本题包括13道小题,每小题只有一个选项符合题意;每小题6分,共78分)
1.下列有关生命的物质基础和结构基础的阐述,不正确的是
A.ATP、染色质、质粒、磷脂共有的化学元素包括C、H、O、N、P
B.洋葱根尖分生区的细胞中,把二磷酸腺苷转变成三磷酸腺苷的酶只分布在线粒体中。
C.正常的男性体细胞的所有染色体可以表示为44+XY,则21三体综合征的女患者的体细胞的所有染色体可以表示为45+XX
D.糖蛋白、抗体、RNA聚合酶、限制性内切酶都是具有识别作用的物质
2.某生物的基因型为AaBB,通过下列技术可以分别将它转变为以下基因型的生物:①AABB;②aB;③AaBBC;④AAaaBBBB。则以下排列正确的是
A.诱变育种、转基因技术、花药离体培养、细胞融合
B.杂交育种、花药离体培养、转基因技术、多倍体育种
C.花药离体培养、诱变育种、多倍体育种、转基因技术
D.多倍体育种、花药离体培养、诱变育种、转基因技术
3.某些细菌在生长过程中不断向菌体外分泌外毒素,其成分为蛋白质。下列说法正确的是
A.控制细菌外毒素合成的基因编码区由外显子和内含子构成
B.细菌外毒素的分泌与高尔基体活动密切相关
C.对数期细菌快速增长,积累的外毒素最多
D.进入人体内的细菌外毒素主要引起机体体液免疫
4. 对下列四幅图的描述正确的是
对下列四幅图的描述正确的是
A.图1中a阶段X射线照射可诱发突变,b阶段用秋水仙素能抑制纺锤体的形成
B.图2中的温度在a时酶分子结构改变、活性较低
C.图3中bc段和de段的变化都会引起C3化合物含量的下降
D.图4中造成cd段下降的原因在有丝分裂和减数分裂中是不同的
5 .某生物小组为了解某生态系统的食物网组成,对其中动物的胃进行解剖,其结果如下表所示。已知甲为该生态系统中的生产者。
|
 8.下图
8.下图 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞
试液的滤纸,
为浸透饱和氯化钠溶液和酚酞
试液的滤纸, 为电镀槽。接通电路后发现
为电镀槽。接通电路后发现 后,使c、d两点短路。下列叙述正确的是
后,使c、d两点短路。下列叙述正确的是  9.如右图,向A充入1molX、1molY,向B中充入2molX、2molY,起始时A、B的体积相等都等于a L,在相同温度和催化剂存在的条件下,关闭活塞K,使两容器中各自发生下述反应,X(g)+Y(g)
9.如右图,向A充入1molX、1molY,向B中充入2molX、2molY,起始时A、B的体积相等都等于a L,在相同温度和催化剂存在的条件下,关闭活塞K,使两容器中各自发生下述反应,X(g)+Y(g) 2Z(g)+W(g);ΔH<0。A保持恒压,B保持恒容,达平衡时,A的体积为1.4aL。下列说法错误的是
2Z(g)+W(g);ΔH<0。A保持恒压,B保持恒容,达平衡时,A的体积为1.4aL。下列说法错误的是 B.
B.
 D.
D.
 15.如图所示,小车上有一个定滑轮,跨过定滑轮的绳一端系一重球,另一端系在弹簧秤上,弹簧秤固定在小车上.开始时小车处于静止状态。当小车匀加速向右运动时,下述说法中正确的是:
15.如图所示,小车上有一个定滑轮,跨过定滑轮的绳一端系一重球,另一端系在弹簧秤上,弹簧秤固定在小车上.开始时小车处于静止状态。当小车匀加速向右运动时,下述说法中正确的是:  °,在整个AC面上有一束垂直于AC的平行光线射入,已知这种介质的折射率n>2 ,则( )
°,在整个AC面上有一束垂直于AC的平行光线射入,已知这种介质的折射率n>2 ,则( ) A.可能有光线垂直AB面射出
A.可能有光线垂直AB面射出  17、质量相等的A、B两球之间压缩一根轻弹簧,静置于光滑水平桌面上。当用板挡住小球A而只释放B球时,B球被弹出落于距桌边距离为s的水平地面上,如图所示。问当用同样的程度压缩弹簧,取走A左边的挡板,将A、B同时释放,B球的落地点距桌边距离
17、质量相等的A、B两球之间压缩一根轻弹簧,静置于光滑水平桌面上。当用板挡住小球A而只释放B球时,B球被弹出落于距桌边距离为s的水平地面上,如图所示。问当用同样的程度压缩弹簧,取走A左边的挡板,将A、B同时释放,B球的落地点距桌边距离 B.
B.
 C.s D.
C.s D.
 两根光滑的金属导轨,平行放置在倾角为θ的斜面上,导轨的左端接有电阻为R,导轨自身的电阻可忽略不计,斜面处在一匀强磁场中,磁场方向垂直于斜面向上、质量为m、电阻可不计的金属棒ab,在沿着斜面,与棒垂直的恒力F的作用下沿导轨匀速上滑,并上升h高度,如图所示,在这过程中
两根光滑的金属导轨,平行放置在倾角为θ的斜面上,导轨的左端接有电阻为R,导轨自身的电阻可忽略不计,斜面处在一匀强磁场中,磁场方向垂直于斜面向上、质量为m、电阻可不计的金属棒ab,在沿着斜面,与棒垂直的恒力F的作用下沿导轨匀速上滑,并上升h高度,如图所示,在这过程中  21.
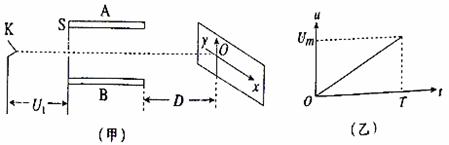
21. 介子衰变的方程为
介子衰变的方程为 ,其中
,其中 介子和
介子和 介子带负的元电荷e,π0介子不带电.如图所示,两匀强磁场方向相同,以虚线MN为理想边界,磁感应强度分别为B1、B2.今有一个
介子带负的元电荷e,π0介子不带电.如图所示,两匀强磁场方向相同,以虚线MN为理想边界,磁感应强度分别为B1、B2.今有一个 介子沿v反方向射出,其运动轨迹为如图虚线所示的“心”形图线.则以下说法正确的是
介子沿v反方向射出,其运动轨迹为如图虚线所示的“心”形图线.则以下说法正确的是
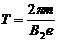
 (1)(6分) 研究电磁感应现象的实验中,采用了如图所示的装置,当滑动变阻器R的滑片P不动时,甲、乙两个相同的电流表指针的位置如图所示,当滑片P较快地向a滑动时,两表指针的偏转方向是( )
(1)(6分) 研究电磁感应现象的实验中,采用了如图所示的装置,当滑动变阻器R的滑片P不动时,甲、乙两个相同的电流表指针的位置如图所示,当滑片P较快地向a滑动时,两表指针的偏转方向是( )
 电流表A1:量程100mA,内阻r1约为4Ω;
电流表A1:量程100mA,内阻r1约为4Ω;  ,导轨右端连接一阻值为
,导轨右端连接一阻值为 的小灯泡L。在CDEF矩形区域内有竖直向上的匀强磁场,磁感应强度B随时间t变化如图乙所示,CF长为
的小灯泡L。在CDEF矩形区域内有竖直向上的匀强磁场,磁感应强度B随时间t变化如图乙所示,CF长为 时刻,电阻为
时刻,电阻为 的金属棒ab在水平恒力F作用下,由静止开始沿导轨向右运动。金属棒从图中位置运动到EF位置的整个过程中,小灯泡的亮度始终没有发生变化。求:
的金属棒ab在水平恒力F作用下,由静止开始沿导轨向右运动。金属棒从图中位置运动到EF位置的整个过程中,小灯泡的亮度始终没有发生变化。求: (2)恒力F的大小;
(2)恒力F的大小; (3)若t=时,将该粒子从MN板右侧沿板的中心线O2O1,仍以速率v0射入M、N之间,求粒子从磁场中射出的点到P点的距离.
(3)若t=时,将该粒子从MN板右侧沿板的中心线O2O1,仍以速率v0射入M、N之间,求粒子从磁场中射出的点到P点的距离. 4ClO2↑+O2↑+2H2O,从反应原理看,应在酸性条件下进行,能否用盐酸来调节溶液的酸性?
4ClO2↑+O2↑+2H2O,从反应原理看,应在酸性条件下进行,能否用盐酸来调节溶液的酸性?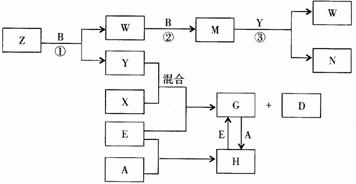
 _____7,其原因是____________________________________________________。
_____7,其原因是____________________________________________________。 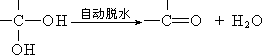


 (2)A、1.010
(2)A、1.010
 ,I1、I2分别为电流表A1、A2的读数,r2为电流表A2的内阻。(4分)
,I1、I2分别为电流表A1、A2的读数,r2为电流表A2的内阻。(4分) (2分)
(2分) ① (2分)
① (2分) V ②
(2分)
V ②
(2分) A
③ (2分)
A
③ (2分) s末金属棒刚好进入磁场,且做匀速运动,
s末金属棒刚好进入磁场,且做匀速运动, A
④ (2分)
A
④ (2分) N
⑤ (2分)
N
⑤ (2分)
 V ⑥ (2分)
V ⑥ (2分) m/s
⑦ (2分)
m/s
⑦ (2分) m/s2
⑧ (2分)
m/s2
⑧ (2分) kg
⑨ (2分)
kg
⑨ (2分) ①(2分)
①(2分) ②(2分)
②(2分)
 ⑤(4分)
⑤(4分) (n=1,2,…) ⑥(2分)
(n=1,2,…) ⑥(2分) (n=1,2,…) ⑦(2分)
(n=1,2,…) ⑦(2分) 2Z(g)+W(g)
2Z(g)+W(g) CH3Cl+HCl CH3Cl+Cl2
CH3Cl+HCl CH3Cl+Cl2 5N2+6H2O;
5N2+6H2O; (2)醛基
(或-CHO)和羧基(-COOH)(对1个给1分,共2分); 4步
; 取代反应(或水解反应)
(2)醛基
(或-CHO)和羧基(-COOH)(对1个给1分,共2分); 4步
; 取代反应(或水解反应)
 2HCHO+2H2O
2HCHO+2H2O
 +H2O(注意加热条件、配平、小分子等的规范)
+H2O(注意加热条件、配平、小分子等的规范) (NH4)2CO3+2Ag↓+2NH3↑+H2O(氧化产物写成CO2、H2CO3或NH4HCO3、HOCOONH4均可以)
(NH4)2CO3+2Ag↓+2NH3↑+H2O(氧化产物写成CO2、H2CO3或NH4HCO3、HOCOONH4均可以) C
C  ;
; C
C 