海门实验学校08―09年度第一学期高二年级期中考试
化学试题(必修)
命题人:吴一平 2008-10-30
1、本试题供非化学班学生使用;满分100,答题时间为60分钟。
2、请将第Ⅰ卷选择题答案填入答题卡中,第Ⅱ卷非选择题答案直接填在试卷上。
第Ⅰ卷(选择题 共69分)
一、选择题(每小题只有一个答案正确,每小题3分,共69分)。
1.日常生活中食用的白糖、冰糖和红糖的主要成分是
A、淀粉 B、葡萄糖 C.蔗糖 D、果糖
2.下列物质不能发生水解反应的是
A.油脂 B.麦芽糖 C.葡萄糖 D.蛋白质
3.欲将蛋白质从水中析出而又不改变它的性质应加入
A、甲醛溶液 B、饱和Na2SO4溶液 C、CuSO4溶液 D、浓硫酸
4.缺铁会引起下列哪些症状:
A.侏儒症 B、骨质疏松症 C、甲亢 D、贫血
5.关于食物的酸碱性,下列说法正确的是( )
A、食物溶于水后的溶液中PH小于7,则为成酸性食物
B、由碳、氮、硫、磷等元素组成的蛋白质是成酸性食物
C、蔬菜、水果多含钾、钠、钙、镁等盐类,习惯称为酸性食物
D、柠檬酸是酸性食物
6.关于平衡膳食宝塔的认识中,正确的是
A、塔底的食物最重要 B、塔顶的食物最重要
C、膳食宝塔所列食物摄入量对任何人都是最佳摄入量
D、膳食宝塔所列食物摄入量是每人每日的建议摄入量,具体到不同的个体要根据自身的情况而调整
7.对于药品的使用和作用,下列说法不正确的是( )
A、R表示处方药,OTC表示非处方药
B、青霉素有阻止多种细菌生长的优异功能,虽经1×107 倍稀释,仍有疗效
C、阿司匹林是一种白色晶体,不溶于水
D、中草药麻黄碱可用于治疗失眠、多梦等症状
8.钛和钛的合金被认为是21世纪的重要材料,它们具有很多优良的性能,如熔点高、密度小、可塑性好、易于加工,钛合金与人体有很好的“相容性”。根据它们的主要性能,下列用途不切合实际的是
A.用来做保险丝 B.用于制造航天飞机
C.用来制造人造骨 D.用于制造汽车、船舶
9.在面盆、痰盂等铁制品表面烧制搪瓷的目的是
A、增大厚度防止磨损 B、美观和杀菌消毒作用
C、增大硬度防止撞坏 D、防止铁生锈且美观
10.普通玻璃的主要成分是
①Na2SiO3 ②CaCO3 ③CaSiO3 ④SiO2 ⑤Na2CO3 ⑥CaO
A. ①③⑥ B.②③④ C. ①③④ D.③④⑤
11.下列有关材料的组成或结构的表示中,正确的是 ( )
A.光导纤维:SiO2
B.陶瓷:由Na2SiO3、CaSiO3、SiO2组成的混合物
C.包装食品的塑料: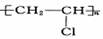
D.天然橡胶:
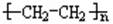
12.化工塑料PVC指的是
A、聚氯乙烯 B、聚丙烯 C、聚丙烯腈 D、聚乙烯
13.下列有关环境保护的叙述中,错误的是 ( )
A.含氮、磷化合物的生活污水大量排放可使水体富营养化
B.工业大量排放二氧化氮是全球气候变暖的主要原因
C.某些装修材料中含有的甲醛、苯等会严重影响人体健康
D.废旧电池中含有的汞、铅、镉等重金属盐对土壤和水源会造成污染
14.下列家庭化学小实验不能达到预期目的的是:
A.用米汤检验食用加碘盐(含KIO3)中含有碘
B.用醋、石灰水验证蛋壳中含有碳酸盐
C.用碘酒检验汽油中是否含有不饱和烃
D.用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验
15.水资源非常重要,联合国确定2003年为国际淡水年。下列关于水的说法中错误的是
A.蒸馏法是海水淡化的方法之一
B.淡水的密度小于海水的密度
C.生活饮用水与饮用纯净水的水质卫生标准相同
D.长期饮用纯净水,有可能引起一些微量元素的缺乏症
16.下列四种垃圾处理方法中,较为合理的是 ( )
A.堆积 B.填理 C.分类回收 D.焚烧
17.下列属于油脂的用途的是 ( )
①人类的营养物质 ②制取肥皂 ③制取甘油 ④制备高级脂肪酸 ⑤制备汽油
A.①②③ B.①③⑤ C.②③④⑤ D.①②③4
18.下列食品添加剂与类别对应正确的一组是( )
A、着色剂 ----- 苯甲酸钠 B、营养强化剂 ----- 粮食制品中加赖氨酸
C、调味剂 ------ 亚硝酸钠 D、防腐剂 ------ 柠檬黄
19.我国及美国、日本等国家都已研制出了一种陶瓷柴油机,这种柴油机的发动机部件的受热面是用一种耐高温且不易传热的材料来制造的,这种材料是
A.普通硅酸盐陶瓷 B.氮化硅陶瓷? C.光导纤维 D.玻璃钢
20.长期吸食或注射毒品会危及人体健康,下列各组中都属于毒品的是
A.冰毒、黄连素 B.海洛因、黄连素
C.大麻、摇头丸 D.黄曲霉素、尼古丁
21.下列拟采用的金属防腐措施,错误的是 ( )
A.给金属衣架或电线外面包上一层塑料层 B.给自行车钢圈镀上一层金属铬
C.将铁闸门与直流电源正极相连 D. 给铁栅栏表面涂上一层油漆
22.下列对于人体健康的有关说法中,错误的是 ( )
A.必须严格控制人体必需的碘、锌等元素的摄入量
B.糖类、油脂、蛋白质、维生素、无机盐和水是人需要的主要营养素
C.“是药三分毒”,必须按医嘱或药物说明书使用药物,防范药物不良反应
D.着色剂、调味剂、防腐剂等食品添加剂,可改善食品的色、味,多用有益
23.市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣物的汗渍、血迹以及人体排放的蛋白质油渍遇到它,都能水解而被除去,下列衣料中不能用及酶洗衣粉洗涤的是 ( )
①棉织品 ②毛织品 ③腈纶制品 ④蚕丝制品 ⑤涤纶制品 ⑥锦纶制品
A.①②③ B.②④ C.③④⑤ D.③⑤⑥
 第Ⅱ卷 (非选择题 满分31分)
第Ⅱ卷 (非选择题 满分31分)
二、填空题(本题包括3小题;共15分)。
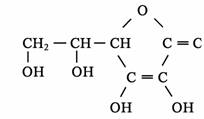
24.(5分)(1)右图是维生素C的结构,它是一种水溶性的维生素,缺乏VC会使人患上 病。切取一片新鲜水果,向切面上滴加淀粉溶液和碘水,若出现 ,说明新鲜水果中含有VC,这是利用VC具有 (填“氧化”或“还原”)性。
(2)为验证某易拉罐材质的主要成分是铁制还是铝制,如用物理方法验证,一般用
即可;如用化学方法验证,可使用的化学试剂为 。
25.(4分)下表是某地区市场上销售的一种“加碘食盐”包装袋上的部分文字说明。请根据此表,结合化学和生物学科的知识,回答下列问题。
配料表
精制海盐、碘酸钾
含碘量
20~40mg/kg
卫生许可证号
××卫碘字(1999)第001号
分装日期
见封底
储藏方法
密封、避光、防潮
食用方法
烹调时,待食品熟后加入碘盐
(1)要在食盐中加碘,是因为碘是人体内合成______________激素的主要原料,缺碘会引起疾病。
(2)食盐中加碘,这碘指的是 ,其中碘元素的化合价为__________。
(3)根据含碘盐的食用方法,可推测碘酸钾在受热时容易___________________。
26.(6分)生活处处有化学,化学与生产、生活密切相关。请回答:
(1)淀粉的化学式是: ;黄铜是生活中常用的金属材料,它是铜和_______的合金;油脂在体内水解后的产物是:
(2)据报道,全世界每年因金属腐蚀造成的直接经济损失约达7000亿美元,我国因金属腐蚀造成的损失占国民生产总值(GNP)的4%。钢铁在潮湿的空气中发生电化学腐蚀时,负极的电极反应式为 。
(3)乙酰水杨酸(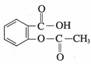 )的俗名为阿司匹林,是常用的解热镇痛药。它遇水能缓慢地水解生成水杨酸,则水杨酸的结构简式可表示为 。
)的俗名为阿司匹林,是常用的解热镇痛药。它遇水能缓慢地水解生成水杨酸,则水杨酸的结构简式可表示为 。
(4)聚苯乙烯是造成白色污染的物质之一,其结构简式为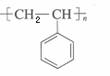 ,则制取聚苯乙烯的单体是
。
,则制取聚苯乙烯的单体是
。
三、填空题(本题包括2小题;共16分)。
27.(8分)用化学方程式表示酸雨的形成过程:
、 , 。
为了降低硫氧化物造成的空气污染,一种方法是在含硫燃料(如煤)燃烧过程中加入生石灰,这种方法叫“钙基固硫”,采用这种方法在燃料燃烧过程中的“固硫”反应为:____ _____________________________________________________________________。
28.(8分)某综合实践活动小组到自来水厂进行参观,了解到源水处理成自来水的工艺流程示意图如下:
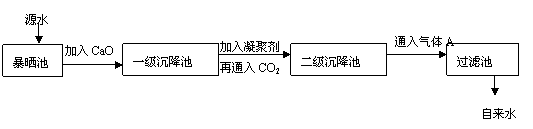
(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入CaO后生成Ca(OH)2,进而发生若干复分解反应,试写出其中的一个离子方程式 。
(2)加入凝聚剂可以除去其中的悬浮固体颗粒,其过程是 。(填写下列各项的序号)
①只有物理过程,无化学过程
②只有化学过程,无物理过程
③既有化学过程又有物理过程
(3)FeSO4?7H2O是常用的凝聚剂,加入后,最终生成红褐色胶状沉淀,则这种红褐色胶状沉淀是 。
(4)下列物质中, 可以作为消毒剂。(填写下列各项的序号)
①ClO2 ②浓氨水 ③SO2 ④浓硫酸
海门实验学校08―09年度第一学期高二年级期中考试
化学试题(必修)答题纸
二、填空题(本题包括3小题;共15分)。
24.(5分)
(1)患上 病。若出现 ,说明VC具有 性。
(2)一般用 即可;化学试剂为 。
25.(4分)
(1)因为碘是人体内合成_____________________激素的主要原料。
(2)食盐中加碘,这碘指的是 ___ ,其中碘元素的化合价为__________。
(3)推测碘酸钾在受热时容易___________________。
26.(6分)
(1)淀粉的化学式是: ;黄铜是铜和__________的合金;油脂在体内水解后的产物是: _____
(2)负极的电极反应式为 。
(3)水杨酸的结构简式可表示为 。
(4)制取聚苯乙烯的单体是 。
三、填空题(本题包括2小题;共16分)。
27.(8分)用化学方程式表示酸雨的形成过程:
_ ___________________ 、
___ ________________________ ,
____________________ 。
“固硫”反应为:_____________________________________ _______。
28.(8分)
(1)试写出其中的一个离子方程式 。
(2)其过程是 。(填写下列各项的序号)
(3)这种红褐色胶状沉淀是 。
(4)下列物质中, 可以作为消毒剂。(填写下列各项的序号)
海门实验学校08―09年度第一学期高二年级期中考试
第Ⅰ卷 (选择题 69 分)
选择题答案卡:(1 ~ 23题,每小题3分,)
题号
1
2
3
4
5
6
7
8
9
10
答案
C
C
B
D
B
D
D
A
D
C
题号
11
12
13
14
15
16
17
18
19
20
答案
A
A
B
A
C
C
D
B
B
C
题号
21
22
23
答案
C
D
B
第Ⅱ卷 (非选择题 31分)
24.(5)坏血、褪色、还原(2)磁铁是否能吸引、氢氧化钠溶液 (各1分)
25.(4分)(1)甲状腺 (2)KIO3 +5 (3)分解 (各1分)
26.(6分)(1) (C6H10O5)n
;、锌(Zn);高级脂肪酸和甘油。(2)Fe-2e―=Fe2+ (3)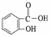 (4)
(4)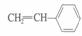 (各1分)
(各1分)
27.(8分)SO2 + H2O = H2SO3 ;2H2SO3 + O2 = 2H2SO4 ;3NO2 + H2O====2HNO3+NO
2SO2 + 2CaO + O2 == 2CaSO4 (每空2分)
28.(共8分,每空2分)
(1)只要写出下列4个离子方程式中的任意一个,即可给2分。

 HCO-3+OH- CO2-3+H2O;Ca2++CO32-+OH- CaCO3↓+H2O;
HCO-3+OH- CO2-3+H2O;Ca2++CO32-+OH- CaCO3↓+H2O;
 Ca2++2HCO-3+2OH- CaCO3↓+CO32-+2H2O;
Ca2++2HCO-3+2OH- CaCO3↓+CO32-+2H2O;
 Mg2++2OH- Mg(OH)2↓
Mg2++2OH- Mg(OH)2↓
(2)③; (3)Fe(OH)3 (4)①