2009-2010学年度烟台招远第一学期九年级第二学段测评
化学试题
同学你好!一个学期的化学学习你一定会感觉到化学世界的奇妙,体验到生活中处处有化学,你的收获一定有很多,请仔细审题,认真解答,将你的收获展示出来。
可能用到的信息――元素周期表(部分)

说明:
1.请将选择题答案填在第Ⅱ卷的答案表内,测试结束后,只收Ⅱ卷。
2.答卷前请将自己的学校、班级、姓名填在密封线内。
第Ⅰ卷(选择题,20小题,共30分)
一、选择题(本题包括10个小题。每小题只有一个正确答案)
1.大力提倡“绿色化学”是消除污染的根本手段,下列措施中属于“绿色化学”范畴的是
A.处理废弃物 B.治理污染点
B.治理污染点
C.减少有毒物 D.杜绝污染源
2.下列做法不会危及人体健康的是
A.把霉变大米淘净后继续食用
B.用甲醛水溶液浸泡水产品
C.用聚乙烯做食品包装袋
D.人体中缺乏钙、铁、碘元素会引起疾病,饮食中摄人的越多越好
3.小明奶奶为他迎接期末考试,制定了如下食谱:米饭、红烧鸡、蛋汤、糖醋鱼、麻辣豆腐。为使营养均衡,你觉得最好还要补充
A.牛肉 B.河虾 C.青菜 D.雪糕
4.空气污染指数是我国城市空气质量日报的主要内容之一。目前计入其中的各项污染物除可吸入颗粒外,还包括的气体是
A.SO2 O2 NO2 B.SO2 CO2 NO2
C.SO N 2 NO2 D.SO2 CO NO2
5.卫生部颁发的《食品添加剂使用卫生标准》从
A.炖肉时加一点亚硝酸钠可使肉易熟
B.做馒头发面时加入适量的碱面
C.食用驴肉汤包时蘸上香醋
D.在煲好的骨头汤中放人适量加碘食盐
6.浩瀚无际的海洋为人类提供了丰富的资源。由海水制备金属镁,主要有以下步骤:①电解熔融的氯化镁;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是
A.②④⑤③① B.③②④①⑤
C.③④②⑤① D.②④③⑤①
7.下图是一幅贴在汽车加油站的宣传广告。以下叙述错误的是
A.玉米汁可用作汽车燃料
B.由玉米生产的酒精可作汽车燃料
C.推广玉米生产的燃料可在一定程度上缓解当前的能源危机
D.以农作物为原料来生产化学品是可行的

8.2009年是一个“气候变化年”。
A.化石燃料燃烧排放的二氧化硫是导致温室效应的主要物质
B.温室效应是导致地球温度升高的主要因素之一
C.冰川融化,造成海平面上升,给人类生存带来威胁
D.建环境友好型社会要减少化石燃料的使用,开发使用新型能源
9.化学与生活、社会密切相关。下列说法不正确的是
A.不吃水果蔬菜,多吃含蛋白质的肉类,更能增强体质
B.购物时减少使用或不用塑料袋,是为了减少“白色污染”
C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
D.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
10.下图是某菜农使用化肥包装袋上的部分说明,该化肥属于
A.氮肥 B.磷肥 C.钾肥 D.复合肥料
B.磷肥 C.钾肥 D.复合肥料

二、选择题(本题包括10个小题,每小题有1个或2个选项符合题意)
11.日常生活中的一些小窍门或小常识往往包含着一些化学原理。下列做法正确的是
①油锅着火时迅速用锅盖覆盖灭火 ②用钢丝球擦洗铝锅上的污垢
③用热的纯碱水洗涤铁锅上的油污 ④煤气泄漏及时打开换气扇排气
A.①② B.①③ C.②③ D.②④
12.为验证Mg、Cu、Ag三种金属的活动性强弱。某化学兴趣小组设计了下图所示的四个实验。其中不必进行的实验是




13.甲、乙两种固体物质的溶解度曲线如下图。下列说法正确的
A.甲物质的溶解度为
B.t℃时,甲、乙两物质的溶解度相等
C.升高温度可使不饱和的甲溶液变为饱和溶液
D.t℃乙物质的饱和溶液降到

14.在甲溶液中滴加几滴石蕊试液,溶液呈蓝色;然后再滴加乙溶液,当滴至甲、乙两物质正好完全反应时,溶液呈紫色;再继续滴加乙溶液时,溶液呈红色。在上述过程中,表示溶液的
pH(纵坐标)与滴加乙溶液的体积V(横坐标)之间的关系的正确图像是

15.北京奥运会吉祥物――“福娃”向世界传递着友谊、和平、积极进取的精神。为儿童安全考虑,有一种“福娃”的外用材料为纯羊毛线,内充物为无毒的聚酯纤维。下列说法正确的是
A.羊毛的主要成分为纤维素
B.这种“福娃”不宜用碱性强的洗涤剂清洗
C.聚酯纤维是天然高分子材料午
D.可以用燃烧的方法区分羊毛和聚酯纤维
16.及时对知识进行分类归纳,是一种重要的学习方法。下面是小洁同学以连线方式对相关主题知识进行归纳的情况,其中完全正确的是
A.化学与健康 人体缺碘――会引起大脖子病 人体缺锌――会影响人体发育人体缺铁――会引起贫血症
B.物质的性质与用途 氢氧化钙能中和酸――可用来改良酸性土壤氧气支持燃烧――可用作燃料食盐溶于水后溶液凝固点降低――可作融雪剂
C.安全常识 误服少量重金属盐溶液――立即喝鲜奶使用燃煤炉子取暖――注意室内通风不慎将浓硫酸沾到皮肤上――立即用大量氢氧化钠溶液冲洗
D.化学与能源 煤、石油、天然气――不可再生的化石燃料风能、水能、太阳能――未充分利用的绿色能源干电池――化学能转化为电能的装置
17.淀粉酶可以将人体不能直接吸收的淀粉转变成易吸收的小分子物质。下图是淀粉酶对淀粉作用过程的示意图,对该过程的表述不正确的是
A.酶起催化作用 B.是物理变化
C.是化学变化 D.酶的化学性质发生了改变

18.为解决日益加剧的温室效应等问题,科学家正在研究建立如下图所示的二氧化碳新循环体系:
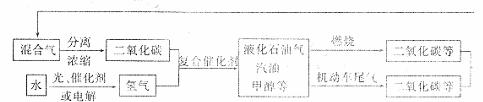
上述关系图能反映的化学观点或化学思想有:
①化学变化中元素种类是守恒的;
②燃烧时化学能可以转化为热能和光能
③化学能可以转化为机械能;
④光能或电能可以转化为化学能;
⑤无机物和有机物可以相互转化;
⑥二氧化碳也是一种重要的资源
A.①②③ B.①②③④⑤ C.①④⑤⑥ D.①②③④⑤⑥
19.下图中连线两端的物质在通常情况下可以相互反应。下列四组选项中,符合该图要求的是

①
②
③
④
⑤
⑥
A
CO2
NaOH溶液
稀HC1溶液
Ca(OH)2溶液
CuC12溶液
Fe
B
CaO
稀HCl
溶液
Fe
稀H2SO4溶液
Na2CO3溶液
Ca(OH)2溶液
C
Fe
稀H2SO4溶液
BaC12溶液
Cu(NO3)2溶液
Ca(OH)2溶液
Na2CO3溶液
D
Zn
稀HC1溶液
CaCO3
CuSO4溶液
NaOH溶液
FeC13溶液
20.下图是a、b、c、d四种固体物质的溶解度曲线;下表是这些固体物质在部分温度时的溶解度。根据图表信息判断下列说法正确的是

NaCl
KCl
NH4Cl
KNO3
A.图中a曲线表示KNO3的溶解度曲线
B.b的溶解度小于a的溶解度
C.要从a与d的混合物中得到a,通常采用冷却热饱和溶液的方法使其结晶
D.KC1的不饱和溶液由
第Ⅱ卷(非选择题部分,共70分)
三、填空题(本题包括5个小题,26分)
21.(6分)“从生活走进化学,从化学走向社会”。请你用化学知识解释以下生活中的问题:
(1)大新发现运动后被汗水浸湿的衣服晾干,常出现白斑。其原因是________________。
(2)做馒头发酵面团时,会产生乳酸等有机酸,揉面团时需加入适量的纯碱或小苏打,让它们相互作用产生______________气体,使蒸出的馒头疏松多孔;若加入的纯碱或小苏打过多,可向面团或蒸锅中滴加少许酸性物质,如_______________,否则蒸出的馒头会变涩,颜色发黄。
(3)某企业因经营不善而停工,一年多来,许多机械设备上已锈迹斑斑。小强将设备上一枚生锈的铁螺丝放入足量的稀盐酸中,观察到铁锈逐渐消失,该反应的化学方程式为:__________。一段时间后,又观察到铁钉表面有气泡产生,写出产生气泡的化学方程式: ______。小强结合学过的化学知识,向留守的管理人员提出了一些防止机械设备进一步锈蚀的建议,请写出一条小强的建议:______________________________________________________________。
22.蛋白质是组成细胞的基础物质,没有蛋白质就没有生命。人体内的血红蛋白、各种酶都是蛋白质。一些可溶性的重金属盐(如Cu2+、Ba2+、Ag+等的可溶性盐)与蛋白质作用会使蛋白质凝固变性,从而丧失其生理功能危及生命。因此,可溶性重金属盐为有毒物质,根据上述所给知识,用化学式回答下列问题:
(1)CuSO4、AgNO3,、Ba(NO3)2、AgCl四种物质中,无毒的是_______________;
(2)在医疗上用X射线检查胃肠疾病时,让病人服用硫酸钡的悬浊液(俗称钡餐),而不能服用碳酸钡,其原因是人体胃液中含有一定量的_______________,与碳酸钡反应后,产生了一定量的使人中毒的氯化钡,其反应的化学方程式是______________________________。
(3)若因氯化钡中毒,下列方案中可作为最佳解毒措施的是_______________(填序号)。
A.多饮糖水 B.饮用纯碱溶液
C.饮用食盐水 D.饮用硫酸钠溶液
23.(7分)小明同学学习了“酸的性质”、“金属”等知识后,对“酸与金属反应”的性质从内容、规律及其应用等方面进行了总结,请你协助小明同学完成相关总结材料
(1)酸与金属之间反应规律的文字表达式__________________________________________
(2)金属与酸之间的反应规律是__________________________________________________
请你用元素符号填写金属活动性顺序_______________________________________。
(3)金属与盐之间能否发生置换反应取决于参加反应的____________和____________,其反应规律是______________________________,该性质的实际应用实例是____________________
24.(3分)人的生活、生存与化学物质密切相关,请用化学知识解释。
(1)新鲜的鸡蛋随时都在进行呼吸作用,因其蛋壳(主要成分为CaCO3)表面有许多小孔而与外界进行气体交换,控制鸡蛋的呼吸作用可以延长鸡蛋的保鲜时间。小花发现妈妈买回鸡蛋后,把鸡蛋放在石灰水中蘸一下,妈妈说这样做可延长保鲜时间:这样做的理由有2个:一是______________________________,二是______________________________。
(2)人体内胃酸是由胃腺壁细胞分泌而来的,其生理功能是促进胃蛋白的催化作用,促使蛋白质的水解而被人体吸收、促使糖类物质进一步分解。但胃酸过多会使人体产生疾病、医疗上常用口服胃舒平(内含氢氧化铝)片的方法治疗胃酸过多,请用化学方程式表示其原理____。
25.(6分)某村根据资源特点将石灰石的开采、加工和高炉炼铁建在一起形成联产。
回答:
(1)炼铁的固体原料有铁矿石、焦炭和_______________。请写出炼铁过程中CO和FeO2,反应的化学方程式:____________________________________________________________。
(2)高炉炼铁排放的废气中含有大量的高温一氧化碳,可作为能源用来煅烧石灰石。
请写出煅烧石灰石的化学方程式:_____________________________________________。
(3)此联产方式的主要优点是______________________________(答出一点即可)。
(4)据CCTV报道,某钢铁有限公司即将报废的高炉重力除尘器顶部泄爆板爆破,造成煤气泄漏,导致2名操作工人当场死亡,另有15名事故抢险人员,因缺乏抢险知识而中毒死亡。煤气中毒实质是_______________中毒,你认为15名抢险人员死亡的原因是:______________________。
四、简答题(本题包括2个小题,共14分)
26.(6分)酸雨是天空降水呈酸性(pH小于5.6)的统称,个别地方酸雨的pH竟低于2.1(食醋的pH=3),可见其严重程度,形成酸雨的主要物质是大气中的SO2和氮氧化物。
(1)SO2,主要来源是煤和石油的燃烧,全世界每年有1.5亿吨SO2的排放量。SO2在空气中受阳光及尘埃等催化时可被氧化,生成三氧化硫,三氧化硫最终与雨水形成酸雨。试写出这一过程中所发生的两个化学反应方程式________________; _________________。
(2)酸雨可导致的危害有_______________(填编号)。
A.腐蚀建筑物 B.导致树木枯萎
C.造成洪涝灾害 D.影响农作物生长
(3)为了减少酸雨的形成,必须减少SO2的排放量,熟石灰的悬浊液、澄清石灰水、浓NaOH溶液都能吸收废气中的SO2,从净化效果、净化成本等方面综合考虑,你认为用_________比较合理。请用简要的文字说明理由。(理由2分)
27.(8分)海洋是个巨大的资源宝库,它不仅孕育着无数的生命,还含有大量的化学物质。 Ⅰ.海水制溴。从海水中提取的溴约占世界溴产量的1/3,工业上常用“吹出法”制溴,其工艺流程如下:

试回答:
(1)步骤②中的化学方程式为2NaBr+Cl2=2NaCl+Br2,其反应类型是_________________。
(2)非金属单质也具有类似金属与盐溶液之间的反应规律,如在溶液中可发生下列反应:Cl2+2KBr=2KCl+Br2 Br2+2KI=2KBr+I2,由此可判断C12、I2、Br2活动性由强到弱顺序是_____。
Ⅱ.食盐制碱。我国著名化学家侯德榜发明的联合制碱法的主要过程是:①向浓氨水中通入足量的二氧化碳生成碳酸氢铵溶液;②然后向溶液中加入食盐细粒充分搅拌,控制条件,利用物质的性质不同,两者发生反应生成碳酸氢钠。便有品体析出;③将析出的碳酸氢钠加热制得碳酸钠、二氧化碳和水。
四种盐在不同温度下的溶解度表:
氯化钠
35.8
36.0
36.3
36.6
37.0
碳酸氢铵
15.8
21.0
27.0
碳酸氢钠
8.1
9.6
11.1
12.7
氯化铵
33.3
37.2
41.4
45.8
50.4
请回答:
(3)过程①中发生反应的化学方程式_____________,该反应类型____________。
(4)根据溶解度表分析过程②中能发生反应的原因是______________________________,过程②发生的化学方程式______________________________该反应的类型为_______________。
(5)过程③中反应的化学方程式是_______________________________________________。
五、实验与探究(本题共2个小题,23分)
28.(11分)小明选择“铝丝和盐酸反应的快慢与什么因素有关”的课题开展探究。
下表是他分别用相同质量的铝丝和足量稀盐酸反应的三组实验数据:
实验编号
盐酸的质量分数/%
反应温度/℃
铝丝消失的时间/S
①
3
20
500
②
6
20
300
③
6
30
80
(1)写出铝和盐酸反应的化学方程式:__________________________________________。
(2)实验②和③表明:该反应快慢与______________________________有关。
(3)能表明盐酸浓度对反应快慢有影响的实验编号是:_______________。
(4)如果把实验①中盐酸的质量分数改为4%,请你推测出铝丝消失时间(用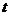 表示)的取值范围:____________________________________________________________
表示)的取值范围:____________________________________________________________
(5)该实验除了用铝丝消失的时间来衡量反应的快慢外,你还能提出新的方法来衡量该反应的快慢吗?方法: _______________________________________。
(6)小明将稀盐酸换成稀硫酸继续实验,发现铝丝和稀硫酸反应现象不明显。
【发现问题】为什么铝丝易与稀盐酸反应而难与稀硫酸反应呢?
【提出假设】C1-的存在使酸和铝的反应容易进行。
【设计实验】请你帮助小明设计一个合理的实验来验证假设
方 案
预期现象
相应结论
29.(12分)甲同学在某食品包装袋内,发现有一个装有白色颗粒状固体A的小纸袋,上面写着“生石灰干燥剂,请勿食用”。甲同学随手将小纸袋拿出来放在空气中,经过一段较长的时间后,发现纸袋内的白色颗粒粘在一起成为块状同体B。请你与甲同学一起对块状固体B进行探究。
(1)猜想一:块状固体B中除氧化钙外还可能有:_______________、______________。
写出白色颗粒状固体A在空气中转化为块状固体B的化学反应方程式:
________________________________________、__________________________________ (2)猜想二:块状固体B溶于水可能有_______________现象(填“放热”或“吸热”)。
(3)取适量块状固体B加人盛有一定量水的试管中,振荡、静置、过滤,得到少量白色固体C。就白色固体C的成分,甲同学与乙同学进行了讨论。
甲同学认为白色固体C可能是:氢氧化钙;
乙同学认为白色固体C可能是:碳酸钙;
你认为白色固体C还可能是:______________________________。
请设计实验证明你的猜想(填写下表):
方 案
预期现象
相应结论
六、计算题(7分)
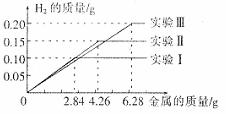
30.某化学调查小组的同学到钢铁厂做社会调查。他们抽取组成完全相同的质量为
试回答(计算结果精确到0.1%):
(1)该钢样含铁的质量分数是______________________________。
(2)稀硫酸完全参加反应的实验中,反应后溶液中溶质的质量分数是多少。