2009-2010学年度临沂市莒南第一学期九年级阶段性质量检测
化学试题
一、选择题(共15小题,每题3分,共45分)
1.下列典故中,从物质变化的角度分析,主要体现化学变化的是
A.司马光砸缸 B.凿壁偷光
C.火烧赤壁 D.铁杵磨成针
B.凿壁偷光
C.火烧赤壁 D.铁杵磨成针
2.中华人民共和国第十一届全运会在我们省胜利闭幕。全运会使用的如意火炬的燃料为丙烷(C3H8)。下列关于丙烷性质的描述,属于化学性质的是
A.无色气体 B.着火点为
C.沸点为一
3.下列实验操作中,正确的是

A B C D
4.下列常见的物质中,属于纯净物的是
A.啤酒 B.食醋 C.加碘食盐 D.蒸馏水
5.下列有关空气各成分的说法正确的是
A.氧气的化学性质比较活泼,属于可燃物
B.氮气的化学性质不活泼,可用于食品防腐
C.空气质量报告中所列的空气质量级别越大,空气质量越好
D.二氧化碳在空气中含量增多会引起温室效应,属于空气污染物
6.在实验室里制取氧气,既可采用分解过氧化氢的方法,也可采用分解氯酸钾的方法。上述两种方法的主要共同点有①采用MnO2均可改变其反应速率②反应都不需加热③都利用含氧化合物分解来达到目的④两种方法所需仪器相同
A.①③ B.③④ C.①② D.②④
7.下列物质中,属于氧化物的是
A.O2 B.H2O C.KCl D.H2SO4
8.榴莲被誉为“果中之王”。切开榴莲时可闻到特殊香味,这说明
A.分子在不断运动 B.分子质量很小
C.分子体积很小 D.分子间有间隔
9.2009年“中国水周”的主题是:落实科学发展观,节约保护水资源。下列认识和做法不符合这一主题的是
A.洗菜、洗衣、淘米的水用来浇花、拖地、冲厕所
B.加强工业废水的排放监控,坚持达标排放
C.合理施用农药、化肥,以减少水体污染
D.淡水资源丰富,所以淡水可以取之不尽,用之不竭
10.著名化学家徐光宪获得了2008年度国家最高科学技术奖,他的研究成果使稀土元素的分离变得更加简单。稀土元素包括镧(La)与钇(Y)等l7种元素,被称作当代的“工业味精”。镧、钇原子的本质区别是
A.电子数不同 B.中子数不同
B.中子数不同
C.质子数不同 D.相对原子质量不同
11.原子序数为94的钚(Pu)是一种核原料,该元素一种原子的质子数的中子数之和为239,下列关于该原子的说法不正确的是
A.中子数为145 B.核外电子数为94
C.质子数为94 D.核电荷数为239
12.化学与人体健康密切相关。市场上有“高钙牛奶”、“加氟牙膏”、“葡萄糖酸锌”等商品,这里的“钙、氟、锌”应理解为
A.原子 B.元素 C.分子 D.单质
13.据报道,用于清洗龙虾的“洗虾粉”中含有柠檬酸钙、亚硫酸钠(Na2SO3)等物质,可能对人体的健康产生危害。Na2SO3中S元素的化合价为
A.+6 B.+4 C.+2 D.一2
14.下列化学用语既能表示一种元素,又能表示一个原子,还能表示一种物质的是
A.O B.Zn C.N2 D.CO
15.甲型H1N1流感在全世界的蔓延,是对人类健康的重大威胁。从中草药“八角”中提取莽草酸是生产抗甲型H1N1流感药物“达菲”的主要原料,其化学式为C7H10O5,下列关于莽草酸的说法中,不正确的是
A.莽草酸是由碳氢、氧三种元素组成的
B.莽草酸的相对分子质量为174
C.莽草酸中含有7个碳原子,10个氢原子和5个氧原子
D.莽草酸是混合物
二、填空题(共6小题,16、17、18每小题1分,19、20每小题2分,共35分)
16.请用化学用语表示:
5个钾原子_________;3个三氧化碳分子_________;4个钠离子_________;
2个氯离子_________;氧化铝中铝的化合价为+3价_________;二氧化硅_________
17.现有①四氧化三铁(Fe3O4)②空气③铁粉(Fe)④氯酸钾(KClO3)、⑤液态氧(O2)⑥水(H2O)⑦氯化钾(KCl) ⑧海水等物质,其中属于单质的是_________,属于化合物的是_________,属于氧化物的是_________,属于混合物的是_________。
18.为了探究“水的净化”过程,某实验小组从护城河中取了水样,观察到:
A.水样呈黄色,有异味
B.水样浑浊,用固体小颗粒
现对水样进行如下处理:
(1)向水样中加入明矾搅拌溶解,静置一段时间后,进行_________(填操作名称),除去固体小颗粒,再向溶液中加入活性炭,利用其_________性除去水样中的颜色和异味,该过程属于_________变化(填“物理”或“化学”)。
(2)通入氯气杀菌消毒,得到自来水,发生的反应如下:Cl2+H2O==HCl+HClO(次氯酸)。
请判断,次氯酸中氯元素的化合价为_________。
(3)为了判断得到的自来水是硬水还是软水,可加入_________进行检验。
19.用分子的相关知识解释下列生活中的现象。
(1)湿衣服在充足的阳光下容易晾干_________。
(2)热胀冷缩_________。
20.下图是同学们在探究氧气性质实验中改进的实验装置图,写出甲中反应的文字表达式:___________________________反应类型_________ 。
简要回答甲、乙两个集气瓶中液体的作用:
甲:____________________________________
乙:____________________________________

21.元素周期律是学习和研究化学的重要工具,下表是元素周期表的部分信息:
1 H
氢
2He
氦
3Li
锂
4Be
铍
5B
硼
碳
7N
氮
8O
氧
氟
10Ne
氖
11Na
钠
12Mg
镁
13Al
铝
14Si
硅
15P
磷
16S
硫
17CI
氯
18Ar
氩
19K
钾
20Ca
钙
认真分析信息,回答:
(1)地壳中含量最多的金属元素的符号是_________。
(2)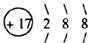 表示的是(填名称)_________。
表示的是(填名称)_________。
(3)由8、l2号元素组成化合物的化学式是_________。
(4)元素周期表同一横行元素的排列规律是:从左到右_________。
三、实验题;(共1小题,共8分。(1)小题每空1分,(2)(3)每空2分)
22.现有下图所示的实验装置,请回答问题:
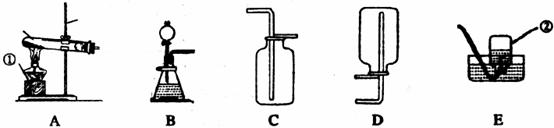
(1)标有序号的仪器名称①_________②_________
(2)在加入药品之前应对实验装置进行__________________。
(3)可用于实验室制备和收集O2的一套装置是(填字母代号)_________。写出用此装置制备O2的文字表达式:___________________________。
四、计算题:(共1小题,总分7分)
23.科学家经过多年研究证明,有一些同学爱吃的小包装零食中,含一定量的有毒、有害、致病的化学物质,如某些油炸食品中含有致癌物质两烯酰胺(C3H5ON)。请你根据丙烯酰胺(C3H5ON)的化学式计算并填写:
(1)丙烯酰胺(C3H5ON)的相对分子质量为__________________。
(2)碳元素和氧元素的质量比是__________________。
(3)氢元素的质量分数为__________________。