2009-2010学年度辽宁省大石桥市第一学期九年级期中考试
化学试卷
时间:80分钟 满分:100分
可能用到的相对原子质量:H―1,C―12,O―16,S―32,Cl―35.5,Ca―40
一、我会选(每小题均只有一个正确选项,每小题2分。共40分)
1.下列括号中对日常生活的变化判断正确的是
A.嘴嚼米饭时有甜味(化学变化)
B.玻璃窗破裂(化学变化)
C.用醋酸清洗热水瓶的水垢(物理变化)
D.纯净物加热后变成混合物(物理变化)
2.下图中各微粒的示意图中,表示阳离子的是
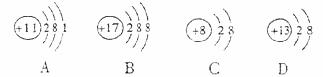
3.下列说法正确的是
A.按质量计算:空气中含有氮气78%、氧气21%、其他气体和杂质1%
B.鱼类能在水中生活,证明氧气易溶于水
C.洁净的空气是纯净物,被污染的空气是混合物
D.实验室常用向上排空气法收集二氧化碳
4.做化学实验必须注意安全:下列属于安全操作的是
A.用嘴吹灭燃着的酒精灯
B.为了节约火柴,可用燃着的酒精灯点燃另一盏酒精灯
C.点燃氢气前,检验氢气的纯度
D.加热试管中的液体时,不用考虑试管口是否对着其他人
5.下列各组物质,按混合物、化合物、单质顺序排列的是
A.冰水共存物、干冰、氢气
B.水、碳、氧化铁
C.洁净的空气、氯化氢、液态氧
D.纯碱、酒精、水银
6.实验证明M气体在空气中燃烧有水生成。仅依据此结果,对M的成分推测正确的是
A.M是氢气 B.M是甲烷
C.M含有氢元素 D.M含有氢、氧两种元素
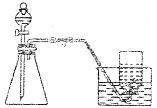
7.下列制取气体的方案,可以直接采用如图所示装置进行的是
①用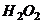 和
和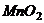 制取
制取 ②用
②用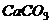 和稀盐酸制取
和稀盐酸制取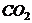
③用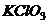 和
和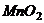 制取
制取 ④用
④用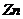 和
和 制取
制取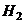
⑤用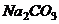 和
和 制取
制取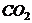
A.①④ B. ①②④ C.①②⑤ D.①②④⑤
8.以下现象,能说明分子间空隙变小的是
A.海绵能吸水 B.打气筒将气体压缩
C.炒菜时闻到香味 D.干冰升华
9.两同学围绕蜂窝煤燃烧进行了如下研究,其中依据质量守恒定律解释的是
A.当煤燃烧正旺时将炉门关上,煤层上方出现蓝色火焰。解释:此时氧气不足而产生的CO在燃烧。
B.煤燃烧完后煤灰质量比煤的质量轻。解释:煤燃烧后产生的二氧化碳等气体逸出。
C.在煤炉上方放一壶水不能防止CO中毒。解释:CO难溶于水
D.将煤做成蜂窝状就更易燃烧。解释:蜂窝状的煤与空气接触面积增大
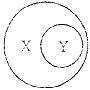
10.学习化学时可用下图表示某些从属关系,下列选项正确的是
A
B
C
D
X
纯净物
单质
单质
分解反应
Y
单质
氧化物
化合物
化合反应
11.某化学活动,小组做了如下四条设想,你认为具有可行性的是
①用“蒸馏法”淡化海水来解决淡水危机
②为了减少水体的污鞋,农业上禁止使用农药和化肥
③洗菜、洗衣、淘米的水用来浇花、拖地,冲厕所
④加高燃煤锅炉的烟囱,减少二氧化硫的排放
A.①② B.①③ C.③④ D.②④
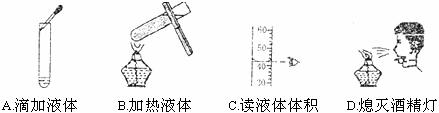
12.下列实验操作正确的是
13.减少污染,净化空气,“还我一片蓝天”,已成为世界各国人民的共同心声,下列气体会造成空气污染的是
A.一氧化碳 B.二氧化碳 C.氧气 D.氮气
14.北京是极度缺水的城市。作为北京市民,下列生活习惯应该摒弃的是
A.用盆接水洗菜 B.用养鱼水浇花草
C.使用节水龙头 D.丢弃未喝完的矿泉水瓶
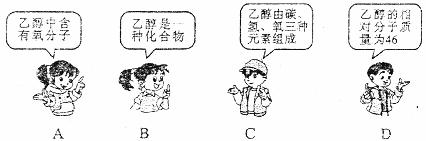
15.国家推广乙醇汽油的应用,可改善机动车燃油问题:所谓乙醇汽油是在汽油中加适量乙醇混合而成,可以减少汽油燃烧后列空气的污染。已知乙醇的化学式为C2H5OH。下面四位同学能说法是,错误的是
16.下列物质在氧气中燃烧,能产生大量白烟的是
A.木炭 B.铁丝 C.一氧化碳 D.红磷
17.下列关于水的说法正确的是
A.水的污染会引起土壤的污染 B.地球上淡水资源非常丰富
C.过滤能够除去水中所有杂质 D.水由氢气和氧气组成
18.很多物质能在氧气中燃烧。下列有关叙述正确的是
A.铁在氧气中燃烧生成黑色的FeO
B.硫在氧气中燃烧生成的SO2中,硫元素的化合价为+2
C.铁丝在氧气中燃烧集气瓶内要预先装少量水或铺一层细沙
D.某物质在氧气中完全燃烧,只生成CO2和H2O,则该物质中一定含有C、H、O三种元素
19.下列化学用语与含义相符的是
A.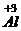 ――1个铝离子带3个单位正电荷
――1个铝离子带3个单位正电荷
B.2H2O――2个水分子
C.2H――1个氢分子由2个氢原子组成
D.Na+――钠元素的化合价为+1价
20.在一密闭容器中有SO2、SO3混合气体,若SO2中氧元素与SO3中氧元素的质量之比为5:6,则容器中SO2与SO3的质量比为
A.2:1 B.1:
二、我会填。(化学方程式每处2分,其余每空1分,共33分)
21.稀有气体元素的原子最外层电子数是_________个(氦原子是________个);金属元素的原子最外层电子数一般少于________个,在化学变化中易________(填“得”或“失”)电子;形成________(填“阴”或“阳”)离子;非金属元素的原子最外层电子数一般多于或等于_______个,在化学变化中易__________(填“得”或“失”)电子,形成__________(填“阴”或“阳”)离子。
22.用正确的化学符号填空:
(1)五氧化二氮________;(2)3个硫酸分子________;
(3)碳酸根离子________;(4)能保持氮气化学性质的最小粒子________
23.通过化学学习,我们认识了很多物质。请从①石墨②二氧化锰③活性炭④肥皂水中选择适当的物质填空(填序号)。
(1)可用于制铅笔芯的是________。
(2)用氯酸钾制氧气时作催化剂的是________。
(3)可用来检验硬水和软水的是________。
(4)可用作除去冰箱中异味的是________。
24.日常生活和生产过程与化学有着密切的联系。请你运用所学的化学知识填空:
(1)体温计中填充的金属是________,它是由________(填“分子”、“原子”或“离子”)构成的。
(2)今年4月份,我区全面推行使用乙醇汽油代替普通汽油作为汽车的燃料,使用乙醇汽油可以减少SO2气体的排放,是因为乙醇中不含________元素。
(3)某气体常在大棚蔬菜的种植中用作气体肥料,其作用是促进植物光合作用,使蔬菜长势良好,该气体是________,它的固体还可用于________。(填一种用途)。
25.下图中①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
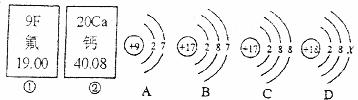
请你回答:
(1)氟元素的相对原子质量为________,钙元素的原子序数为________。
(2)X=________。
(3)A、B、C、D中属于同种元素的粒子是________(选填序号)。
(4)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似________(选填序号)。
26.1909年化学家哈伯在实验至首次合成了氨。2007年化学家格哈德?埃特尔在哈伯研究所证实了氧气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖。
(1)将氢气和氯气在高温、高压和催化剂的条件下合成氢(NH3)。反应的化学方程式为__________________________________。
(2)用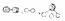 ,分别表示N2、H2、NH3。观察下图,写出符合在催化剂表面合成氨反应过程的顺序_________________(将下面五张图按反应过程顺序用序号排列)
,分别表示N2、H2、NH3。观察下图,写出符合在催化剂表面合成氨反应过程的顺序_________________(将下面五张图按反应过程顺序用序号排列)
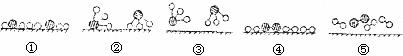
(3)表面化学对于化学工业重要。它可以帮助我们了解不同的过程。在潮湿的空气里,铁表面吸附了一层薄薄的水膜,同时由于空气中O2的溶解,水膜呈中性。若空气中CO2溶解,水膜呈酸性,写出该反应的化学方程式_____________________。
在汽车排气管上安装尾气净化装置,可使尾气中的CO和NO在催化剂表面发生反应。产生两种空气组成成分的气体,写出该反应的化学方程式_____________________。
三、我会答。(3分+4分=7分)
27.用分子原子的观点解释下列事实:
(1)在花园中可以闻到花的芳香:_____________________;
(2)用打气筒可将空气压入足球内:_____________________;
(3)水在通电条件下分解为氢气和氧气,说明_____________________。
28.化学知识中有很多的“相等”例如:化合物中元素化合价的正价总数与负价总数的数值相等,请再举两例:
①_______________________________________________________________;
②_______________________________________________________________。
三、我会探究。(7分+6分=13分)
29.根据下图所示水、二氧化碳和氧气的性质实验;请回答以下问题。
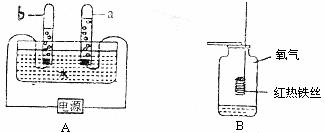
(1)A装置中发生反应的化学方程式为________________________________。用带火星的木条检验a中的气体,观察到木条复燃,该气体是__________。
(2)通电后,b试管中电极连接的是电源__________极。
(3)集气瓶B中的现象:铁丝在氧气中剧烈燃烧,__________,放出大量的热、有黑色固体生成。该反应的化学方程式为________________________________________。
30.化学是一门以实验为基础的科学。
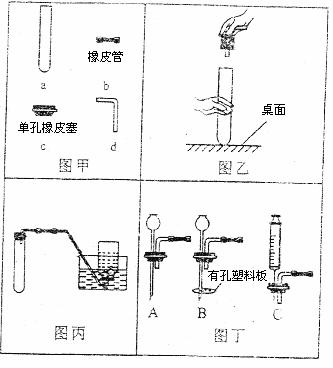
(1)根据图甲回答:
①写出a的名称___________;
②在连接c和d时,使d较易插入c中的措施是___________。
(2)采用图乙所示操作可能造成的后果之一是______________________。
(3)利用图丙装置(夹持装置未画出)能进行的实验是___________,
A.用高锰酸钾制氧气 B.用石灰石与稀盐酸制二氧化碳
C.用锌与稀硫酸制氢气 D.用双氧水与二氧化锰制氧气
(4)图丙中的气体发生装置虽然简单,操作方便,但无法控制反应速率。请从图丁中选取_________(选填序号)与图甲中a组装或新的气体发生装置,以达到控制反应速率的目的:
五、我会算。(7分)
31.石灰石是我市的主要矿产之一,我校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,采集了一些矿石样品,并取稀盐酸
实验序号
1
2
3
4
加入样品质量(g)
3
10
15
20
生成CO2的质量(g)
1.76
3.52
4.4
m
(1)反应中矿石有剩余的是_______________(填序号)。
(2)上表中m的数值是_______________。
(3)试计算这种石灰石矿石中碳酸钙的质量分数。