2009-2010学年度内蒙古包头五中第一学期九年级期中考试
化学试卷
可能用到的相对原子质量:
H―1, O―16, Mg―24, Fe―56,Cu―64, Zn―65,Al―27 Ag-108
一、选择题(1―8每小题只有1个选项符合题意,9―12每小题有1~2个选项是正确的,请将正确答案填入括号内。共28分)
1.生活中常见的下列物质,属于溶液的是( )
A.牛奶 B.泥水 C.蔗糖水 D.花生油
2.人类的生产和生活中离不开金属材料。通常所说的“金属材料”,既包括纯金属,也包括各种合金。下列金属材料不属于合金的是( )
A.青铜 B.黄铜 C.铁锈 D.焊锡
3.金属、金属材料的性质在很大程度上决定了它们的用途。下列说法中不正确的是 ( )
A.不锈钢抗腐蚀性好,常用于制造医疗器械
B.铁具有良好的导热性,可以用于制造炊具
C.铝合金轻而坚韧,可作汽车、飞机和火箭的材料
D.铅锑合金的熔点较低、电阻率较大,常用于制成发热体
4.下列有关对自行车的做法不合理的是( )
A.车架表面喷涂油漆 B.钢圈表面镀防护金属
C.车把手上涂一层油 D.链条表面涂机油
5.铜粉中含有少量的铁粉,最佳的除铁办法是( )
A.加入足量硫酸锌,过滤 B.在空气中灼烧
C.高温下加热并通入氢气 D.加入足量硫酸铜溶液,过滤
6.下列关于海水晒盐原理的分析,正确的是( )
A.利用阳光照射使海水升温得到食盐
B.利用机械动力搅拌得到食盐
C.利用阳光和风力将水分蒸发得到食盐
D.利用海水在阳光下发生分解反应制得食盐
7.下列反应中,不属于置换反应的是( )
A.H2+CuO Cu+H2O B.C+2CuO
Cu+H2O B.C+2CuO 2Cu+CO2↑
2Cu+CO2↑
C.CO+CuO Cu+CO2 D.2Al+3CuO
Cu+CO2 D.2Al+3CuO 3Cu+Al2O3
3Cu+Al2O3
8.某样品6.
A.Fe B.Mg C.Al D.Cu
9.把铁片分别放入下列物质的溶液中,过一段时间取出,溶液质量减少的是( )
A.Al2(SO4) B.CuSO
10.某学生为了验证铁、锌、铜三种金属的活动性顺序,设计了四种方案:其中可行的是( )
A.将Zn、Cu分别加入到FeSO4溶液中;
B.将Zn、Cu分别加入到ZnSO4溶液中;
C.将Zn分别加入到FeSO4、CuSO4溶液中;
D.将Fe 分别加入到ZnSO4、CuSO4溶液中。
11.某单质X能从某溶液中置换出单质Y,由此推断下列说法中正确的是( )
A.X一定是排在金属活动顺序表中氢以前的金属
B.X是金属时,Y可能是金属,也可能是非金属
C.X是金属时,Y一定比X活泼
D.X、Y都是金属时,X一定比Y活泼
12.向含AgNO3、Cu(NO3)2 、Mg(NO3)2混合溶液中,加入一定量的锌粒,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气体生成,则滤出的固体中一定有( )
A.Ag、Cu、Mg B.Cu、Mg、Zn
C.Ag、Cu、Zn D.Ag、Mg、Zn
二、填空题(共22分)
13.烧菜用的铁锅,主要是利用铁的________性质;铁锅长期在_____________中易生锈,铁锈的主要成分中铁呈 价。
14.生铁和钢都是铁的合金,它们的区别主要是 。
15.颗粒大小达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”。在高温条件下,用H2与FeCl2反应,可生成“纳米铁”和一种溶于水显强酸性的气体,写出该反应的化学方程式 。
16.构建知识网络是一种重要的学习方法。下图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为红色固体单质。请回答下列问题:
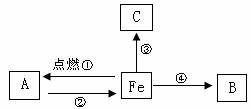
(1)A物质的化学式为 。
(2)B物质的一种用途是 。
(3)反应②还需要的一种反应物是 (填化学式)。
(4)写出反应③的方程式,并注明基本反应类型: ( )。
17.下列有三种制取硝酸铜的方案:
方案一:Cu + 4HNO3(浓) = Cu(NO3) + 2NO2↑+ 2H2O
方案二:3Cu + 8HNO3(稀) = 3Cu(NO3) + 2NO↑+ 4H2O
方案三:2Cu + O2 + 4HNO3(稀) = 2Cu(NO3)2 + 2H2O
请你从经济、环保的角度分析考虑选择一种最适宜的方案 ,你选择方案而不选其它方案的理由是(写两点): 。
18.为了探究影响金属与酸反应程度的因素,进行了以下实验:
实验序号
实验过程
实验现象
1
镁粉和铁粉分别与5%盐酸反应
镁粉产生气体快
2
铁粉和铁片分别与10%盐酸反应
铁粉产生气体快
3
铁片分别与5%盐酸和10%盐酸反应
10%盐酸产生气体快
由此得出影响金属与酸反应剧烈程度的因素有:
因素一:____________________________________________________;
因素二:_____________________________________________;
因素三:___________________________________________。
19.在Cu(NO3)2、AgNO3的混合溶液中,加入一定量的锌粉,充分反应后,可能有下列情况:
(1)若反应后锌有剩余,则此时反应后的混合物过滤,滤纸上留有的残留物是 ;滤液中存在 。
(2)若将反应后的混合物过滤,向所得的固体物质中滴加稀盐酸,没有气泡产生,则固体物质中一定有 ,可能有 。
三、实验与探究(共14分)
20.有位同学设计了下列实验(装置及所用药品如图所示),仔细观察后回答下列问题。

(1)写出图中标有序号的仪器名称①_______②_________
(2)在给氧化铁加热时,要先通入一氧化碳气体后加热,其目的是 。
(3)在C处看到的现象是 ,反应的化学方程式________________。
(4)本实验设计中,在B处所采取措施的目的是 ,其优点是
21.同学们一起探究铝、铁、铜三种金属的活动性,小刚同学设计了用铜丝、铁丝、铝丝和稀盐酸,只用一只试管,取一次盐酸的探究方案。请你和他们一起完善下表的探究方案并回答有关问题。
(1)填表
实验步骤
观察到的现象
①在试管中取少量盐酸,插入铁丝,充分作用。
②在①所得的溶液中,插入 ,充分作用。
无明显现象
③在②所得的溶液中插入 ,充分作用。
结论:金属活动性Al > Fe > Cu
(2)小华同学认为在小刚设计的方案中,只要补充一个实验,就可得出Al > Fe > H >Cu的结论。小华要补充的实验是 ;
(3)小强同学认为要得到Al > Fe > H >Cu的结论,不必做补充实验,中需将小明同学方案中插入金属的顺序调整即可,你认为调整后插入金属的顺序是 。
四、计算题(6分)
22.100 t含80%的赤铁矿石能冶炼出含杂质3%的生铁多少吨?