2008-2009学年度曲阜市第二学期九年级中考考前检测
化学试卷
温馨提示:
本试题分第Ⅰ卷和第Ⅱ卷两部分,共6页。第Ⅰ卷为选择题,共2页,16分;第Ⅱ卷为非选择题,共4页,34分;第Ⅰ卷和第Ⅱ卷共50分;考试时间为50分钟。
可能用到的相对原于质量:H―
第Ⅰ卷(选择题共16分)
一、选择题(下列各题只有一个正确选项。其中,1-4小题各1分,5―10小题各2分,本大题共16分)
1.下列日常生活中的变化属于物理变化的是( )
A.咀嚼米饭时有甜味. B.玻璃窗破裂
C.用醋酸清洗热水瓶的水垢. D.纯净物加热后变为混合物
2.下列说法正确的是( )
A.河水、井水、海水是混合物,自来水是纯净物
B.液态的水分子不断运动,固态的水分子不运动
C.水由气态变成液态放出热量,该变化是放热反应
D.水通过天然循环,实现了水的自身净化,补充了淡水资源
3.下列图示实验操作中,正确的是( )
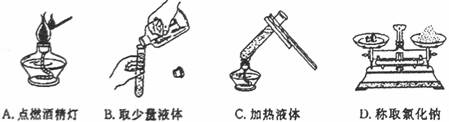
4.
A.洗菜、洗衣、淘米的水用来浇花、拖地、冲厕所
B.用罐纸过滤,除去海水中盐分
C.合理施用农药、化肥,以减少水体污染
D.加强工业废水的排放监控,坚持达标排放
5.根据下列微粒的结构示意图,其中属于阳离子的是( )
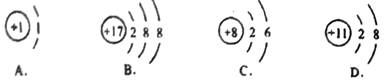
6.“绿色化学”是21世纪化学发展的主导方向,要求从根本上杜绝污染。它包括“原料绿色化”、“化学反应绿色化”、“产品绿色化”等内容。其中“化学反应绿色化”要求原料物质中的所有原子全部转入期望的产物中,下列符合“化学反应绿色化”要求的是( )
A.制取氢气:Zn十H2SO4=ZnSO4+H2↑
B.制取氧气:2KMnO4 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
C.制取碳酸氢铵:CO2+H2O+NH3=NH4HCO3
D.制取氨气:(NH4)2SO4+Ca(OH)2=CaSO4+2NH3↑+2H2O
7.物质的用途与性质密切相关,下列说法不正确的是( )
A.氮气常用作保护气,是由于氮气的化学性质不活泼
B.钨常用来制造灯泡中的灯丝,是因为钨的熔点高
C.铁制栏杆表面常涂“银粉漆”(铝粉)防生锈,是由于铝的化学性质比铁稳定
D.CO常用来冶炼金属,是因为它是还原剂,具有还原性
8.关于下图两种物质的溶解度曲线说法正确的是( )
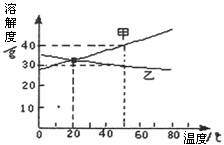
A.升高温度,可使甲的不饱和溶液变为饱和溶液
B.
C.要使乙从其浓溶液中析出,可冷却乙的热浓溶液
D.
9.下列归纳中有错误的是( )
A.灭火方法
B.食品安全
森林着火时,向火源喷水;实验桌上少量酒
精着火,用湿抹布盖灭
霉变食品、甲醛水溶液浸泡过的海鲜,食用
后危害人体健康,不能食用
C.能源与环境
D.实验安全
太阳能、水能、风能是人类正在利用的主要
能源;煤、石油、天然气燃烧后的产物对环境无影响
不能用嘴吹灭燃着的酒精灯;用试管加热少
量液体试剂时,试管口不能对着人
10.下列图象正确反映对应的变化关系的是( )
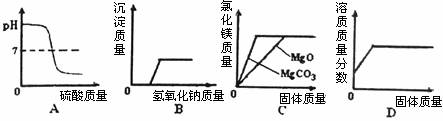
A.向一定量的氢氧化钠溶液中滴加稀硫酸至过量
B.向一定量的硫酸和硫酸镁混合溶液中滴加氢氧化钡溶液
C.将足量碳酸镁和氧化镁固体分别加入相同质量、相同质量分数的稀盐酸中
D.在一定温度下,向饱和的硝酸钠溶液中不断加入硝酸钠固体,充分搅拌
第Ⅱ卷(非选择题 共34分)
二、填空与简答(共17分)
11.(2分)用适当的数字和符号填空:
(1)4个五氧化二磷分子_________________
(2)2个氢氧根离子_________________
(3)n个亚铁离子_________________
(4)海水“制碱”得到的“碱”_________________
12.(3分)化学是造福人类的科学,在日常生活、人体保健、医疗卫生等方面作出了重大贡献。请你用所学的化学知识解答有关问题。
(1)在新农村建设中,许多家庭兴建沼气池。沼气的主要成分是_____________
(2)大米的主要成分是淀粉。淀粉属于六大营养素中的_____________
(3)餐具上的油污用加入洗洁精的水更易洗掉,原因是_____________
(4)市场上食盐的品种丰富,有碘盐、锌盐、钙盐、硒盐等。这些食盐中含的碘,、锌、钙、硒等是指_____________(选填“原子”、“离子”、“元素”或“单质”)。
(5)油炸食物不宜多吃,因长时间煎炸会产生有毒物质丙烯醛(C3H4O),丙烯醛在空气中完全燃烧时,生成二氧化碳和水。
请写出丙烯醛完全燃烧的化学方程式__________________________________________
(6)食盐是人维持正常生理活动的重要物质。人体细胞中约含NaCl 0.9%,一般成年人每日需NaCl的量为
13.(2分)请回答下列与物质提纯有关的问题:
(1)下列两个方案都可以除去铜粉中的少量氧化铜
①用稀盐酸除去氧化铜; ②用CO还原氧化铜。
从环境保护和操作简便等方面考虑,较好的方案是_______(选填“①”或“②”);
(2)要除去K2SO4溶液中的少量KOH,不能选用稀盐酸,原因是会生成______________(填写具体物质的名称或化学式),而引入新的杂质。
(3)要使NaCl溶液中的少量Na2SO4转化为沉淀而除去,可选用适量的___________。
(4)要除去氢气中的少量水蒸气和氯化氢气体,将混合气体先通过足量的浓硫酸再通过足量的氢氧化钠溶液后,氢气中仍含有的杂质是____________________。
14.(6分)金属材料在生产、生活中有着广泛的应用。
(1)人类每年从自然界提取大量的金属,其中提取量最大的是铁。用赤铁矿和一氧化碳炼铁的化学方程式为_______________________
(2)为探究锰与铁的金属活动性,在相同温度下,取大小相同、表面光亮的两种金属薄片,分别投入等体积、等榕质质量分数的足量稀盐酸中(反应中Mn显+2价),请回答:
金属
铁
锰
与盐酸反应现象
放出气泡速率缓慢
放出气泡速率较快
结论
活动性铁______(填“>”“<”)锰
除了比较与酸反应产生气体速率的快慢,请你再举出一种可比较这二种金属活动性强弱的方法(写出所需药品即可):___________和_________________。
(3)金属矿物的储量有限,而且不能再生,所以保护金属资源尤为重要。保护金属资源的有效途径是_________________________________________________(答出两条即可)。
15.(4分)在下面关系图中,A、B、C、D是初中化学中常见的单质,甲、乙分别是乙炔燃烧时一定会产生的两种物质,丁是常用建筑材料的主要成分,C为无色有刺激性气味的气体,能使紫色石蕊试液变蓝,J是赤铁矿的主要成分。
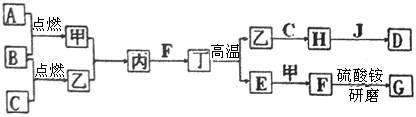
(1)写出化学式:甲是__________,G是__________;
(2)物质丙与F反应生成物质丁的反应类型:______________________________;
(3)J溶解于稀盐酸中,溶液呈黄色,写出变化的化学方程式:____________________
______________________________。
三、实验与探究(共11分)
16.(1)(6分)实验室常用下列装置来制取氧气:

①写出图中其中一种有标号仪器的名称:b__________;
②用双氧水和二氧化锰来制取氧气时,可选用的发生装置是__________ (填序号),其中二氧化锰起__________作用。
③检验氧气是否集满的方法是________________________________________。
④实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小。NH3极易溶于水,其水溶液呈碱性。制取并收集NH3,应该从上图中选择的发生装置是__________,收集装置是____________________。
(2)(本题共5分)小丽同学发现很多物质都能溶解在水中,但它们溶解有快有慢,那么影响同种物质溶解快慢的因素有哪些呢?请你根据生活经验以冰糖为例提出你的猜想,并选择其中一种影响因素设计实验方案。
①(1分)你认为影响冰糖溶解快慢的因素有_________________________________;
②(1分)你选择的因素是_________________________________________________;
③(1分)你设计的实验方案:
实验步骤:________________________________________________________________
___________________________________________________________________________
④(2分)在你所设计的方案中,需要改变的量是________________________________,需要控制的量是________________________________________________________。
四、计算与应用(共6分)
17.(2分)张坤同学帮家里去一家生资公司购买了氮肥NH4NO3,NH4NO3含有几种元素_____________氮元素的质量分数__________
18.(4分)在一次课外活动中,先后有三组同学用含有碳酸钠的氯化钠固体进行了如下实验。实验老师提供的试剂有:①盐酸②氯化钙溶液③氢氧化钡溶液。
(1)为了得到纯净的氯化钠溶液,第一组同学取一定量的上述固体混合物,全都溶解于水,然后加入所选试剂,生成沉淀,恰好完全反应后过滤,所得滤液为氯化钠溶液。则该组同学选择的试剂是_______(填写所选试剂编号)。
(2)为测定该固体混合物中氯化钠的质量分数,第二组同学取该固体混合物