2009年莱芜市中等学校招生考试
化学试题
注意事项:
1.答题前考生务必在规定的位置将姓名、准考证号等内容填写准确。
2.本试题分第Ⅰ卷和第Ⅱ卷两部分。第Ⅰ卷为选择题,20分;第Ⅱ卷为非选择题,30分;共50分。与物理同场考试,两科考试时间共120分钟。
3.请将第Ⅰ卷选择题答案填写在第Ⅱ卷卷首答案栏内,填在其它位置不得分。
4.考试结束后,由监考教师把第Ⅰ卷和第Ⅱ卷一并收回。
可能用到的相对原子质量:
H:
第Ⅱ卷(选择题共20分)
一、选择题(本题包括l0小题,每小题2分,共20分。每小题只有一个正确答案)
1.合理利用资源是当今世界所关注的话题。下列做法与之不相符的是
A.设计雨水回收系统 B.建设风力发电站
C.使用太阳能路灯 D.深埋废弃金属
2.“关爱生命,拥抱健康”是永恒的主题。下列做法有利于身体健康的是
A.为避免受到黄曲霉毒素的伤害,霉变的花生米可以油炸后食用
B.常食新鲜水果和蔬菜,保证人体有充足的维生素
C.食品厂用CuS04溶液浸泡粽叶,使粽叶变得鲜绿
D.使用聚氯乙烯薄膜包装食品
3.日常生活中常见的下列物质,属于化合物的是
A.医用酒精 B.矿泉水 C.体温计中的水银 D.冰水混合物
4.用分子的知识解释下列现象,正确的是
A.缉毒犬能根据气味发现毒品,是由于分子不断运动
B.石灰石能被研磨成粉末,说明分子很小
C.变瘪的乒乓球放入热水中能鼓起来,是由于分子受热体积变大
D.降温能使水结成冰,是因为在低温下水分子静止不动
5.下列观点错误的是
A.化学反应进行得越快、越彻底就一定越好
B.化学变化中分子的种类会发生变化,但构成分子的原子种类不会发生变化
C.绿色化学有助于人类解决环境问题,实现人与自然和谐共处
D.宏观物质是由微观粒子构成的,微观粒子的种类和数量不同、彼此的结合方式多样,决定了物质的多样性
6.达菲是抗击甲型HlNl流感的有效药物,合成达菲的重要中间体为莽草酸(化学式C7H10O5)。 下列有关莽草酸的说法不正确的是
A.莽草酸是一种有机化合物
B.莽草酸中氧元素的质量分数为52%
C.莽草酸由三种元素组成
D.莽草酸分子中C、H、O的原子个数比为7:l0:5
7.向含硝酸银和硝酸锌的工业废液中,加入过量的铁粉回收金属,过滤。滤纸上固体成分为
A.Fe、Zn、Ag B.Fe、Ag C.Fe、Zn D.Ag
8.下面是李明同学对所学知识进行归纳的情况,其中有错误的一组是
A.性质与用途
B.元素与人体健康
氢气能燃烧―作燃料
铜具有导电性―作导线
人体缺铁―易患贫血症
人体缺碘―易患甲状腺肿大
C.生活常识
D.环保与物质的利用
通电的线路着火时―立即用水浇灭
饮水解渴―水越纯越好
减少水污染―合理使用农药、化肥
减少“白色污染”―使用可降解的塑料
9.推理是化学学习中常用的思维方法。下列推理正确的是
A.酸能使石蕊试液变红,CO2也能使紫色的石蕊试液变红,所以CO2是酸
B.锌和铜均是金属,锌与稀硫酸反应生成氢气,则铜也能与稀硫酸反应生成氢气
C.碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性
D.溶液中有晶体析出,其溶质质量减小,所以溶质的质量分数一定减小
10.下表是某实验报告中的一组数据:
实验序号
试剂l
试剂2
混合前温度/℃
混合后温度/℃
①
35mL水
3.2gNa2CO3固体
20
24.3
②
35mL稀盐酸
20
25.1
根据表中提供的信息,下列有关说法中正确的是:
①Na2CO3溶于水放出热量;②Na2CO3溶于水吸收热量;
③Na2CO3与稀盐酸反应放出热量;④Na2CO3与稀盐酸反应吸收热量
A.①④ B.①③ C.②③ D.②④
第Ⅱ卷(非选择题 共30分)
二、理解与应用(本题包括4小题,共l5分)
11.(3分)溶解度曲线为我们定量描述物质的溶解性强弱提供了便利。请你根据图A、B、C物质的溶解度曲线回答下列问题:
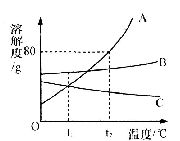
(1)在tl℃时,溶解度最大的物质是_____________
(2)现有接近饱和的C物质溶液,要使其变为饱和溶液,可采用的方法有_________,_________;(写出两种方法)
(3)t
12.(3分)A、B、C、D是初中化学常见的四种物质,它们分别是铁、稀盐酸、氢氧化钠溶液、硫酸铜溶液中的一种。请回答下列问题:
(1)某同学想写出这四种物质两两间发生反应的化学方程式,你认为他最多能写出___________个。
(2)如果A和B能反应生成蓝色沉淀,则该反应的化学方程式是________,C和D反应的基本反应类型为__________反应。
13.(4分)下表是几种家用清洁剂的功能、有效成分。
清洁剂名称
洁厕灵
活性彩漂
漂白精
功 能
清除马桶内的污垢
漂洗衣物,使色彩更亮丽
快速漂除衣物污渍
有效成分
HCl
H2O2
NaClO(次氯酸钠)
据表回答下列问题:
(1)纯碱也是家庭中常用的去污清洁剂,“洁厕灵”能否与纯碱混用?____________
(2)在盛有少量“活性彩漂”液体的试管中,加入少量二氧化锰,观察到的现象是__________,其反应的化学方程式为___________
(3)“洁厕灵”与‘‘漂白精”不能混用。二者若混合易产生一种有毒气体,反应的化学方程式为:NaClO+2HCl=NaCl+X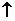 +H2O,则X的化学式是___________
+H2O,则X的化学式是___________
14.(5分)某学习小组将"从空气中制取氮气”作为研究课题,以下是他们的实验方案:

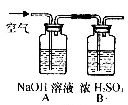
(1)除去二氧化碳和水蒸气:写出图装置A中发生反应的化学方程式________;
(2)除去氧气:他们分别收集一瓶(1)中得到的气体,用图装置进行实验,其中甲同学选用红磷,乙同学选用木炭。你认为选用“红磷”或“木炭”)的方法不科学,原因是________
(3)分析误差:此法得到的氮气密度与氮气的实际密度有误差,请你分析产生误差的可能原因________________
(4)利用物质间某些性质的差异选用不同的方法将它们分离,是分离物质的基本思路。例如:在工业上,分离空气中的氮气和氧气是利用它们沸点的不同。请列举一种你所知道的利用物质性质差异分离物质的方法______________________
三、实验与探究(本题包括2小题,共10分)
15.(4分)化学是一门以实验为基础的科学,具备基本的化学实验技能是学习化学和进行化学探究活动的基础和保证。
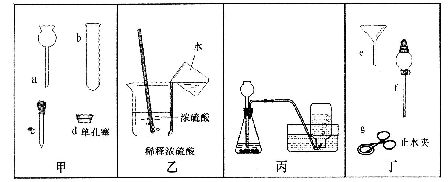
根据上图回答以下问题:
(1)将仪器a与d连接,一般采取的措施是_____________;
(2)图乙所示的操作可能造成的后果是_____________________________;
(3)利用装置丙能进行的实验是_________________(填写序号);
A.用双氧水和二氧化锰制取氧气
B.用锌和稀硫酸制取氢气
C.用氯酸钾制取氧气
(4)图丙的气体发生装置还存在一定的不足,要使装置更加完善,可选用图丁中的________(填写仪器序号)与之重新组合。
16.(6分)通过学习氧气的性质,知道镁在氧气中燃烧会生成白色固体物质。但某学习小组的同学发现在空气中点燃镁条时,生成的白色固体物质中夹杂着少量的淡黄色固体。为了探究其原因,他们做了以下工作:
[提出问题]淡黄色固体物质的成分是什么?
[查阅资料]通过查阅资料,记录了下列几种物质的颜色:
物质
MgO
MgCl2
Mg3N2
Mg(NO3)2
MgCO3
Mg(OH)2
颜色
白色
白色
淡黄色
白色
白色
白色
某同学推断产物中一定不存在氯化镁,你认为他的理由是_____________;
[提出猜想]分析以上资料,同学们认为淡黄色的固体可能是镁与空气中的_________(填写化学式)反应生成的;
[实验探究]如果让你设计实验验证上述猜想,你的方案是__________________
[实验结论]根据实验结果,写出镁条在空气中燃烧时发生反应的化学方程式: _____________、____________
[反思与评价]通过上述探究,你对燃烧的新认识是____________
四、分析与计算(本题包括l小题,共5分)
17.(5分)肥田粉是常用的氮肥,图为某品牌肥田粉的部分标签,为了计算该品牌肥田粉的纯度(硫酸铵的质量分数),小玉和小昊采用了两种不同的方法。
×××牌肥四份
有效成分:硫酸铵(NH4)2SO4
含氮量:20.0%
生产日期:
小玉根据标签所示的含氮量直接进行理论计算,过程如下:
解:硫酸铵中氮元素的质量分数:
 ×100%
×100%
=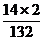 ×100%
×100%
=21.2%
设样品中硫酸铵的纯度为x
100%:21.2%=x:20.0%
x=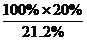 =94.3%
=94.3%
答:样品中硫酸铵的庸量分数为94.3%
小昊通过实验测得有关数据,然后进行计算,过程如下:
称取7.
Ca(OH)2+(NH4)2SO4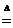 CaSO4+2NH3
CaSO4+2NH3 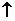 +2H2O
+2H2O
(请你在下面帮助小昊吴完成计算)
(1)小昊依据实验数据得出的计算结果和小玉的理论计算结果不相同,原因可能是__________________________________________________
(2)根据小昊实验的反应原理分析,施用肥田粉时应注意______________________