2009年福建省南平市初中毕业、升学考试
化学试卷
(满分:100分;考试时间:60分钟)
可能用到的相对原子质量: H - 1 O -
一.选择与判断(本题10小题,共30分,每题仅一个正确选项)
1.鱼肉、牛肉等食物中富含的营养素是……………………………………( )
A.油脂 B.糖类 C.维生素 D.蛋白质
2.下表是人体几种重要体液的正常pH范围,其中酸性最强的是
体液
唾液
胃液
血液
胆汁
正常pH范围
6.6~7.1
0.8~1.5
7.3 5―7.45
6.8~7.4
A.唾液 B.胃液 C.血液 D.胆汁
3.以下几种常见的化学肥料属氮肥的是…………………………………………( )
A.硫酸钾(K2SO4 ) B.尿素[CO(NH2)2]
C.磷矿粉[有效成分Ca3(PO4)2 ] D.磷酸二氢钾(KH2PO4 )
4.下列关于煤、石油和天然气的说法错误的是…………………………………( )
A.都是可再生的能源 B.在地球上的蕴藏量都是有限的
C.都属于混合物 D.完全燃烧时都有二氧化碳生成
5.材料与人类生活密切相关。下列物品是由有机合成材料制成的是…………( )
A.羊毛衫 B.塑料脸盆 C.不锈钢餐具 D.玻璃杯
6.下列说法错误的是………………………………………………………………( )
A.区别硬水和软水可以用肥皂水 B.洗洁精在清除油污时起乳化作用
C.铁制品外表涂油漆只是为了美观 D.限制使用塑料袋有利于减少“白色污染”
7.下列实验操作正确的是…………………………………………………………( )
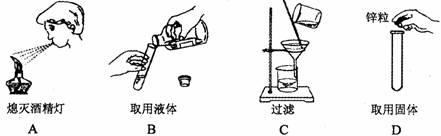
8.选择铸造硬币的金属材料不需要考虑的因素是………………………………( )
A.硬度 B.价格 C.耐腐蚀性 D.导电性
9.下图是水分解的微观示意图,其中 表示氧原子,●表示氢原子。以下说法正确的是…………………………………………………………………………………………( )
表示氧原子,●表示氢原子。以下说法正确的是…………………………………………………………………………………………( )
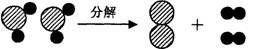
A.反应前后原子种类没有改变 B.图中所示微粒构成的物质均属于化合物
C.该反应属于置换反应 D.该反应的化学方程式为:H2O == H2 + O2
10.下图是甲、乙两物质的溶解度曲线,以下说法正确的是……………………( )
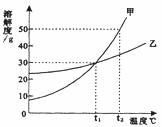
A.t
B.甲物质的溶解度大于乙物质的溶解度
C.甲、乙两物质的溶解度受温度影响的程度相同
D.t
二、填空与简答(本题5小题,共41分)
11.(10分)回答下列问题:
(1)在H、H2、H+中表示氢离子的是
(2)已知锂(Li)元素的化合价为+1,写出氧化锂的化学式 。
(3)在反应4HNO3
 4NO2↑+2H2O + X↑中,X的化学式为 。
4NO2↑+2H2O + X↑中,X的化学式为 。
(4)清凉油的主要成分薄荷脑(C10H10O)是由 种元素组成,分子中碳、氢、氧原子个数比为 。
12.(6分)氢氧化钠溶液和稀盐酸均为无色液体,区别它们常用 ;氢氧化钠跟盐酸反应的化学方程式为 ;医生常建议胃酸过多的病人可服用药品“斯达舒”(含氢氧化铝),其中氢氧化铝的作用是 。
13.(6分)某品牌牙膏中的摩擦剂是经过一系列加工而制得的极细小的碳酸钙粉末,它的生产过程如下:
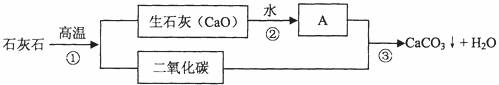
(1)请写出A物质的名称 (或化学式)
(2)请从①②③三个反应中选择一个,写出反应的化学方程式 。
(3)二氧化碳有许多用途,请举出其中一例 。
14.(11分)在成都市公交车燃烧事故的原因调查中,多项证据显示,有人携带汽油上车。
(1)当空气中悬浮着一定量的汽油时,一个小火星就足以使其燃烧,这说明汽油的着火点较 (选填“高”或“低”);汽油主要成分的化学式为C8H18,完全燃烧时生成二氧化碳和水,写出反应的化学方程式 。
(2)加油站必备的消防用品之一是沙子,用沙子灭火的原理是 。
(3)乘坐汽车、火车等公共交通工具时,下列物品禁止携带的是 (填序号,可多选,下同)。
A.鞭炮 B.瓶装饮料 C.书刊杂志 D.酒精
(4)这次事故引发了人们对公共交通消防安全问题的讨论,下列观点合理的是 。
A.公交车上要配备消防器材
B.公交车上坐椅用阻燃材料制成
C.对司乘人员进行消防安全知识培训
15.(8分)请根据常见金属性质回答问题:
(1)将以下常见金属的活动顺序补充完整。
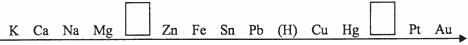
金属活动性由强逐渐减弱
(2)黄金首饰不易锈蚀的主要原因是 。
(3)从Mg、Zn、Cu、Fe中选出适当的物质与稀硫酸反应,写出反应的化学方程式
(写一个即可)。
(4)用CuSO4 配制农药波尔多液时不能在以下 (填序号)中进行。
A.塑料桶 B.铁桶 C.木桶
三.实验与探究(本题2小题,共1 9分)
16.(10分)结合以下实验室制取气体的常用装置回答问题:
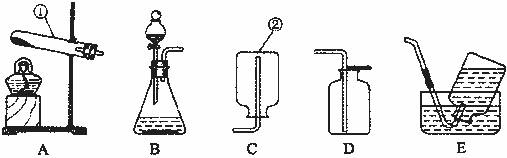
(1)写出标号仪器的名称:① ;② 。
(2)实验室用过氧化氢溶液与二氧化锰固体混合制取氧气时,应选用的发生装置是 (填序号,下同),收集装置是 ,反应的化学方程式为 。
(3)能用C装置收集的气体,必须具备的性质是 。

问题一:食盐加碘可以有效地预防
问题二:食盐是比较稳定的,而说明中强调“防热”是否因为受热会造成碘的损失?
【实验一】探究温度对碘损失率的影响
老师指导他们将一定浓度的碘酸钾溶液分成5等份,于不同温度下加热十分钟后,用硫代硫酸钠标准溶液测定碘酸钾浓度,计算碘损失率并记录如下:
温度
煮沸
碘损失率(%)
0
0.3
0.67
1
5.56
分析上表可得出的结论是 。
实验后,小林建议妈妈烧菜时最好是菜出锅前再放碘盐。
问题三:烧菜时加醋对碘的损失率是否也有影响?
【实验二】探究酸碱性对碘损失率的影响
(1)此组对照实验,要控制在碘酸钾溶液的浓度和质量、加热的 和 均相同,溶液的 不同的条件下进行。
(2)实验中需要调节溶液的酸碱性,下列物质不能选用的是 (填序号)。
A.氢氧化钠 B.纯碱粉末 C.食盐晶体 D.食醋
四.计算与分析(本题2小题,共1 0分)
18.(4分)配制
19.(6分)某厂生产的产品碳酸钠中混有少量碳酸氢钠。为了测定产品中碳酸钠的质量分数,取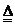 Na2CO3 + H2O + CO2↑
,碳酸钠受热不分解),完全分解生成二氧化碳气体
Na2CO3 + H2O + CO2↑
,碳酸钠受热不分解),完全分解生成二氧化碳气体
(1)样品中碳酸氢钠的质量。
(2)样品中碳酸钠的质量分数。