2009年四川省达州市高中阶段教育学校招生统一考试
化学试卷
(总分75分,50分钟完卷)
第Ⅰ卷(选择题 共24分)
可能用到的相对质量:H-1 O-16 S-32 Cl-35.5 Ba-137
一、选择题(每小题3分,共24分。只有一项符合题目要求)
1.绿色能源不会产生或残留对环境造成污染的物质,下列能源中不能称为绿色能源的是
A.铅蓄电池 B.氢能 C.风能 D.太阳能
2.下列物质中属于氧化物的是
A.高锰酸钾 B.臭氧(O3) C.干冰 D.矿泉水
3.不能用燃着的木条鉴别的一组物质是
A.空气和氧气 B.氮气和二氧化碳
C.聚乙烯塑料和聚氯乙烯塑料 D.羊毛和化纤布料
4.我国使用“长征3号甲”运载火箭将“嫦娥Ⅰ号”送上月球轨道,该运载火箭的动力是由高氯酸铵(NH4ClO4)分解所提供的,反应方程式为2 NH4ClO4===N2↑+Cl2↑+4H2O↑+2O2↑,请判断该反应的基本反应类型是
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
5.氢气不仅可以在空气中燃烧,还可以在氯气中燃烧,反应方程式为H2+Cl2===2HCl ,若用“○”表示氯原子,“●”表示氢原子,则上述反应可表示为
A.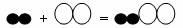 B.
B.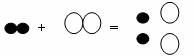
C.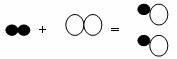 D.
D.
6.生活中常见的三种物质:①柠檬汁,②肥皂水,③食盐水。柠檬汁能使紫色石蕊试液变红,肥皂水显碱性,食盐水的pH=7。它们的pH由小到大排列,正确的是
A.①②③ B.①③② C.②①③ D.③①②
7.请你根据所学化学知识判断,不列说法正确的是
A.铁管在潮湿的空气中不易锈蚀 B.铵盐氮肥与碱性物质混合施用
C.天然气泄漏,点火寻找泄漏处 D.体温计中的水银属于金属材料
8.在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:
物质
甲
乙
丙
丁
反应前的质量(g)
20
50
80
30
反应后的质量(g)
0
100
10
x
请根据质量守恒定律判断x的值
A.50 B.
第Ⅱ卷(非选择题 共51分)
二、填空题(本大题共3个小题,共18分)
9.(4分)已知浓硝酸是一种易挥发的强酸,见光易分解,其分解的反应方程式为:4HNO3===2H2O+4NO2↑+X↑。根据上述信息,回答下列问题:
⑴浓硝酸的化学性质: (写出一种即可);
⑵水中氢、氧元素的质量比: (最简整数比);
⑶判断X的化学式: ;
⑷二氧化氮分子由氮原子和氧原子构成,其中,氮原子的原子结构示意图为 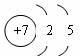 ,氮原子的最外层上的电子数为:
。
,氮原子的最外层上的电子数为:
。
10.(6分)为了探究“不的净化”过程,某实验小组从护城河中取了水样,观察到:
A.水样呈黄色,有异味 B.水样浑浊,有固体小颗粒。
现对水样进行如下处理:
⑴向水样中加入明矾搅拌溶解,静置一段时间后,进行 (填操作名称),除去固体小颗粒,再向滤液中加入活性炭,利用其 性除去水样中的颜色和异味,该过程属于 变化(填“物理”或“化学”)。
⑵通入氯气杀菌消毒,得到自来水,发生的反应如下:Cl2+H2O=HCl+HClO(次氯酸)。请判断,次氯酸中氯元素的化合价为 。
⑶为了判断得到的自来水是硬水或软水,可加入 进行检验。
⑷将自来水蒸馏得到纯净水,把下列物质分别加入纯净水中,用玻璃棒不断搅拌,能形成无色溶液的是 (填序号)。
A.粉笔灰 B.硫酸铜 C.蔗糖 D.食用油
11.(8分)实验室中,利用下列装置可以制取某些气体,请回答下列问题。
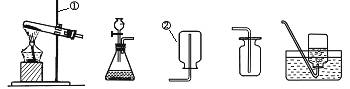
A B C D E
⑴写出带标号的仪器的名称:① ;② 。
⑵向气体发生装置内加入药品前,应该进行的操作是 。
⑶实验室若用高锰酸钾制取氧气,选择的发生装置是 ;用双氧水制氧气的化学方程式为
⑷乙炔又称电石气,是一种无色、无味、密度比空气略小,不溶于水的气体;工业上常用它燃烧产生的高温来切割和焊接金属;实验室用电石(固体)与水反应制取乙炔。你认为制取乙炔应选择的发生装置是 ;收集装置是 。
三、简答题(本大题共3个小题,共17分)
12.(4分)某种营养素补充剂的标签如下:
【主要原料】 碳酸钙、维生素D、大豆油、明胶……
【功效成份及含量】每
【注意事项】本品不能代替药品,不宜超过推荐量或与同类营养补充剂同时食用
⑴标签中的“钙
A.元素 B.原子 C.分子 D.离子
⑵该营养素具有补钙功能,同时还能补充人体所需的营养成分: (写出一种即可)
⑶淀粉是人们食用的最主要的糖类,由于淀粉能与碘作用呈 色。因此常用碘水(或碘酒)来检验食物中是否含有淀粉。
⑷蛋白质是人体所需的重要营养成分之一,是构成细胞的基础物质,人如果食用甲醛溶液浸泡过的鱼会危害身体健康,其原因是 。
13.(7分)请根据下列已知条件设问,使其成为一道完整的计算题,然后解答。
一定质量的氯化钡(BaCl2)固体和
14.(6分)有A、B、C、D四种物质,如图所示,A、B、C在一定下可以发生转化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A。D与A、B、C均能发生反应,D与C发生中和反应,D与A反应有CO2气体产生,D与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀。

⑴请根据已知条件推断四种物质的化学式:
A B C D
⑵请写出下列反应的化学方程式:
C溶液中通入CO2,溶液变浑浊
D与A反应
四、探究题(本大题共2个小题,共16分)
15.(11分)小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
【探究目的】探究所得溶液的酸碱性
【提出猜想】所得溶液可能呈碱性,也可能呈 性,还可能呈 性。
【实验验证】
实验操作
实验现象
结论
用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡
无色酚酞试液变
溶液呈碱性
无色酚酞试液不变色
溶液呈
【分析与思考】
⑴若溶液呈碱性,则溶液中使其呈碱性的离子是 (填写微粒符号),为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入 溶液,直到不再产生沉淀为止。然后过滤,把滤液倒入蒸发皿中加热,得到氯化钠晶体,该过程涉及的化学方程式为 。
⑵若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入碳酸钠溶液,若观察到 ,则所取溶液呈酸性;若无明显现象,则呈中性。
方案二:取样,加入金属锌,若有所泡产生,则所取溶液呈酸性,该反应的化学方程式为 ;若无明显现象,则呈中性。
16.(5分)下表是生活中某种常见金属X的部分性质:
颜色状态
硬度
密度
熔点
导电性
导热性
延展性
银白色固体
软
良好
良好
良好
将金属X投入盐酸中,有大量气泡生成。根据上述信息,回答下列问题:
⑴试推断金属X可能的一种用途 。
⑵将金属X放入硫酸铜溶液中,观察到的现象是 。
⑶请自选试剂,设计实验比较金属X与Mg的活动性强弱。完成下表:
你的一种猜想
操作
现象
结论
假设成立,金属X的活动性比镁弱