2008-2009学年度淄博市周村和平学校第一学期九年级期末考试
化学试卷
相对原子质量:H:
第Ⅰ卷 选择题
一、选择:每小题给出的四个选项中,只有一个是正确的,将正确答案填入题后答题栏中。
1.下列括号中对日常生活的变化判断正确的是
A.嘴嚼米饭时有甜味(化学变化) B.玻璃窗破裂(化学变化)
C.用醋酸清洗热水瓶的水垢(物理变化) D.纯净物加热后变为混合物(物理变化)
2.下列图示实验操作中,正确的是 ( )

A.加热液体 B.滴加试剂 C.过滤 D.读取液体体积
3.2008年6月中旬,奥运圣火在重庆境内传递,以表达重庆市民迎奥运的热烈心情。火炬燃烧必须具备的条件是①有可燃物②有足够的氧气③温度达到可燃物的着火点④使用铝合金作外壳
A.①②③ B.②③④ C.①③④ D.①②④
4.下表列出了不同温度下每立方厘米活性炭所能吸附的常见气体的体积。分析表中数据与气体组成、性质等的关系,你认为下列结论正确的是
H2
CO2
O2
N2
Cl2
气体的沸点(℃)
?252
?78
?183
?196
?34
被吸附的体积(mL)
4.5
97
35
11
494
A.气体分子所含原子个数多时,气体易被吸附
B.沸点越低的气体,越易被吸附
C.气体是化合物时,易被吸附
D.气体的相对分子质量越大,越易被吸附
5.以下对生活中的一些事实解释不合理的是
A.铁栏杆上涂油漆是为了防止生锈
B.在水中加入明矾是为了杀死水中的细菌
C.油锅着火时盖上锅盖是为了隔绝空气
D.在暖瓶中倒入食醋是为了除去水垢
6.有专家分析认为美国“哥伦比亚”号航天飞机在空中失事的原因可能是航天飞机机壳底部的石墨瓦在空中脱落,击中机翼。航天飞机表面覆盖石墨瓦可以起隔热和保护作用,这主要是因为石墨
A.能导电 B.熔点高、耐高温,化学性质稳定
C.有润滑作用密度小 D.硬度小
7.合金在我们的生产和生活中有着广泛的用途,下列关于“合金”的叙述:①合金中至少有两种金属;②合金中元素以化合物形式存在;③合金中一定含有金属;④合金一定为混合物;⑤合金依然具有金属特性,其中正确的是( )
A.④ B.①②③ C.③④ D.③④⑤
8.小刚把锌片投入到一种溶液中,他观察到锌片溶解且溶液质量减轻,又没有气体产生。这种溶液可能是
A.H2SO4 B.CuSO
9.下列是小红配制一定溶质质量分数的NaOH溶液的实验操作,其中会引起NaOH溶液中溶质的质量分数偏小的是
A.称量完固体NaOH时天平指针略向左倾斜
B.实验所用的固体NaOH在空气中久置已部分变质
C.转移已配好的溶液时,有少量溶液洒落在瓶外
D.量取水时俯视读数
10.
A.甲>乙 B.甲<乙 C.甲=乙 D.不一定
11.根据下列金属与盐溶液发生的置换反应,判断x、y、z三种金属单质的活动性顺序为
z + ySO4 → zSO4 + y x + z(NO3)2 → x(NO3)2 + z
A.x>y>z B.z>x>y C.z>y>x D.x>z>y
12.“三效催化转换器”可将汽车尾气中的有毒气体处理为无污染的气体,下图为该反应的微观示意图(未配平),其中不同符号的球代表不同种原子。下列说法不正确的是
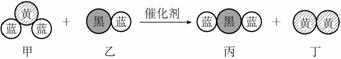
A.乙和丙中所含元素种类相同 B.甲和丁中同种元素化合价不相等
C.该反应中共有三种元素 D.化学方程式中乙、丁的化学计量数均为1
13.为研究铁丝的粗细对铁在氧气中燃烧的影响,下列实验能达到目的的是( )
A.在同一瓶氧气中,先后进行不同粗、细铁丝的燃烧实验
B.在两瓶不同浓度的氧气中,分别同时进行粗、细铁丝的燃烧实验
C.在两瓶相同浓度的氧气中,分别同时进行粗、细铁丝的燃烧实验
D.在两瓶不同浓度的氧气中,分别同时进行相同铁丝的燃烧实验
14.钨是熔点最高的金属,可以制作灯泡中的钨丝。冶炼钨的过程中有反应:
WO3+3H2 W+3H2O。从该化学方程式中你能获得的信息有
W+3H2O。从该化学方程式中你能获得的信息有
A.化学反应速率很快 B.此反应属于复分解反应
C.氢气是最轻的气体 D.此反应的发生需要吸收能量
15.物质的性质决定物质的用途。下列因果关系不成立的是
A.因为磷燃烧能产生白烟,所以可用于制作烟幕弹
B.因为铜化学性质不活泼,所以可用铜制造火锅
C.因为氮气化学性质不活泼,所以常用于食品防腐
D.因为石墨具有导电性,所以可用于制作电极
16.下列事实及对这些事实的解释,二者不相符合的是
A.金属导电………………………………原子是运动的
B.夏天钢轨之间的缝隙变小……………原子之间有间隔
C.糖是甜的,醋是酸的…………………不同分子性质不同
D.电解水制取氢气和氧气………………分子在化学反应中可以再分
17.齐齐哈尔市第二制药有限公司生产、销售假药案件,造成了多人死亡的严重后果。而该公司生产的“亮菌甲素注射液”等假药的原料即来自于江苏泰兴化工总厂的假“丙二醇”。其真丙二醇的化学式为C3H8O2,下列说法错误的是
A.丙二醇中碳氢氧元素的质量比为3∶8∶2
B.丙二醇的相对分子质量是76
C.丙二醇充分燃烧的生成物是二氧化碳和水
D.每个丙二醇分子含13个原子
18.下图是甲、乙、丙、丁四种物质的溶解度曲线,温度 为t℃时,将等质量甲、乙、丙、丁四种物质分别加到

A.甲 B.乙 C.丙 D.丁
19.某无色气体可能含有CO2、CO、H2中的一种或几种,依次进行以下实验(假设每步反应均完全进行);①通过赤热的炭层后,恢复到原状态,气体体积不变;②通过灼热的CuO时,固体变成红色;③通过白色CuSO4粉末时,粉末变成蓝色晶体;④通入澄清石灰水中,石灰水变浑浊。下列判断正确的是
A.原混合气体中一定含有CO2、CO、H2
B.原混合气体中一定没有CO2,可能含有H2和CO
C.原混合气体中一定含有H2和CO,可能含有CO2
D,根据①④,可推断实验过程中一定有CO2生成
20.Y、Z、W是四种不同的金属,为比较金属活动性的强弱,某同学利用这四种金属单质、盐酸、Z的硝酸盐、W的硝酸盐,进行有关实验,结果如下表(能发生置换反应的记为“√”,不能反应的记为“一”,无标记的表示未做该实验)。这四种金属的活动性顺序为
X
Y
Z
W
盐酸
√
―
―
√
Z的硝酸盐
√
W的硝酸盐
√
―
A.X>W>Y>Z B.X>Y>W>Z C.W>X>Y>Z D.Y>W>Z>X
第Ⅱ卷 选择题
21.氧气是一种重要的物质,根据你对氧气的认识填写下列空白。
(1)人类生存离不开氧气,氧气约占空气总体积的 。
(2)实验室里有多种方法可以制氧气,写出用过氧化氢溶液制氧气的化学方程式:
(3)下列化学变化中,氧气不作为反应物的是
①天然气燃烧 ②缓慢氧化 ③光合作用 ④钢铁生锈
22.下图中的①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。请你回答:


(1)氟元素的相对原子质量为 ,钙元素的原子序数为 ;
(2)X= ;
(3)A、B、C、D属于同种元素的粒子是 (填序号);
(4)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似 (填序号);
23.请你各举一个实例,说明下列有关溶液的叙述是错误的。
(1)溶液一定是无色的。实例:_____________(填化学式)溶液,不是无色的。
(2)溶液中的溶质一定是固体。实例:________(填化学式)可做溶质,但不是固体。
(3)某溶液露置在空气中一段时间后,溶质的质量分数一定变大。实例___________(填名称)在空气露置一段时间后,溶质的质量分数是变小的。
24.经过课外的学习发现,金属锰(Mn)也能排到下列的金属活动性顺序表中:
K、Ca、Na、_____、Al、Mn、Zn、Fe、Sn、Pb、(H)、Cu、Hg、_____、Pt、Au
(1)用元素符号完成上述金属活动性顺序表
(2)根据对上表的分析,发现Mn位于Al、Zn之间,请你设计合理的实验证明,写出有关的化学方程式_________________________________________ (Mn的化合价显+2价)。
25.甲乙丙三种物质的溶解度曲线如下图所示。据图回答:
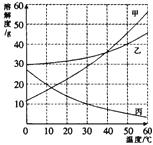
(1)要使接近饱和的甲乙丙三种物质溶液变为饱和,均可采取的一种措施是 ;
(2)要从甲和丙混合物中提纯甲可采取的方法是
(3)将等质量
26.请根据下表信息回答:
序号
金属
熔点/℃
导电性
硬度
化学性质
金属冶炼的大致年限
①
Al
660
61
2~2.9
常温下与氧气反应,表面形成致密的薄膜
约200年前
②
Fe
1535
17
4~5
在潮湿的空气着火易生锈
约3000年前
③
Cu
1083
99
2.5~3
在高温时易与氧气反应
约6000年前
说明:导电性以银的导电性为100作标准,硬度以金刚石的硬度为10作标准。
(1)菜刀用铁做而不用铝做的主要原因是 ;
(2)表中导电性最强的金属是 ;
(3)①中形成薄膜的化学方程式 ;
(4)金属的冶炼体现了人类文明的发展水平。之所以有先后,主要取决于 。
27.
【资料在线】我国生活饮用水的标准
感官指标
化学指标
细菌学指标
水质无色无味
且澄清透明
pH 6 5~8.5;总硬度<250mg/L。
(以碳酸钙计);铜<l 0mg/L,……等
细菌总数<100个/mL等
(1)除去水中难溶性的固体物质可用___________的方法。
(2)榆验水样是硬水还是软水,可用的物质是___________
(3)符合感官和化学指标的水还不一定是安全的饮用水,理由是__________________
_____________________________________
28.1909年化学家哈伯在实验室首次合成了氨。2007年化学家格哈德?埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,获得诺贝尔化学奖。
(1)将氢气和氮气在高温、高压和催化剂的条件下合成氨(NH3)。反应的化学方程式为_________________________________________。
(2)用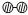 、
、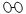 、
、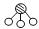 分别表示N2、H2、NH3。观察下图,写出符合在催化剂表面合成氨反应过程的顺序________________________(将下面五张图按反应过程顺序用序号排列)。
分别表示N2、H2、NH3。观察下图,写出符合在催化剂表面合成氨反应过程的顺序________________________(将下面五张图按反应过程顺序用序号排列)。
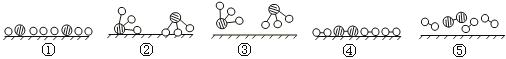
(3)表面化学对于化学工业很重要,它可以帮助我们了解不同的过程。在潮湿的空气里,铁表面吸附了一层薄薄的水膜,同时由于空气中O2的溶解,水膜呈中性。若空气中CO2溶解,水膜呈酸性,写出该反应的化学方程式______________________。
三、实验于探究
29.过氧化氢(H2O2)溶液在二氧化锰(MnO2)作催化剂的作用下能迅速分解生成氧气和水。分液漏斗可以通过调节活塞控制液体的滴加速度,如图所示,回答下列问题:

(1)分液漏斗中应放入的物质是___________锥形瓶内应放入的物质是_____________。
(2)要收集一瓶纯净的氧气,应选择装置___________(填序号)。
(3)某同学在观察到锥形瓶内有大量气泡时,开始用B收集氧气,过一段时间后,用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃,其原因是________________________。
(4)若实验时用此方法代替加热高锰酸钾制取氧气,优点是_____________(填序号)。
①生成物只有氧气 ②不需加热 ③需加热
(5)装置A中反应剧烈,据此提出的安全注意事项是__________________(填序号)。
①控制液体的滴加速率
②用体积较小的锥形瓶
③加热反应物
30.实验室欲配制
(1)计算:需氢氧化钠固体
g,水
mL(水的密度是
(2)称量:用质量为
砝码/g
100
50
20
20
10
5
打“√”表示选用
并在下列标尺中选出能正确表示游码位置的选项 (填字母)
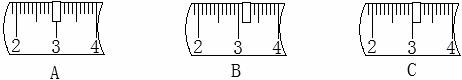
(3)溶解:将氢氧化钠固体溶于水,用 搅拌,使氢氧化钠全部溶解,冷却至室温。把配好的溶液装入试剂瓶,盖好瓶盖并贴上标签,放入试剂柜中。
四、分析与计算(本题包括1小题,共5分)
31.某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成。分四次取样品与稀硫酸反应,其实验数据记录如下表。
1
2
3
4
取样品质量(g)
50.0
50.0
50.0
50.0
取稀硫酸质量(g)
40.0
80.0
120.0
160.0
产生气体质量(g)
0.4
0.8
1.0
1.0
试计算(1)黄铜中锌的质量分数
(2)所用稀硫酸中溶质的质量分数
32.草木灰是农村常用的一种钾肥,其中只有其有效成分K2CO3能溶于水。实验中学化学兴趣小组的同学为了测定某草木灰中K2CO3的含量,称取该草木灰
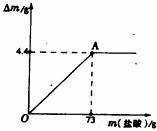
(1)写出坐标中曲线上A点的含义:______________________________________________
__________________________________________________________;
(2)草木灰中K2CO3的质量分数和所用稀盐酸中溶质的质量分数各是多少?