2008-2009学年度山东省泗水县第一学期九年级期末考试
化学试卷
可能用到的相对原子质量:H-1
O-16 Na
I卷 选择题 (共16分)
一、选择题(1-4题每题1分、5-10题每题2分共16分)
1.下列物质中,属于纯净物的是( )
A.洁净的空气 B.矿泉水 C.碘酒 D.胆矾
2.下列关于原子的叙述中,不正确的是( )
A.原子是构成物质的一种微粒
B.原子不带电是因为原子中不存在带电的微粒
C.原子在不停地运动
D.原子是化学变化中的最小微粒
3.下列各组微粒中,属于同一种元素的是( )
A.Cl和Cl-
B.CO2和CO C.H和He
D. 
4.能决定元素种类的是( )
A.电子数 B.中子数 C.最外层电子数 D.质子数
5.下列敞口放置的物质,一段时间后质量增加并发生化学变化的是( )
A.浓硫酸 B.浓盐酸 C.生石灰 D.氯化钠
6.学习化学我们要经常做实验,根据你的理解下列操作正确的是( )
A.将鼻子凑到容器口去闻药品的气味 B.用过滤法除去水中的难溶性杂质
C.直接用手拿药品 D.将水倒入浓硫酸中
7.下图是a、b、c三种物质的溶解度曲线,现有一定温度下的a、b、c的不饱和溶液,分别通过加溶质、蒸发溶剂或升高温度三种方法,均可变成饱和溶液的是( )

A.a的溶液 B.b的溶液 C.c的溶液 D.a溶液和c的溶液
8.下列化学方程式符合题意且书写正确的是( )
A.不能用铁制容器配制波尔多液:2Fe+3CuSO4=Fe2(SO4)3+3Cu
B.炼铁时用一氧化碳还原氧化铁:Fe2O3+3CO高温2Fe+3CO2
C.医疗上用氢氧化镁中和胃酸过多:Mg(OH)2+H2SO4 =MgSO4+2H2O
D.证明铜的活动性比银强:Cu+2AgCl=CuCl2+2Ag
9.下列叙述不正确的是( )
A.在不同的碱性溶液中OH-越多,碱性越强,PH越大
B.酒精不属于人们常说的化石燃料
C.用滴加Na2CO3溶液或通入CO2气体的方法,可鉴别澄清石灰水和氢氧化钠溶液
D.燃烧、缓慢氧化和自燃的相同点是都属于氧化反应并有热量放出
10.在一定质量分数的氯化钠饱和溶液中逐渐加入食盐固体,下列图像符合该溶液中溶质质量分数变化规律的是( )

(Ⅱ卷 非选择题 共34分)
二、填空与简答题:(共15分)
11.(4分)甲、乙、丙、丁、戊五种元素,甲的单质是空气中含量最多的气体;乙是地壳中含量最多的金属元素;丙是地壳中含量最多的元素;丁元素原子核外只有一个电子;戊是地壳中含量居第二位的金属元素、也是常用的黑色金属。用化学符号填空:
甲的单质是____;丙和丁形成的化合物是____;乙的原子结构示意图是____。丙、丁、戊三种元素形成的红褐色化合物是____。
12.(4分)生活中有许多物质需要密闭保存,如酒精溶液和碳酸饮料。因为酒精易挥发,挥发出的是__(填名称)分子;碳酸饮料中的碳酸易分解,分解产生的物质是____。结合以上两个实例,谈谈你对挥发和分解反应的认识_____________。酒精(以X表示)燃烧的化学方程式为
X+3O2点燃2CO2+3H2O,则酒精的化学式为_________。
13.(2分)为验证相同状况下二氧化碳气体的密度比空气大,通常用:取等质量的同样大小的两容器(如气球、针筒、烧杯等),分别收集等体积的二氧化碳气体和空气,然后称其质量的方法。该方法的原理是___________。
14.(5分)可生成二氧化碳的反应很多,例如:①酒精的燃烧 ②木炭在空气中燃烧③高温下碳与氧化铜反应 ④高温煅烧石灰石 ⑤石灰石与稀硫酸反应 ⑥石灰石与稀盐酸反应 ⑦碳酸钙粉末与浓盐酸 ⑧人和动物的呼吸作用。其中可用于实验室中制取二氧化碳的是_____ ,(填序号)原因是:____。请分类说明某些反应不能用于实验室中制取二氧化碳的原因_________。
三、实验与探究(共13分)
15.(8分)甲、乙两同学想了解氢氧化钠溶液的酸碱性。他们做了以下研究:
实验操作
检测结果
甲同学
取pH试纸放在玻璃片上;用玻璃棒蘸取氢氧化钠溶液沾在PH试纸上;将试纸显示的颜色与标准比色卡比较。
pH>7
乙同学
将pH试纸直接浸入氢氧化钠溶液中,把试纸显示的颜色与标准比色卡比较。
pH>7
(1)根据两位同学的实验可得出氢氧化钠溶液酸碱性的结论:_______________。
(2)根据两位同学的实验操作,你认为 ______同学操作不规范。为什么?
(3)如果实验室没有pH试纸,又要一次测定未知溶液的酸碱性,可选用_____试液来进行实验,该试剂从____色变成____色,能确定其酸碱性;若实验室有两瓶失去标签的氢氧化钠溶液,一瓶浓溶液、一瓶稀溶液____(填能或不能)用该试剂测定其浓稀,原因是_________。
16.(5分)下图是初中化学学习中的常见装置,请按要求回答下面问题:
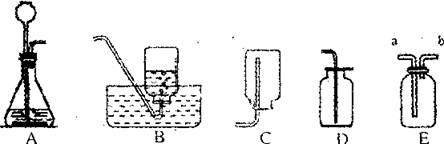
①利用上述装置的组合可以制取的气体有__,写出其中一种气体制备的化学反应原理___________________
②有的同学认为装置E可以代替装置B、C、D收集气体,欲收集具备下面性质的气体,应如何使用装置E?
收集比空气重的气体:_______________________________
收集难溶于水的气体:_______________________________
③装置E还具有其他用途,请举一例说明______________________
四、计算与应用(共6分)
17.(2分)核糖是人类生命活动中不可缺少的一种有机物,它的化学式是O5H10O5,
(1)核糖的相对分子质量是_______。
(2)核糖中碳元素的质量分数_______。
18.(4分)长期使用的热水壶底部有一层水垢,主要成分是碳酸钙和氢氧化镁,用稀盐酸可以清除水垢。某学校化学研究性学习小组的同学通过实验测定水垢中碳酸钙的含量:将过量的稀盐酸加入到
时间/s
0
30
60
90
120
150
180
增加的质量/g
0
60
100
120
132
132
132
(1)请在坐标纸上,以反应时间为横坐标,以NaOH溶液增加的质量为纵坐标,画出能够表明产生气体的质量随反应时间变化规律的关系曲线。并写出CO2气体被足量NaOH溶液吸收的化学方程式__________________
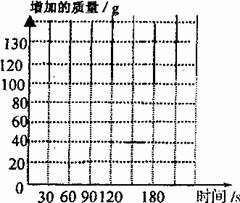
(2)从表中看出:NaOH溶液质量增加