2008-2009学年度金平区第一学期九年级教学质量评估
化学试卷
可能用到的相对原子质量:C-12 H-1 O-16 Ca- 40 Cl-35. 5
一、选择题(本大题14小题。1~8题每小题2分,9~14题每小题3分,共34分。)(每小题只有一个答案是正确的,请将正确答案填在答题卷相应题号的空格内)
1.下列有关空气中各成分说法正确的是
A.氧气化学性质比较活泼,能燃烧
B.氮气的化学性质不活泼,可在食品包装时充入防腐
C.稀有气体不与其他物质发生反应
D.二氧化碳含量增多会引起温室效应,属于气体污染物
2. 轻轨电车是近年来城市发展的一种无污染的新兴交通工具,当轻轨电车开动时,轻轨电车与架空电线的接触点由于高速摩擦会产生高温,因此接触点上的材料应该具有耐高温,不易氧化,能导电的性质,你认为接触点上的材料应选用
A.金刚石 B.铝 C.石墨 D.铜
3.下列事实及对这些事实的解释,二者不相符合的是
A.夏天钢轨之间的缝隙变小……………原子之间有间隔
B.糖是甜的,醋是酸的…………………不同分子性质不同
C.金属导电………………………………原子是运动的
D.电解水制取氢气和氧气………………分子在化学反应中可以再分
4.利用太阳能使水分解产生氢气是人们的愿望。我国科学家在寻找光解水的催化剂方面取得了很大的进展,BaTi4O9是最新研究的催化剂之一,该物质中钛元素(Ti)的化合价为
A.+4
B.+
5.化学的研究目的就是帮助人们认识、改造和应用物质,把金属矿物冶炼成金属就是人们利用化学方法实现物质改造的典型范例。下表中不同的金属被开发和利用的年代不同,从化学反应的角度看,决定这一年代先后顺序的关键因素是
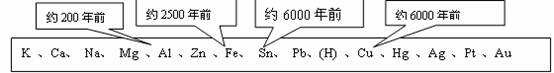
A.地壳中金属元素的含量 B.金属的活动性
C.金属的延展性 D.金属的导电性
6.下列化学实验基本操作正确的是
①把烧杯放在铁圈上直接加热;
②点燃可燃性气体前,不一定要先检验气体纯度;
③制O2结束时,先熄灭酒精灯,后将导管移出水面;
④用完酒精灯,必须用灯帽盖灭,不可用嘴去吹灭;
⑤制取氧气结束后,应立刻把装反应物的试管用冷水冲洗干净;
⑥制备气体时先检验装置的气密性,后装药品
A.①和② B.②和④ C.④和⑥ D.③和⑤
7.为了解决人们饮水问题,某地对河水进行净化,进而达到饮用水的标准。下列采取的净化步骤合理的操作顺序是
①化学沉降(用明矾) ②杀菌消毒(用漂白粉) ③自然沉降 ④过滤
A.③④①② B.③①④② C.①②③④ D.①③②④
8.利用家中的杯子、玻璃及塑料瓶子、碗、筷、匙、饮料吸管、棉纱,进行家庭小实验时,即使经过加工改造,对下列实验室中的常见仪器,也无法替代的是
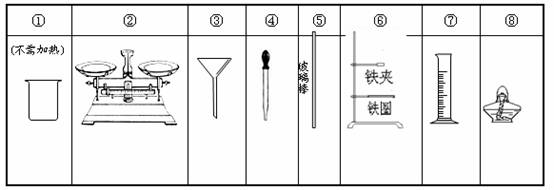
A.②⑥ B.③⑦⑧ C.②③⑥ D.无法确定
9.下图是元素周期表中的一种元素,下列有关该元素的信息正确的是

A.相对原子质量是11 B.它是非金属元素
C.原子在化学反应中容易得电子 D.原子序数是11
10.通过下列实验可以得出的结论,其中不合理的是
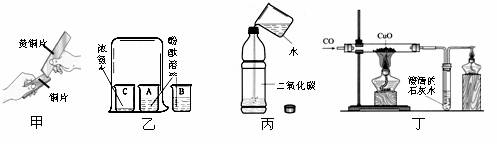
A.甲实验中黄铜片能在铜片上刻画出痕迹可以说明黄铜的硬度比铜片大
B.乙实验既可以说明分子在不停的运动着,又可以说明氨水显碱性
C.丙实验既可以说明二氧化碳易溶于水,又可以说明二氧化碳具有酸性
D.丁实验既可以说明一氧化碳具有还原性,又可以说明一氧化碳具有可燃性
11.某学生用量筒量取液体,量筒摆放平稳,且学生面对刻度,他首先俯视液面读数为79mL,倾倒出部分液体后,又仰视读数为70mL,则该生实际倒出的液体的体积为
A.9mL B.大于9mL C.小于9mL D.无法判断
12.下列各图所示装置的气密性检查中,漏气的是

A B C D
13.晓航同学用光亮的铁丝做了如图所示实验。放置1―2周后,他观察到I、II中铁丝 无变化;III中铁丝生锈,试管内液面上升约1/5体积。于是得出下列分析结果:①铁在潮湿空气中易生锈 ②空气中氧气约占1/5体积 ③铁不能与氧气反应 ④用表面刷漆的铁丝进行实验III,铁丝无变化,试管内液面不上升 ⑤ 不能确定铁生锈是否与二氧化碳有关。其中正确的分析结果是

A.①②④⑤ B.①②③④ C.①③④ D.①②③④⑤
14.某密闭容器内有四种物质,在一定条件下充分反应。测得反应前后各物质质量如下表,下列有关说法中不正确的是
物 质
X
Y
Z
Q
反应前质量/g
224
10
0
2
反应后质量/g
2
170
44
a
A.a的值等于20
B.X是反应物
C.该反应属于化合反应
D.若Y和Z的相对分子质量之比为20:11,则Y和Z的化学计量系数(即化学方程式中化学式前的系数)之比为2:1
二、填空题(本大题4小题,共23分。请把下列各题的正确答案填写在答题卷对应的横线上)
15.(6分)请用恰当的化学用语填写在横线上:
①汽水中含有的一种酸 ;
②可用于制干冰、温室气体肥料 ;
③“西气东输”工程中输送天然气 ;
④“五粮液”的主要成分(除水之外) ;
⑤两个镁离子 ;
⑥氧化铝中铝元素的化合价显+3价 。
16.(4分)高铁酸钾(K2FeO4)是具有紫色光泽的微细结晶粉末,它的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌、灭藻的新型、高效的多功能水处理剂。干燥的高铁酸钾在
(1)高铁酸钾的物理性质是 ;
(2)保存高铁酸钾时应注意 ;
(3)试完成高铁酸钾与水反应的化学方程式。

17.(3分)根据下列几种粒子的结构示意图,回答问题。

(1)其中属于阳离子的是 (填序号,下同)
(2)具有相似化学性质的元素是 。
(3)某元素R形成的氧化物为R2O3,则R的原子结构示意图可能是 。
18.(10分)化学家舍勒和普利斯特里早在18世纪就先后独立发现了氧气,但由于受“燃素理论”的影响(即认为一切可以燃烧的物质都是由灰和“燃素”组成,物质燃烧后剩下灰,而燃素则变成光和热,散逸到空气中),使他们放弃了自己的研究成果 。根据“燃素”理论推知:燃烧后物质的质量应该减少,但法国化学家拉瓦锡在研究磷以及一些金属燃烧时,应用天平作为研究工具,作了大量实验,实验结果都与“燃素理论”相违背。他大胆质疑,尊重实验事实,进行深入研究,克服重重阻力,打破了“燃素理论”真正发现了氧气。请回答:
⑴拉瓦锡之所以成为氧气的真正发现者,应该归功于他具有_____________________ _________________________ 的科学精神。
⑵拉瓦锡推翻“燃素理论”的实验事实_______________________________________。 ⑶用学过的理论解释磷燃烧时质量的变化情况 _____________________________
_________________________________________。
⑷写出用高锰酸钾制取氧气的化学方程式___________________________________ 。
⑸实验室可以用 _______________ 或 _______________ 法收集氧气。
⑹用(4)(5)中的方法制取并收集氧气,需要用到的玻璃仪器是(填序号) 。
a试管;b漏斗;c酒精灯;d导管;e胶头滴管;f集气瓶;g量筒;h玻璃水槽
三、(本题共3小题,18分)
19.(4分)自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:

(1)图乙所示反应的基本反应类型为 反应;
(2)D物质中氯元素的化合价为 ;
(3)写出图甲所示反应的化学方程式 。
20.(6分)根据下列信息写出相应的化学反应方程式:
(1)实验室用双氧水制氧气既方便快捷又环保 ;
(2)燃烧红磷当烟幕弹 ;
(3)人们炸油条时,当面团放入油锅后,碳酸氢钠(NaHCO3)受热分解成碳酸钠、水和二氧化碳,不断产生的二氧化碳会使油条膨胀并浮出油面。其中碳酸氢钠(NaHCO3)受热分解的化学反应方程式为: 。
21.(8分)现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为浅绿色溶液,G 为蓝色溶液,它们之间存在如下关系:
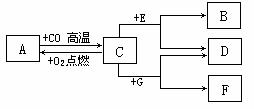
(1)推测下列物质的化学式:B ,D ,F ;
(2)写出C→A转化的化学方程式: 。
四、实验题(本题包括3小题,共28分)
22.(6分)为了探究影响金属与酸反应程度的因素,进行了以下实验
实验序号
实验过程
实验现象
1
镁粉和铁粉分别与5%盐酸反应
镁粉产生气体快
2
铁粉和铁片分别与10%盐酸反应
铁粉产生气体快
3
铁片分别与5%盐酸和10%盐酸反应
10%盐酸产生气体快
由此得出影响金属与酸反应剧烈程度的因素有:
因素一:_________________________________________________;
因素二:_________________________________________________;
因素三:_________________________________________________。
23.(7分)(1)纸火锅(见下图)在城市里悄然兴起,这种纸火锅精巧漂亮,白色的底衬着火锅食料,干净、醒目;纸火锅在使用时无烟、无味;不会被火点燃。纸火锅烧不着的原因是: ___________________________。

(2)人们常使用固体酒精做为纸火锅加热的热源。小刚观察到服务员用盖子熄灭固体酒精。服务员利用的灭火原理是___________________________ 。
(3)小刚无意中发现,将饮用的某品牌碳酸饮料所放出气体喷在燃烧着的固体酒精上,火焰熄灭。
【猜想与假设】根据上述现象推测,该气体是____________,该气体所具有的性质是______________________________。
【实验验证】将该气体通入澄清石灰水,有白色沉淀生成,该反应的化学方程式是
。
24.(15分)下图是实验室用于制取、干燥和收集气体的装置图。(浓硫酸或碱石灰可作干燥剂)
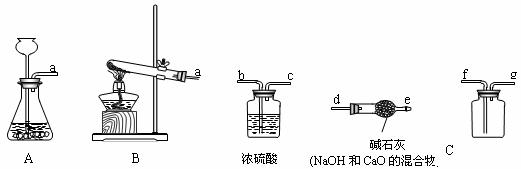
(1)写出组合成装置A的仪器名称:导管、______________、_________、__________
(2)若用装置A制取氧气,装置中放入的药品为:________________ 和_____________。
若用装置B制取氧气,写出反应的化学方程式: 。
(3)实验室制取二氧化碳气体的化学方程式:___________________________________。
现要制取并收集一瓶干燥的二氧化碳气体,请在上述装置中选择合适的装置,按气体的流向用导管的编号将装置连接好:a →___________________________________
(4)欲收集一种难溶于水的气体,可以利用C装置采用排水法来收集。请简述应如何使用C装置来收集该气体:________________________________________________.
若想知道收集的气体的体积,可以在排出水的导管连接一个量筒,请简述应如何正确读数?______________________________________________ ______。
五、计算题 (本题2小题,共17分)
25.(8分)新兴大脑营养学发现,大脑生长发育与不饱和脂肪酸有关。从深海鱼油中提取出来的一种不饱和脂肪酸被称为“脑黄金”,它的化学式为C26H40O2,它的一个分子中所含原子总数为______个,它是由_______种元素组成的,它的相对分子质量为________,其中碳与氢两种元素的质量比为________,碳元素的质量分数为(精确到0.1%)____ 。
26.(9分)石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用
稀盐酸的用量
第一次加入
第二次加入
第三次加入
第四次加人
剩余固体的质量
l g
(1)计算该石灰石样品中碳酸钙的质量分数。
(2)计算该