2008-2009学年度烟台市招远第一学期初四第二学段测评
化学试卷
第Ⅰ卷(选择题部分, 30分)
一、我会选择(本题共10个小题,每小题只有一个选项符合题意,每小题1分,共10分)
1.医生建议患甲状腺肿大的病人多食海带等海产品这是因为海带中含有丰富的
A.氟元素 B.碘元素 C.锌元素 D.钙元素
2.关于多金属结核的叙述,正确的是
A.多金属结核是锰的合金
B.多金属结核也称锰结核
C.锰结核中只有一种金属
D.全世界多金属结核含量微乎其微
3.下列说法中正确的是
A.浓溶液一定是饱和溶液
B.稀溶液一定是不饱和溶液
C.在一定温度下,析出晶体后的溶液一定是饱和溶液
D.饱和溶液的溶质质量分数一定比不饱和溶液的大
4.下列物质中不属于碱的是
A.纯碱 B.消石灰 C.火碱 D.氢氧化铜
5.下列物质不属于合金的是
A.不锈钢 B.青铜 C.磁铁矿石 D.生铁
6.小明为了证明铁的金属活动性比铜强,下列不能达到目的的试剂组是
A.铜片、氯化亚铁溶液 B.铁片、氯化铜溶液
C.铁片、铜片、稀硫酸 D.铁片、铜片、盐酸
7.下列铁制品在使用和保存时的注意事项,不正确的是
A.避免长期接触潮湿空气
B.用铁制品盛装食醋
C.应保持铁制品表面洁净、干燥
D.为防止机床生锈,在机床表面涂一层矿物油
8.如果人体缺乏某种维生素会使人患病,患夜盲症是由于缺乏
A.维生素A B.维生素B C.维生素C D.维生素D
9.关于蛋白质的有关说法错误的是
A.蛋白质是构成人体细胞的基础物质.
B.蛋白质是帮助人体生长和修补身体破损组织所需要的主要营养物质
C.人体对蛋白质的摄人是多多益善
D.蛋白质进入人体后,被分解成可被人体吸收的另一类重要有机物――氨基酸
10.下列关于糖类的有关认识不正确的是
A.糖类都属于高分子化合物
B.人体内在淀粉酶和水的作用下,淀粉转变成葡萄糖
C.人体所需热量的60%―70%来自糖类
D.可用碘水来检验食物中是否含有淀粉
二、我能选择(20分)(本题包括10个小题。每小题有l-2个选项符合题意-每小题2分,共20分。多选、错选均不得分,漏选1个扣1分)
11.下列关于人体健康的有关话题中不正确的是
A.体弱多病者应多补充一些蛋白质
B.人们体育锻炼后,消耗能量较大,应多补充一些葡萄糖
C.油脂在人体内消耗不完时,会以脂肪的形式储存起来,导致人体发胖,所以应尽量不吃油脂类食物
D.如果牙龈经常出血,应多吃一些水果和蔬菜
12.下列元素与人体关系的叙述中,不正确的是
A.缺铁会引起贫血 B.缺钙易患佝偻病或骨质疏松
C.缺硒易患坏血病 D.缺锌易引起生长迟缓、发育不良
13.化学在生活中无处不在。下列各项中,你认为合理的是
A.变霉大米用水洗净后煮熟可放心食用
B.合格的火腿肠中含有少量亚硝酸钠,因此也不能食用
C.不可用工业盐(NaNO2)腌制咸菜
D.CO与血红蛋白的结合能力比O2的大
14.根据维生素C能够使紫色高锰酸钾溶液褪色的原理,用下图所示的实验可以测定出苹果汁和橙汁中维生素C含量的相对多少。要得出正确结论,实验过程中不需要进行控制的条件是

A.烧杯中溶液的体积
B.两个胶头滴管滴出的每滴果汁的体积
C.烧杯中紫色高锰酸钾溶液的浓度
D.膝头滴管滴出的果汁的滴数
15.一定条件下,对同一反应而言,溶液中溶质的质量分数越大,反应速率越大。现用
①氢氧化钠 ②水 ③氧化镁 ④硫酸钠溶液
A.只有② B.①③ C.②④ D.②③④
16.下列从原料到制取较纯的最终产物的实验设计中,理论上正确、操作可行、经济上合理的是
A.Cu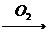 CuO
CuO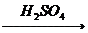 CuSO4
CuSO4
B.Cu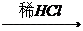 CuCl2溶液
CuCl2溶液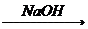 Cu(OH)2
Cu(OH)2
C.Fe  Fe2O3
Fe2O3
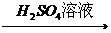 Fe2(SO4)3
Fe2(SO4)3
D.CaCO3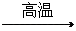 CaO
CaO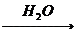 Ca(OH)2溶液
Ca(OH)2溶液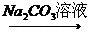 NaOH溶液
NaOH溶液
17.根据下图,下列说法错误的是
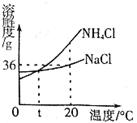
A.
B.NaCl和NH
C.将
D.t℃时,NH
18.某金属加工厂生产过程中产生的废液含有少量硝酸银和硝酸铜,为回收利用资源和防止污染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤出的固体中加入少量稀盐酸,无气体产生,则下列有关说法中正确的是
A.滤出的固体中含有银和铜,一定不含铁
B.滤出的固体中一定含有银,可能含有铜,一定不含铁
C.滤液中一定有硝酸亚铁,一定没有硝酸银和硝酸铜
D.滤液中一定有硝酸亚铁,可能有硝酸银和硝酸铜
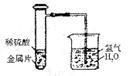
19.某中学兴趣小组,设计了如图所示的装置,用来研究不同金属跟稀硫酸反应的快慢,他们用此装置,选择了甲、乙、丙、丁四种大小相同的金属片,分别与相同体积、相同质量分数的稀硫酸反应,观察30s内从导管口冒出的氢气泡多少,记录在下表中.(“+”越多表示产生的气泡越多)
金属
甲 -
7
丙
丁
氢气泡多少
+ +
+ + + +
+ + +
+
如果四种金属分别是镁、铝、铁、锌中的一种,则甲最有可能是
A.镁 B.铝 C.铁 D.锌
20.t℃时,将某硝酸钾溶液第一次蒸发掉l
A.等于
第Ⅱ卷(非选择题部分,共70分)
三、我会填空(36分,每空1分)
21.(4分)(1)氢气是未来最理想的能源,具有广阔的开发前景,有许多优点。请写出三条①____________,②___________,③___________.
(2)人们正在开发和利用新能源,除了氢能源外,还有(任举一种)___________.
22.(5分)工业制玻璃的原料是___________、___________、___________.在玻璃窑中发生反应的化学方程式是______________________,______________________。
23.(4分)玻璃、塑料、玻璃钢、不锈钢四种物质,其中属于金属材料的是___________;属于无机非金属材料的是___________;属于有机高分子材料的是___________,属于复合材料的是___________.
24.(4分)以下是几种常见化肥的主要成分
①NH4HCO3 ②K2CO3 ③(NH4)2HPO4 ④KCl
(1)属于复合肥的是___________(填序号)
(2)如果小花发现自家的玉米苗得了“软骨病”,抗风力低,易倒伏,小花应建议父亲施___________(填序号)
(3)碳酸氢铵受热易分解,写出其反应的化学方程式______________________.
(4)以硫酸铵为例,用方程式标明铵态氮肥不能与碱性物质混合使用的原因_______________________________________________________。
25.(4分)某校食堂中的午餐食谱如下:
主食:大米饭
配菜:红烧排骨 煎鸡蛋 炸鸡腿 豆腐汤 炒猪肝
主食和配菜中应该主要含有维生素、___________、___________、___________、无机盐和水等物质,考虑到各种营养成分的均衡搭配,食谱中应该增加的配菜是___________.
26.(2分)春节就要到了,放假离校之际,你总要打扫卫生,……假设你在整理自己的东西时,清理出如下物品:A.废作业本 B.矿泉水瓶 C.霉变的饼干 D.空易拉罐 E.生锈铁钉
(1)你应该放人“可回收垃圾箱”的是____________________________________.
(2)请你写一句劝告其他年级同学节约资源,保持环境的话语。
________________________________________________________________________.
27.(3分)国家环保总局已将各类实验室纳入环保监管范围,某班同学进行“碱和盐的性质"实验,使用的试剂有:石灰水、盐酸、氢氧化钠溶液、碳酸钠溶液和无色酚酞试液等,实验后将废液集中到废液缸中,测得废液的pH=2,回答下列问题:
(1)由此可知该废液呈_________(填“酸性”、“碱性”或“中性”).
(2)实验室的废液未经处理直接排放会污染环境,从原料的成本来考虑.你对该废液的最佳处理方法是:__________________,发生反应的化学方程式是__________________.
28.(8分)A、B、C、D、E、F六种物质都是初中化学中涉及的化合物,它们之间的转化关系如下图所示,其中D是最常见的溶剂,回答下列问题:
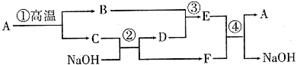
(1)根据上图推断,A是(填写化学式,下同)_________,D是_________,E是_________。
(2)写出下列反应的化学方程式:
①_________________________________②_________________________________
④_________________________________
反府①属于________反应,④属于________反应(填写基本反应类型).
29.(2分)将质量相等的A、B两块金属,分别放人溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系如下图所示(产物A、B两种元素的化合价相同),分析下图,填空(“>”或“<”)
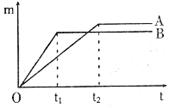
(1)金属活动性A________B.
(2)相对原子质量A________B.
四、我要探究(24分)
30.(5分)小明家住在山清水秀的山脚下,几年前,村里为了发展经济,在村边建起一座氮肥厂。近段时间,小明发现村里的井水,在烧水或用碱性洗衣粉洗衣服时,总闻到水里散发出一股与氮肥厂附近相似的刺激性气味。
【提出猜想】联想到所学的化学知识,小明猜想可能是氮肥厂排出的废水污染了井水。他猜想的依据是________________________________。
【表达交流】请你根据上述信息帮助小明归纳污染物的化学性质:
(1)________________________________;(2)________________________________。
【设计实验】为了验证猜想,小明设计了如下实验方案:
(1)从氮肥厂取来氮肥作为样品。
(2)取适量样品放人玻璃杯中,加入井水充分溶解。将所得溶液分为2份。
(3)一份加入碱性洗衣粉,搅拌后闻气味;另一份加热后闻气味。
【反思评价】小明的实验方案存在着问题,你认为应怎样改进?
________________________________________________________________
【获得结论】小明通过改进后的实验,确认是氮肥厂排出的废水污染了井水。
【探究启示】目前该村村民还需饮用井水,请你提出一条简便的处理方法:
________________________________________________________________
31.(8分)下图是实验室制取气体的发生装置图,请根据此装置图回答下列问题:
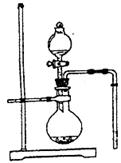
(1)利用图中装置,你能够制备的常见气体有哪几种?
(2)请写出你所能制取气体的相应化学方程式。
(3)说出能用此装置制取上述气体的简单理由。
32.(11分)小东家有一件久置的铜器件,其表面有大量“铜绿"。小东找来同伴一起探究它的成分,他们向一支试管中加入少量刮下的“铜绿”粉末,格下图所示实验装置来探究它的成分,回答下列问题。
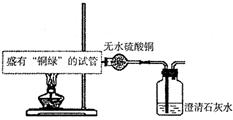
查阅资料知:无水CuSO4是白色粉末,遇水会变成蓝色;碳粉是黑色粉末,通常情况下不与酸、碱反应。
(1)固定放有“铜绿"的试管时试管口应________________________________。
(2)将铜绿分解的产物依次通过无水硫酸铜、澄清石灰水时,他们看到无水硫酸铜粉末变为蓝色,说明“铜绿”中含________元素;澄清石灰水变浑浊,说明“铜绿”中含________元素。
(3)待完全反应后,发现试管中剩下部分黑色粉末。针对黑色粉末,他们提出了如下猜想:
①黑色粉末是氧化铜
②你把他们提出的另一种猜想写出来________________________________。
请你设计简单的实验,证明他们的猜想可能是正确的。
猜想
简要实验方案
现象
结论
①
②
(4)根据“铜绿”的分解产物,请你推测,铜发生锈蚀的原因可能是铜和空气中的(填化学式)________________________反应生成。
五、我会计算
33.(4分)向盛有
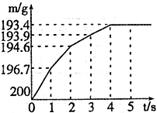
2NaHCO3+H2SO4==Na2SO4+2H2O+2CO2↑
试回答下列问题:
(1)当碳酸氢钠与硫酸溶液恰好完全反应时,所需时间为___________。
(2)当碳酸氢钠与硫酸溶液恰好完全反应时,所产生的二氧化碳的质量为________。
(3)反应后,生成硫酸钠质量是_____________。
34.(6分)我国化工专家侯德榜的“侯氏制碱法"为世界制碱工业做出了突出的贡献。工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质。现称取只含氯化钠杂质的纯碱样品
(1)该纯碱样品的纯度(计算结果精确到0.1%);
(2)所得溶液中溶质的质量分数。