2008-2009学年度淄博市张店第一学期初四期末学业水平测试
化学试卷
说明:1.试卷满分50分。考试时间理、化共120分钟。考生不准使用计算器。
2.相对原子质量:H:1 C:12 N:14 O:16 Na:32 Cl:35.5 Ca:40
一、选择题(本题包括15小题,每小题1分,共15分。每小题只有一个选项符合题意)
1.材料是时代进步的重要标志,复合材料是新型材料研制的重要发展方向。以下属于复合材料的是
A.玻璃钢 B.普通玻璃 C.合金 D.塑料
2.一些食物的近似pH如下:牛奶6.3~6.6;鸡蛋清7.6~8.0;柠檬2.2~2.4;番茄4.0~4.4。其中酸性最强的是
A.牛奶 B.鸡蛋清 C.柠檬 D.番茄
3.生铁和足量的稀盐酸充分反应后,总会留有残渣,残渣的主要成分是
A.铁 B.碳和少量杂质 C.氯化亚铁 D.三氯化铁
4.下列物质长期露置于空气中,因发生化学变化而使溶液质量减少的是
A.浓硫酸 B.浓盐酸 C.石灰水 D.氯化钠溶液
5.下图所示实验操作不正确的是
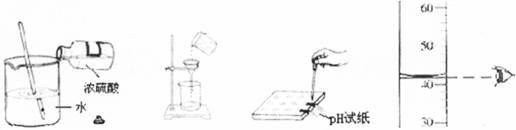
A.稀释浓硫酸 B.过滤 C.测pH D.读取液体体积
6.下列实际应用中,利用中和反应原理的是
①用生石灰作食品干燥剂 ②用熟石灰和硫酸铜配制波尔多液
③施用熟石灰改良酸性土壤 ④用氢氧化钠溶液处理泄漏的浓硫酸
A.①② B.③④ C.①④ D.②③
7.化学时刻影响着我们的生活,它在工农业生产和日常生活中起到了非常重要的作用。下列说法中正确的是
A.微量元素在人体内的需求量很小,不需要从外界摄取
B.纤维素无法被人体吸收,所以食物中的纤维素对人体毫无意义
C.草木灰是一种碱性肥料,主要成分是K2CO3,但不能与氮肥混合使用
D.海水晒盐是应用氯化钠的溶解度随温度的升高而增大的原理
8.用一种试剂一次就能将澄清石灰水、氢氧化钠溶液、稀盐酸三种无色溶液区别开的是
A.无色酚酞试液 B.二氧化碳气体 C.氯化钡溶液 D.碳酸钠溶液
9.人体所摄入的主要物质有:①蛋白质②糖类③油脂④维生素⑤无机盐⑥水⑦空气等。其中属于有机化合物的是
A.①②③④ B.①②⑤⑥ C.②⑤⑥⑦ D.③④⑥⑦
10.下列各种情况中,埋在地下的铸铁管道腐蚀速率最慢的是
A.在潮湿、疏松、透气的中性土壤中 B.在潮湿、疏松、透气的酸性土壤中
C.在干燥、致密、不透气的中性土壤中 D.在沿海潮湿的土壤中
11.下列物质间的转化只有加入酸才能一步实现的是
A.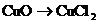 B.
B.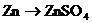
C.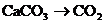 D.
D.
12.下列化学反应中,属于置换反应的是
A.
B.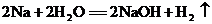
C.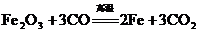
D.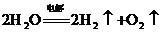
13.除去下列物质中所含杂质(括号内为杂质),所选用试剂及操作方法均正确的一组是
选项
待提纯的物质
选用的试剂
操作方法
A
NaOH(Na2CO3)
氯化钙溶液
溶解、过滤、结晶
B
CaO(CaCO3)
水
溶解、过滤
C
Cu(CuO)
稀盐酸
溶解、过滤、洗涤、干燥
D
CuSO4(H2SO4)
氢氧化钠溶液
过滤
14.现有一杯
A.加入一定量的硝酸钾 B.恒温蒸发部分水
C.升温到60℃ D.加入一定量的水
15.下列图像中不能正确反映对应的变化关系的是
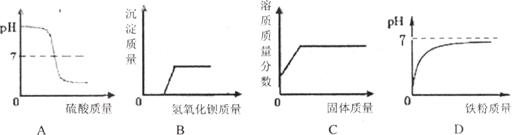
A.向一定量的氢氧化钠溶液中滴加稀硫酸至过量
B.向一定量的硫酸和硫酸镁混合溶液中滴加氢氧化钡溶液
C.在一定温度下,向不饱和的硝酸钠溶液中不断加入硝酸钠固体,充分搅拌
D.向一定量的稀盐酸中加入铁粉,充分反应
二、理解与应用(本题包括5小题,共16分)
16.(2分)现有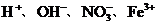 四种离子,请写出它们可能组成的酸、碱、盐、氧化物的化学式,填在相应的位置。
四种离子,请写出它们可能组成的酸、碱、盐、氧化物的化学式,填在相应的位置。
酸___________、碱___________、盐___________、氧化物___________。
17.(2分)在“浓硫酸、氯化钠、大理石、高锰酸钾、钛合金”中选用适当的物质填空。
(1)可用作调味品的是___________; (2)可用作某些气体干燥剂的是__________;
(3)可用来制造人造骨的是_________;(4)用作建筑材料的是___________。
18.(4分)下图是甲、乙两种固体物质的溶解度曲线,试回答下列相关问题。

(1)t
(2)t
(3)t
(4)若要从甲中含有少量乙的混合溶液中提纯甲,可采用的方法是______________。
19.(4分)某校“绿色”环保小组的同学用精密酸度计测得实验室中甲、乙、丙、丁四种废液的pH如下表。现请你和他们一起实验并回答:
废液
酸碱度
甲
乙
丙
丁
pH
6.5
11.3
7
2.0
(1)各取溶液少许,分别滴入1~2滴无色酚酞试液,能使酚酞试液变红的废液是_____。
(2)实验老师告知:乙、丁分别是未用完的氢氧化钾溶液和稀硝酸。为了防止废液对环境的污染,小聪将丁溶液逐滴滴入乙中,刚好完全反应,此时溶液的pH_______7(填“<”、“>”、“=”)。该反应的化学方程式为:______________________。小明说:“反应后所得溶液中的溶质还是农作物生长所需的肥料呢!”请问,该肥料属于___________(填“氮肥”、“磷肥”、“钾肥”、“复合肥”)。
20.(4分)广泛应用于航空、航天方面的金属镁是从海水中提取出来的。主要生产流程如下图所示。

(1)石灰乳是熟石灰和水的混合物,对_________有腐蚀作用,使用时应注意安全。
(2)步骤③的化学方程式为____________________________________。
(3)小红在实验室模拟该生产流程,为了使现象明显、操作更加简便,她用(填物质名称)_________溶液代替石灰乳进行实验。步骤④中需要加过量的该物质,如果只使用本题中出现的药品,检验该物质是否加过量的方法是__________________。
三、实验与探究(本题包括3小题,共13分)
21.(3分)九年级九班的学习小组,正在设计实验证明Fe、Cu、Ag三种金属的活动性强弱。他们提出了许多设计方案,小虎设计了这样两种方案:
(1)将三种金属分别加入稀盐酸,观察有无气泡产生:再将铜丝插入硝酸银溶液中,观察现象。
(2)将铁丝插入硫酸铜溶液中,将铜丝插入硝酸银溶液中,观察现象。请回答:你认为利用这两种方案能否得到正确的结论?_________。请写出实验(2)中发生反应的其中一个化学方程式:____________________________________;你设计的简单实验方案是:___________________________________________________。
22.(4分)某固体可能由Na2SO4、NaCl、Na2CO3、KNO3中的一种或几种组成,现进行如下实验:
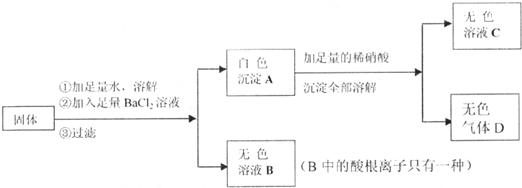
试回答:
(1)白色沉淀A的化学式为_________;
(2)原固体中一定含有_________,一定不含有_________,可能含有_________。
23.(6分)自
A.这项措施能达到节能减排的目的
B.塑料购物袋是造成“白色污染”的来源之一
C.塑料购物袋是由合成材料制成的
D.为防止污染,可以将塑料购物袋直接烧掉
(1)新规定实行后预计塑料袋的使用量将减少2/3,但是其危害作用并没有根本解决,为尽量减少其危害,请你提出一条合理化建议___________________________。
(2)日常生活中使用的塑料袋有两种,一种是用聚乙烯【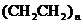 】制成的,可用于盛装食品;另一种是用聚氯乙烯【
】制成的,可用于盛装食品;另一种是用聚氯乙烯【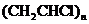 】制成的。聚氯乙稀燃烧的化学方程式是:
】制成的。聚氯乙稀燃烧的化学方程式是: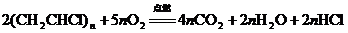 。
。
①通过点燃的方法可以鉴别聚乙烯和聚氯乙烯。如果塑料点燃时有强烈的刺激性气味,这种塑料可能是由__________________制成的。
②某同学设计了如下图所示实验来验证塑料燃烧的产物。
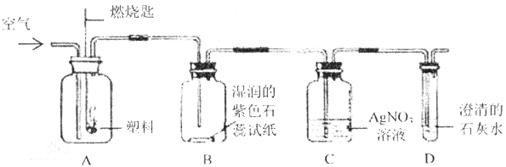
若A瓶燃烧的是聚氯乙烯塑料,在B瓶中可以看到的现象是___________,C、D两瓶中发生反应的化学方程式为__________________、__________________。
四、分析与计算(本题包括1小题,共6分)
24.(6分)长期使用的热水壶底部有一层水垢,主要成份是碳酸钙和氢氧化镁,用稀盐酸可以清除水垢。某学校化学研究性学习小组的同学通过实验测定水垢中碳酸钙的含量:将过量的稀盐酸加入到
时间/s
0
30
60
90
120
150
180
增加的质量/g
0
30
50
60
66
66
66
试回答下列问题:
(1)请在下边的坐标纸上,以反应时间为横坐标,以产生CO2气体的质量为纵坐标,画出能够表明产生气体的质量随反应时间变化规律的关系曲线。
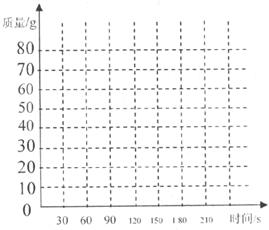
(2)从表中可以看出,
(3)计算水垢中碳酸钙的质量分数。