2008-2009学年度肥城市第一学期九年级期末质量检测
化学试卷
相对原子质量:H l N l4 O16 Na 23 S 32
一、选择题(本题包括l0小题.每小题只有一个选项符合题意,请将符合题意的选项序号填入下面相应的空格内)。
1.学习了化学使我们对商品的标签和标识有了更深层次的认识,以下四枚标识使用不恰当的是
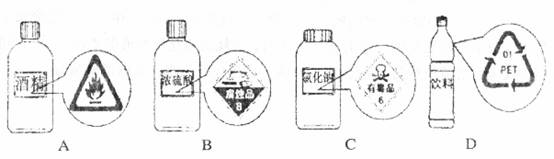
2.2008年北京奥运会提出了要突出"绿色奥运、科技奥运、人文奥运"的理念,其中"绿色奥运"指的是
A.把环境保护作为奥运设施规划和建设的首要条件
B.运动员的食品全部是未加任何添加剂的食品
C.奥运场馆建设均使用天然材料建造,不使用人工合成材料
D.所有奥运用品全部是绿色的
3.下列叙述中,正确的是
A.原子是构成物质的最小粒子
B.不同元素的原子的核电荷数一定不同
C.核外电子排布相同的粒子一定属于同种元素
D.二氧化碳分子是由一个碳原子和一个氧分子构成的
4.下列厨房常用的物质与水混合,不能形成溶液的是
A.食盐 B.植物油 C.白糖 D.白酒
5.第39个"世界地球日"的主题是"认识地球,和谐发展"。"防止污染、优化生态环境、与大自然和谐相处",应从身边小事做起。在下面①~⑥项中,你认为与其不相符的是
①随意丢弃废旧电池②吃完的口香糖随地吐掉③每年参加植树活动
④尽量使用手帕,减少餐巾纸的使用 ⑤将生活垃圾分类放入路两侧的垃圾桶内
⑥生活污水倒入县城内道路两侧的绿化带内
A.只有①②⑥ B.只有②③④ C.只有①⑤ D.只有①②
6.下列实验方案中,能达到预期目的的是
A.用NaOH溶液除去CO2中混有的HCl气体
B.用点燃的方法除去N2中混有的少量H2
C.用BaCl2溶液除去KNO3溶液中混有的少量K2SO4,得到纯净的KNO3溶液
D.用稀盐酸除去热水瓶胆壁上的水垢(主要成分是碳酸钙和氢氧化镁)
7.在配制一定溶质质量分数的氯化钠溶液时,下列出现的操作失误,会引起所配溶液的溶质质量分数降低的是
A.用托盘天平称量氯化钠时,将砝码放左盘,但未使用游码
B.用量筒量取蒸馏水读数时,仰视凹液面最低处
C.将量筒中的水倒人烧杯时,有水洒出
D.将配好的氯化钠溶液转移到细口瓶中时,不慎洒出部分溶液点燃
8.根据质量守恒定律判断:X+3O2=2CO2+3H2O中,X的化学式为
A.CH3OH B.CH3COOH C.C2H5OH D.CH4
9.下列说法中,正确的是
A.盐酸能使紫色石蕊试液变蓝
B.浓硫酸露置于空气中,溶质的质量分数变大
C.打开盛浓盐酸的试剂瓶,瓶口会产生白雾
D.露置于空气中的固体氢氧化钠,其成分不会发生变化
10.下列做法中合理的是
A.油锅着火时,可以用水浇灭
B.少量氢氧化钠溶液滴在桌上.应立即用湿抹布擦净
C.较多的浓硫酸溅到皮肤上,应迅速用水冲洗,然后再做其他处理
D.酒精灯使用过程中要添加酒精,灯焰可以不熄灭,但一定要用漏斗
二、(本题包括6小题)
11.化学与我们的生活密切相关,日常生活中的化学知识有很多。请你填写生活中常用的下列物质所含的化学成分(填化学式):
(1)干冰常用于人工降雨,干冰是指____________;
(2)天然气是常用的气体燃料,天然气是指___________;
(3)被称为理想的"绿色能源"的是__________。
12.2008年春节期间,我国南方大部分地区都受到冰雪的袭击,请你用所学的化学知识结合生活经验回答下列事例中的有关问题:
(1)在这次冰雪灾难中,属于化学变化的是___________(填序号)。
A.房屋倒塌 B.树木折断 C.冰雪融化 D.铁轨生锈
(2)小明建议向积雪上撒入食盐,目的是________ (选填"升高"或"降低")凝固点,使积雪更快融化。
13.已知,在水溶液中,乙醇(C2H5OH)不发生电离;溴化氢(HBr)电离产生氢离子(H+)和溴离子(Br-);氢氧化钠电离产生钠离子和氢氧根离子。请回答下列问题:
(1)根据这三种溶液的组成推断,医用酒精(含乙醇75%的水溶液)显_______性,溴化氢的水溶液显________性。
(2)写出上述物质之间发生中和反应的化学方程式____________________________。
(3)氢氧化钠溶液中存在的微粒有(用化学符号表示)____________________________。
14.某农场附近新建了一座燃煤火力发电厂后该农场的小麦产量急剧下降。经农场技术员测定:雨水pH约为4、土壤pH约为5。已知一些重要作物最适宜生长的土壤的PH如下表:
作物
①水稻
②小麦
③玉米
④油菜
⑤马铃薯
pH
6~7
6.3~7.5
6~7
6~7
4.8~5.5
(1)根据上表数据,你认为这种土壤最适合种植的作物是(填编号)_____________。
(2)若继续种小麦,你认为最好选用以下(填编号)__________试剂来改良土壤。
①工业盐酸 ②熟石灰 ③纯碱
(3)该地区形成酸雨的主要原因是_________________________________________。
15.为了防止灾后疫情的发生,灾区需要进行多次反复的消毒。其中二氧化氯消毒粉作为新一代高级消毒粉有很多的优点,二氧化氯消毒可以杀灭各种致病性大肠菌群、球菌、军团菌、真菌、芽孢等,适用于食品加工厂、制药厂、饮用水厂等环境要求较高的企业化工厂,二氧化氯作为消毒剂后不会对环境造成进一步的影响,请回答下列问题:
(1)二氧化氯的化学式为______________________;
(2)二氧化氯中氯元素的化合价为_________________________;
(3)二氧化氯所属物质的类别是_____________________。
16.图甲是两种元素在周期表中的信息,图乙是氟原子的原子结构示意图。请完成下列问题:

(1)图甲方框的横线上填的是________,图乙方框横线上的数字是_______________;
(2)图甲所示两种元素形成化合物的化学式是______________________________
三、本题包括2小题
17."即食即热"型快餐适合外出旅行使用。小新和小意对它的原理产生浓厚的兴趣,于是进行了如下探究:
【初步探究】小新和小意发现:快餐内层用铝箔包裹,外层是分开包装的两包化学物质。使用时拉动拉线,使这两种物质接触,便可对食物进行加热。打开来看:一包是无色液体,一包是白色粉末。小意作出如下猜想:
猜想①:这两包物质分别是生石灰和水
猜想②:这两包物质分别是熟石灰和水
【查阅资料】常温下,可用铝罐车运输浓硫酸。
【实 验】根据下图进行实验,观察发生的现象,完成下表。

化学物质
生石灰和水
熟石灰和水
现象
温度计内液柱______________________
温度计内液柱升幅小
解释
(1)___________________
(2)___________________
小新建议把这两包物质换成浓硫酸和水。他的建议合理吗? (填"合理"或"不合理").原因是__________________________________________________.
18.为了研究 的性质,需要制取并收集
的性质,需要制取并收集 气体。以下是老师提供的一些实验装置。
气体。以下是老师提供的一些实验装置。

(1)制取并收集 气体,可采用的装置组合是____(填字母,下同),检验集气瓶中
气体,可采用的装置组合是____(填字母,下同),检验集气瓶中 是否收集满的方法是______,若在该实验中气体无法收集满,可能的原因是_____________。
是否收集满的方法是______,若在该实验中气体无法收集满,可能的原因是_____________。
(2)实验室制取 的化学方程式___________________________________________。
的化学方程式___________________________________________。
(3)实验室用过氧化氢制取并收集氧气,可采用的装置组合是____________________。
四、(本题包括2小题)
19.合作学习小组的同学看了硝酸铵产品包装袋上的说明(如下图),对产品的含氮量产生了疑问,于是运用所学的知识对硝酸铵的含氮量进行了计算,都认为包装袋上标注的含氮量不准确。小组中李华同学的计算过程如下: ,而王明同学计算的结果大于34%。由于计算结果不同,小组中的同学进行了讨论。
,而王明同学计算的结果大于34%。由于计算结果不同,小组中的同学进行了讨论。

(1)你认为李华同学的计算是(填对或错):__________________________________;
(2)计算硝酸铵中的含氮量,你的方法是:________________________________________
20.节约资源和保护环境已经成为我们的基本国策。我市环保部门对某工厂的废水进行抽样分析,结果表明废水中含少量硫酸。取一定量废水用质量分数为2%的氢氧化钠溶液中和(已知废水中的其它成分不与氢氧化钠反应),至pH=7时,消耗氢氧化钠溶液的质量为