2007-2008学年度泰州海陵区公办初中第一学期九年级期末考试
化学试卷
(满分100分,时间90分钟)
说明:
1.本试卷分第一部分选择题和第二部分非选择题。
2.可能用到的相对原子质量:H:
第一部分 选择题(共40分)
一、(本题包括15小题,每小题2分,共30分。每小题只有一个选项符合题意,请将答案填在对应的空格内。)
1.下列我国古代的发明中不属于化学工艺的是
A.钢铁的冶炼 B.火药的发明
C.瓷器的烧制 D.指南针的发明
2.旅游资源开发要讲究人与自然的和谐发展。关于达到将传统旅游向生态旅游转化,使之成为可持续发展的经济增长点的目的,下列建议和认识不合理的是
A.开发和生产无汞电池
B.将收集的一次性发泡塑料餐具倒入长江,以减轻污染
C.开发、保护旅游资源,人人有责
D.要求旅客将垃圾分类放置
3.下列社会问题与化学有关的是
①无氟冰箱与臭氧层空洞 ②二氧化碳排放与温室效应
③酸雨的形成、危害与防治 ④一次性塑料袋与“白色污染”
A.①③④ B.①②④ C.①②③④ D.①②③
4.欲用托盘天平称取
A.添加适量药品 B.取出适当药品
C.将游码向左边移动 D.将右边的调节螺丝向左边移动
5.小明发现罩在蜡烛火焰上方的烧杯内壁被熏黑。他的下列做法不正确的是
A.反复实验并观察是否有相同的现象
B.认为与本次实验无关,不予理睬
C.查找蜡烛成分资料,探究黑色物质
D.向老师请教生成黑色物质的原因
6.前中国国民党主席连战先生在参观陕西秦始皇兵马俑博物馆时,秦俑馆向他赠送了一块弥足珍贵的“秦土”。它取自秦始皇兵马俑考古现场的坑道遗址。下列关于“秦土”的说法正确的是
A.是纯净物 B.是混合物
C.不含任何化学物质 D.用“秦土”烧制兵马俑时只发生物理变化
7.小科用如图装置来测定空气中氧气的含量,对该实验认识正确的是
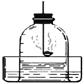
A.使用红磷的量多或量少,都不会影响实验结果
B.燃烧足够的红磷才可使进入容器的水占容器的4/5
C.红磷燃烧消耗空气中的氧气,使容器内压强减小水面上升
D.红磷燃烧结束,要立即观察,并记录水进入容器的刻度
8.抗氧化剂能吸收氧气降低食品内部及周围的含氧量,阻止氧气和食品发生氧化反应,从而延长食品的保质期。一些食品的包装盒内常印有“抗氧化剂”的小包,内盛灰黑色的粉末,该灰黑色的粉末可能是
A.铁粉 B.氧化铜 C.铜粉 D.氧化镁
9.在盛有5mL 5%过氧化氢溶液的试管中,加入少量的二氧化锰,反应结束后,下列三项:①过氧化氢的质量 ②水的质量 ③二氧化锰的质量,与反应前相比,其中发生变化的是
A.仅① B.仅② C.仅①和② D.①②③
10.水蒸气通过炽热的炭层时,发生反应:C+H2O H2+CO,该反应类型属于
H2+CO,该反应类型属于
A.置换反应 B.分解反应 C.化合反应 D.复分解反应
11.军事上有一种“非致命武器”叫“芬太奴”,是一种强有力的麻醉剂,曾被用作解救人质,其化学式为C20H24N2O,下列关于芬太奴的说法中正确的是
A.芬太奴由20个碳元素、24个氢元素、2个氮元素和1个氧元素构成
B.芬太奴由20个碳原子、24个氢原子、2个氮原子和1个氧原子构成
C.芬太奴由液体变成气体时,分子本身没有改变,但是分子间隔变大
D.芬太奴中碳、氢、氧、氮四种元素的质量比为20┱24┱2┱1
12.已知8.4gA与一定量B恰好反应生成11.2gC和13.2gD,则A与B反应的质量比为
A.3┱1 B.21┱
13.将过量铁粉投入硫酸铜和稀硫酸的混合溶液中,充分反应后过滤,滤液中含有
A.硫酸铁 B.硫酸铜 C.硫酸 D.硫酸亚铁
14.一般说来,大多数作物适宜在中性或接近中性的土壤中生长。经测定某土壤的pH为5.5,要改良它,应在土壤中施加适量的
A.熟石灰 B.稀硫酸 C.烧碱 D.食盐
15.下列各组物质,只用水就可以鉴别的是
A.固体:氯化钠、碳酸钙、高锰酸钾
B.气体:氢气、氧气、二氧化碳
C.液体:豆油、酒精、菜油
D.固体:氯化钠、氯化钙、氯化镁
二、(本题包括5小题,每小题2分,共10分。每小题有一个或两个选项符合题意,请将答案填在对应的空格内。)
16.下列物质中有一种与其他三种物质都能发生反应,这一种物质是
A.铁 B.稀盐酸 C.碳酸钙 D.氢氧化钠
17.用括号中的试剂或方法除去下列物质中所含杂质,所用药品错误的是
A.NaOH溶液中混有Na2CO3(稀硫酸)
B.NaCl溶液中混有Na2SO4(BaCl2溶液)
C.CO2中混有CO(点燃)
D.Cu中混有Fe(稀硫酸)
18.推理是学习化学常用的思维方法。以下四个推断中正确的是
A.燃烧一般都伴随发光、放热现象,所以有发光、放热的现象就是燃烧
B.氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物
C.酸与碱反应生成盐和水,所以生成盐和水的反应一定是酸与碱的反应
D.在加压的情况下,可将石油气液化装入钢瓶中,由此可知分子之间有间隔
19.向含有AgNO3、Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气体生成,则滤出的固体一定为
A.Ag、Cu两种单质的混合物
B.Cu、Fe两种单质的混合物
C.Ag、Fe两种单质的混合物
D.Ag、Cu、Fe三种单质的混合物
20.下列各组物质,无需另加试剂,只需利用组内溶液本身或相互混合,就能鉴别出来的是
A.K2SO4 BaCl2 NaNO3 NaCl
B.HCl Na2CO3 BaCl2 Na2SO4
C.KOH Na2SO4 CuSO4 MgCl2
D.KCl AgNO3 KNO3 NaCl
第二部分 非选择题(共60分)
三、(本题包括6小题,共37分)
21.(6分)用化学用语表示:
⑴两个氢原子 ⑵三个水分子
⑶五个亚铁离子 ⑷人体中含量最多的元素
⑸五氧化二磷中磷元素显+5价 ⑹氩气
22.(6分)从H、C、O、Na、Cl、N六种元素中,选择适当的元素填写符合下列要求的化学式(每空只需各写一个符合题意的化学式)
⑴充入食品包装袋中可防腐的单质是
⑵家中厨房常用的调味品是
⑶溶于水后溶液呈碱性的气体是
⑷溶于水使溶液温度升高的固体是
⑸含有四种元素的化合物是
⑹能与人体血红蛋白结合使人中毒的是
23.(8分)用化学方程式或电离方程式表示下列问题的原因:
⑴铝具有良好的抗腐蚀性能,是因为它能与空气中的氧气反应产生致密的氧化膜
⑵氢氧化钠露置在空气中会变质,是因为它能吸收空气中的二氧化碳
⑶食品包装袋内常用生石灰作干燥剂,是因为它能吸收空气中的水分
⑷电解水时,在水中加入的稀硫酸能够增强水的导电性,是因为它能电离出自由移动的离子
24.(6分)甲、乙、丙三种物质的溶解度曲线如下图所示。据图回答:
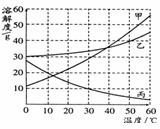
⑴
⑵
⑶要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是 。
⑷
⑸
25.(5分)第29届夏季奥运会将于今年8月8日在我国首都北京举行,“人文奥运、科技奥运、绿色奥运”是本届奥运会的主题之一。请回答下列有关问题:
⑴奥运会的场馆建设中,外墙将大量采用新型塑料膜材料ETFE(ETFE的化学名称为:聚氟乙烯,它是由氟乙烯聚合而成的,氟乙烯的化学式为:C2H
⑵有人建议使用大型遥控飞艇(类似气球)作宣传工具以渲染奥运气氛。
①为了使飞艇在空气中飞行安全而有效,你认为飞艇中填充的气体应具备下列性质中的 (填序号)。
A.密度比空气小 B.密度比空气大 C.化学性质稳定 D.具有可燃性
②根据上述选择的性质,你认为飞艇内最好填充的气体是 (填序号)。
A.氢气 B.氦气 C.氮气 D.二氧化碳
26.(6分)某固体可能由Na2SO4、NaCl、Na2CO3、KNO3中的一种或几种组成,现进行如下实验:
①向固体中加足量的水进行溶解;
②加入足量的BaCl2溶液;
③过滤后得到白色沉淀A和无色溶液B(B中的酸根离子只有一种);
④向白色沉淀A中加入足量的稀硝酸,沉淀全部溶解,并得到无色溶液C和无色气体D
⑴白色沉淀A的化学式为 ,无色气体D的化学式为 。
⑵原固体中一定含有 ,一定不含有 ,可能含有 。
⑶为检验上述可能含有的物质是否一定存在,小魏同学又设计了如下实验方案:
①取少量固体溶于水,加入足量的Ba(NO3)2溶液,充分反应后,过滤。
②取少量滤液滴加AgNO3溶液,观察有无白色沉淀生成,由此得出结论。
在小魏同学设计的实验方案①中,加入足量的Ba(NO3)2溶液的目的是
。
四、(本题包括2小题,共17分。)
27.(10分)请根据下图所示的实验装置图填空。
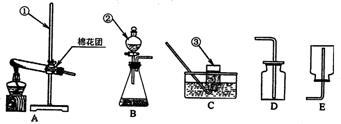
(1)指出图中标有数字的仪器的名称:① ,② ,③ 。
(2)在实验室用高锰酸钾制氧气时,试管口的棉花团的作用是 ,写出反应的化学方程式: 。
(3)当用B装置制取氧气时,仪器②内盛放的液体是 ,仪器②的作用是 。
(4)在实验室制二氧化碳可选用 装置,收集二氧化碳可选用 装置,写出实验室制取二氧化碳的化学方程式: 。
28.(7分)学校实验室的废液缸中收集了学生在实验室制取CO2后残留的废液。小红同学想探究废液中溶质的成分,请你一同参与探究并回答下列问题:
【提出问题】废液中的溶质是什么?
【做出猜想】小红认为废液中的溶质只有CaCl2 。
你认为还可能含有的溶质是 (填化学式)。
【查阅资料】CaCl2溶液呈中性。
【实验与结论】①小红取少量CaCl2溶液和废液分别加入到两支试管中,并向其中分别滴加无色酚酞试液做对比实验,结果两试管中溶液均无色,于是小红认为自己的猜想是正确的。
②你认为小红的实验 (填“能”或“不能”)证明她的猜想,理由是 。
③如果要证明你的猜想是正确的,你选择的试剂是 ,实验中可能看到的现象是 。
【拓展与应用】①若实验证明你的猜想是正确的,想要处理废液只得到CaCl2溶液,应向废液中加入过量的 ,反应完成后过滤。
②通过以上探究,你认为实验室的废液未经处理直接倒入下水道,可能造成的危害是 (只需要写一条)。
五、(本题包括1小题,共6分。)
29.(6分)某化学兴趣小组用化学方法测定一种钢样品中铁的含量。同学们称取了
反应时间 / min
4
8
12
烧杯和药品总质量 /g
125.6
125.5
125.5
⑴反应中产生氢气 ,这种钢样品中铁的质量分数为 。(请写出计算过程)
⑵钢的类型分为:低碳钢,其含碳量为0.03%~0.3%;中碳钢,其含碳量为0.3%~0.6%;高碳钢,其含碳量为0.6%~2%。假设残留在烧杯中的黑色固体全部是炭,则这种钢属于 。
⑶有同学提出:灼烧可使钢中的炭变为二氧化碳挥发掉,灼烧后钢样品质量会减轻。可是他们将一定量的钢样品灼烧后,发现质量反而增加了许多。其原因是 。