2007-2008学年度安徽省淮北市西园中学九年级第四次月考
化学试卷
可能用到的相对原子质量:H―l Li―
AI―27 Zn―65 Fe一56 S一32 Na一23 Mg―24
一、选择(单选题 每小题2分,共20分)
1、下列叙述中,正确的是
A、含钙40%的碳酸钙是混合物 B、化学变化中一定有物理变化
C、氢氧化钠潮解是化学变化 D、不饱和溶液一定比饱和溶液稀
2.铁酸钠(Na2FeO4)是净水处理过程中使用的一种新型净水剂,铁酸钠中铁元素的化合价是
A.+6
B.+
3.配制溶质质量分数一定的氯化钠溶液的一些操作步骤如下图。正确的操作顺序是
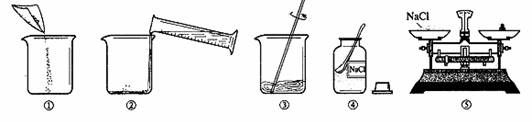
A.④⑤①②③ B.①②③④⑤ C.③④①②⑤ D.②①④③⑤
4.将ag20%的NaOH溶液与ag20%的盐酸溶液混合后,滴入紫色石蕊试液,溶液呈
A.紫色 B.蓝色 C.红色 D.无色
5、只用一种试剂,一次性验证铜、铁、银三种金属的活动性强弱,该试剂是
A、CuSO4溶液 B、FeSO4溶液 C、AgNO3溶液 D、稀盐酸
6、下列溶液中能分别跟盐酸、二氧化碳、氯化铜溶液反应,并产生不同现象的是
A.H2SO4 B.NaOH C.KOH D.Ba(OH)2
7.把足量的镁粉和铜粉的混合物分别加入下列各组物质的溶液中,充分反应后过滤,溶液中只有一种溶质的是
A.HgCl2、Hg(NO3)2 B.H2SO4、FeSO4
C.HCl、H2SO4 D.Na2SO4、CuCl2
8、人口腔内唾液的PH值在进食过程中和进食后会发生变化。一般来说从进食开始至10分钟,酸性逐渐增强,10分钟至40分钟酸性逐渐减弱并趋于正常。与上述事实符合的函数图象是

9、等质量的镁、锌、铁三种金属分别跟相同质量、相同质量分数的足量稀硫酸反应,能够正确反映时间(t)和产生氢气质量(m)关系的曲线是
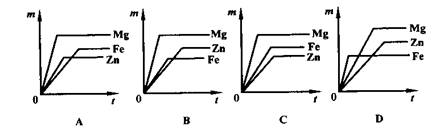
10、以下验证“盐酸中哪种粒子使紫色石蕊试液变红色”的实验设计不合理的是
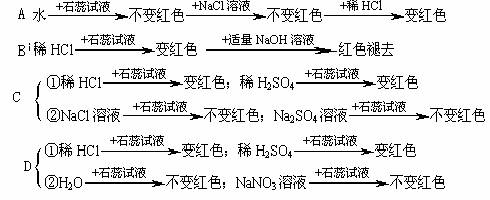
二、填空(6小题,共35分)
11、(5分)将“元素、原子、分子、离子、质子、中子、电子”填入下列空格内。
(1)化学变化中的最小粒子是
(2)氢气 是保持氢气化学性质的最小粒子
(3)Na与Na+属于同―种
(4)铁原子核内含有26个质子和30个
(5)在离子化合物中,元素化合价的为+1,表示1个的原子失1个
12、(4分)欲采用化学方法除去下表中第I栏内4种物质中的少量杂质(括号内为杂质),请分别从第II、第Ⅲ栏内选取合理选项的字母,填在对应的答案栏内。
Ⅰ.物质
Ⅱ.除杂试剂及操作
Ⅲ.反应类型
答案
①CuO固体(C)
A.高温 a.复分解反应
B.铜网、加热 b.分解反应
C.盐酸、蒸发 c.化合反应
D.氧气、加热 d.置换反应
⑴
②NaCl固体(Na2CO3)
⑵
③N2(O2)
⑶
④CaO固体(CaCO3)
⑷
13. (4分)下列有三种制取硝酸铜的方案:
方案一:Cu+4HNO3(浓) = Cu(NO3)2 + 2NO2↑+ 2H2O
方案二:3Cu+8HNO3(稀) = 3Cu(NO3)2 + 2 NO↑+ 4H2O
方案三:2Cu+O2+4HNO3(稀) = 2Cu(NO3)2+ 2H2O
请你从经济、环保的角度分析考虑选择一种最适宜的方案 ,你选择该方案而不选其它方案的理由是(写两点): _________ ; 。
14.同学们在物理学习中知道金属材料的电阻大小与材质、长度、横截面积、温度有关。在化学学习过程中,含有自由移动离子的溶液也能导电。请你猜想:溶液导电性能的强弱可能有哪些因素有关呢?(至少写出两条,多写一条[答案合理]得2分,最多加4分,试卷满分不超过60分)
(1)
(2)
(3)
(4)
(5)
15. (6分))根据下表所列部分物质在水中的溶解性(
阴离子
阳离子
OH-
NO3-
Cl-
SO42-
CO32-
Na+
溶
溶
溶
溶
溶
Ca2+
微溶
溶
溶
微溶
不溶
Mg2+
不溶
溶
溶
溶
微溶
Cu2+
不溶
溶
溶
溶
不溶
试回答:
(1)写出下列溶液中的离子:
NaCl溶液中有 ,
MgSO4溶液中有 ,
Cu(NO3)2溶液中有 。
(2)CaCO3和HCl溶液反应的化学方程式:_______________________
(3)写出CaCl2解离方程式:
16.(12分)某同学将一小包铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到固体和蓝色滤液,并对滤液的组成进行探究。
(1)锌和硝酸银溶液反应的化学方程式是 __________ 。
(2)同学们对滤液中所含的溶质做出多种猜想,其中有两种猜想可能成立。
①溶质为_____ ___;②溶质为__ __。
(3)请你设计两种实验方案来验证以上猜想。
方案
实验操作
实验现象
结 论
方案一
如果
猜想 成立
方案二
如果
猜想 成立
三、计算(共5分)
17、(5分) 某研究性学习小组称取含NaCl的Na2CO3固体
计算:原固体中Na2CO3的质量分数和消耗盐酸的总质量。