2008年河北省初中毕业生升学文化课考试
理科综合化学部分
(满分120分,考试时间120分钟)
一、选择题(本大题共22个小题;每小题2分,共44分。在每小题给出的四个选项中,只有一个选项是正确的)
1.下列变化过程中,一定发生化学变化的是
A.西瓜榨成西瓜汁 B.铝块压制成铝箔
C.石蜡熔化成蜡油 D.玉米酿制成酒精
2.列各组物质混合搅拌后,能形成溶液的是
A.面粉和水 B.汽油和水 C.蔗糖和水 D.食用油和洗涤剂
3.化学与生活密切相关。生活中,下列做法不正确的是
A.食用牛奶补充蛋白质
B.用霉变的大豆制作豆腐
C.用灼烧的方法鉴别羊毛和涤纶
D.食用含钙食品预防骨质疏松
4.元素周期表是学习化学的重要工具。如下图是元素周期表中的一格,从中获取的信息正确的是

A.该元素原子的核内有20个质子
B.该元素离子的核外有20个电子
C.该元素属于非金属元素
D.该元素原子的质量为
5.正确的操作能保证实验顺利进行。下列实验操作正确的是
A.稀释浓硫酸时,将水沿容器壁慢慢注入浓硫酸中,并不断搅拌
B.实验室制取二氧化碳时,先加入药品,再检查装置的气密性
C.做铁丝在氧气中燃烧的实验时,在集气瓶底部预先加少量水或铺一层沙子
D.加热高锰酸钾制氧气并用排水法收集,实验结束时应先熄火酒精灯再撤导管
6.为验证Fe、Cu、Ag三种金属的活动性是依次减弱的,某化学兴趣小组设计了如图所示的四个实验,其中不必进行的是
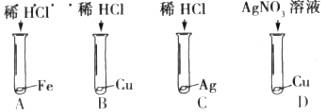
7.推理是化学学习中常用的思维方法。下列推理正确的是
A.酸能使紫色石蕊溶液变红。通入CO2后的紫色石蕊溶液变红,所以CO2是酸
B.酸性溶液的pH小于7。食醋是酸性溶液,所以食醋的pH小于7
C.在同一化合物中,金属元素显正价,所以非金属元素一定显负价
D.溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小
8.如图所示物质的用途中,主要利用其物理性质的是

A B C D
9.参与节能减排是每一位公民应尽的义务。下列做法不符合节能减排要求的是
A.尽量使用一次性餐具 B.用布袋代替翅料购物袋
C.关闭电器后拔掉插头 D.杜绝自来水的跑、冒、滴、漏现象
10.用分子的知识对下列现象的解释,正确的是
A.做饭时炊烟袅袅,是由于分子间存在斥力
B.一块金属很难被压缩,是由于分子问没有间隙
C.变瘪的乒乓球放入热水中鼓起来,是由于分子受热变大
D.房间里放一箱苹果,满屋飘香,是由于分子做无规则运动
11.下列现象的产生,与空气中的水蒸气无关的是
A.酥脆的饼干放置在空气中变软
B.夏天从冰箱取出的冰糕冒“白气”
C.冬季的早晨看到窗户的玻璃上有“冰花”
D.进入久未开启的菜窖或干洞深井使人感到气闷、头昏
二、填空题(本大题共9个小题;第23小题3分,其余小题每空1分,共31分。请将正确答案填在题中的横线上或空格内)
27.2008年北京奥运会使用的“祥云”火炬,内装燃料是液态丙烷。常温下,丙烷气体通过_____________的方法变为液态,灌装在火炬内。丙烷燃烧的化学方程式为C3H8+ O2
O2 yCO2+
yCO2+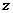 H2O,则
H2O,则 的值为________。已知丙烷的热值为5.04×107J?kg
的值为________。已知丙烷的热值为5.04×107J?kg ,完全燃烧
,完全燃烧
28.如图所示的是电解水实验装置。通电一段时间后,在两个试管中分别收集到气体 和气体
和气体 。
。

请回答:
(1)电解水时,将________转化为化学能;
(2)气体 为________;
为________;
(3)实验室检验气体b的方法是________________。
29.空气、水是人类赖以生存的自然资源。
(1)空气中含有氮气、氧气、稀有气体等,是一种________ (填物质类别)。人类时刻都离不开空气,是因为空气中的氧气能________________。
(2)天然水中含有许多杂质,将天然水变成纯水的方法是________。利用蒸发原理可以从海水中提取食盐,实验室蒸发食盐水时用到的仪器有________ (填序号)。
①带铁圈的铁架台 ②酒精灯 ③漏斗 ④玻璃棒 ⑤量筒 ⑥蒸发皿
30.金属材料在生产、生活中有着广泛的应用。
(1)人类每年从自然界提取大量的金属,其中提取量最大的是铁。用赤铁矿(主要成分为Fe2O3)和一氧化碳炼铁的化学方程式为________________。
(2)北京奥运会用到多种材料。下列应用中使用金属材料的有________ (填序号)。
①使用金、银和铜等制作奖牌
②使用纯羊毛和聚酯纤维制作“福娃”
③使用新型钢材建造“鸟巢”
④使用聚氟乙烯制造“水立方”外层膜
(3)金属矿物的储量有限,而且不能再生,所以保护金属资源尤为重要。保护金属资源的有效途径是_______________________ (答出两条即可)。
31.A―H都是初中化学中的常见物质,它们之间的转化关系如图所示。A是天然气的主要成分,E是一种常见的食品干燥剂。
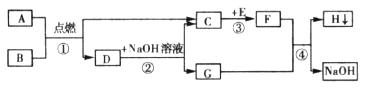
请回答:
(1)A的化学式为______________________;
(2)反应③的基本反应类型是____________________________;
(3)反应②的化学方程式为_____________________;
反应④的化学方程式为_____________________。
三、实验探究题(第36、37小题各5分)
36.为了探究燃烧的条件,小军查阅资料得知,白磷的着火点为
①试管中的白磷燃烧,产生大量的白烟;
②试管中的红磷不燃烧;
③烧杯中的白磷不燃烧。
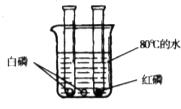
(1)白磷燃烧的化学方程式为____________________。
(2)分析实验现象,得出结论。
由现象①②得到的燃烧条件是____________________;
由现象①③得到的燃烧条件是_____________________。
(3)请举一例说明燃烧必须有可燃物参加。
__________________________________________________。
(4)请你根据小军查阅的资料和实验现象,指出他设计的装置有何不足。
__________________________________________________。
37.人的胃液里含有适量的盐酸,可以帮助消化,但如果胃酸分泌过多,人会感到胃痛。小军拿来了一种抗酸药(治疗胃酸过多的药物),该药物说明书的部分内容如图所示。

为了验证该药物的主要成分是碳酸盐,他进行了如下实验:首先将药片放入试管中,向其中加入适量的稀盐酸,然后_______________________________________(写实验操作和实验现象)。
当小军看到药物说明书上的服用方法后,对此产生了探究的兴趣,请你和他一起完成探究活动。
【提出问题】抗酸药为什么嚼碎后服用?
【作出猜想】他的猜想是____________________________。
【设计实验】实验一:将一片完整的药片放入试管中,向其中加入5 mL 5%的稀盐酸;
实验二:将______________放入试管中,向其中加入5 mL 5%的稀盐酸。
【现象与结论】实验二比实验一反应快。证明小军的猜想正确。
【拓展探究】(1)氢氧化镁、碳酸钙、碳酸氢钠等也常用于制作抗酸药。这些物质必须具备两个条件:一是能与胃酸作用;二是_______________________________。
(2)患有胃溃疡(胃黏膜溃烂)的病人胃酸过多时,不宜服用含碳酸盐的抗酸药,其原因是________________________。
四、计算应用题(第38小题5分,第39小题6分.解答时,要求有必要的文字说明、公式和计算步骤等,只写最后结果不得分)
38.过氧化氢溶液长期保存会自然分解,使得溶质质量分数减小。小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定溶质质量分数。他们取出该溶液
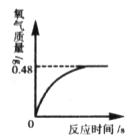
(1)完全反应后生成氧气的质量为__________________。
(2)计算该溶液中溶质的质量分数。