2008-2009学年度淄博张店实验中学第一学期初四期中学业自评
化学试卷
一、选择题:(每小题只有一个正确答案,请将正确答案写在下表中。)
1、下列说法中不正确的是( )
A.石蕊试液是一种酸碱指示剂 B.酸溶液能使红色石蕊试纸变蓝
C.酸溶液中都含有氢离子 D.碱溶液中都含有氢氧根离子
2、一些食物的近似pH如下:牛奶6.3~6.6 鸡蛋清7.6―8.0 柠檬2.2~2.4 番茄4.0~4.4其中碱性最强的是( )
A.牛奶 B.鸡蛋清 C.柠檬 D.番茄
3、欲使任意一种不饱和溶液转变为饱和溶液,不行的方法是( )
A.改变温度 B.蒸发溶剂 C.加溶质 D.倒出一些溶液
4、向滴有酚酞的NaOH溶液中,逐滴滴入稀硫酸至过量,下面的叙述中正确的是( )
A.溶液由红色变为无色,pH逐渐增大 B.溶液由无色变为红色,pH逐渐减小
C.溶液由红色变为无色,pH逐渐减小 D.溶液颜色不变,pH逐渐增大
5、下列说法正确的是( )
A.盐酸能使紫色石蕊试液变蓝
B.浓硫酸露置于空气中溶质的质量分数变大
C.打开盛浓盐酸的试剂瓶,瓶口会产生白雾
D.露置于空气中的固体氢氧化钠,其成分不会发生变化
6、下列质量增加的变化有一种与其它三种存在着本质的区别,这种变化是( )
A.长期放置在空气中的氢氧化钠 B.长期敞口放置的浓硫酸
C.久置在空气中的生石灰 D.久置在空气中的铁钉
7、下列各物质不能与稀盐酸发生反应的是( )
A.镁条 B.生锈铁钉 C.碳酸钙 D.氯化铜溶液
8、NaOH+H2SO4,HCl+Ca(OH)2这两个反应的共同点是( )
①都是中和反应②都是复分解反应③都有气体生成④都生成白色沉淀
A.①② B.①④ C.②④ D.①④
9、欲除去氯化钙溶液中含有的少量盐酸,在不用指示剂的条件下,应加入的试剂是( )
A.生石灰 B.石灰水 C.纯碱 D.石灰石
10、只用一种物质一次就能将稀硫酸、水、澄清石灰水三种无色液体鉴别出来,可供选用的物质是:( )
①PH试纸、②酚酞试液、③稀盐酸、④碳酸钠溶液、⑤石蕊试液,其中能用鉴别的是
A.①④⑤ B.①②⑤ C.①②③ D.③④⑤
11、怎样判断某一溶液是否为饱和溶液?( )
A.保持溶剂的质量不变,降低温度观察是否有溶质析出
B.保持溶液的温度不变,蒸发水分观察是否有溶质析出
C.保持溶液的温度不变,继续加入同种溶质,观察能否继续溶解
D.保持溶液的温度不变,继续加入不同种溶质,观察能否继续溶解
12、下列关于海水晒盐原理的分析,正确的是( )
A.利用阳光照射使海水升温得到食盐
B.利用阳光和风力将水分蒸发得到食盐
C.利用机械动力搅拌得到食盐
D.利用海水在阳光下发生分解反应制得食盐
13、下列物质中不属于盐的是( )
A.纯碱 B.高锰酸钾 C.硫酸钡 D.蔗糖
14、下列气体能用浓硫酸干燥,而不能用氢氧化钠固体干燥的是( )
A.H2 B、O
15、下列说法正确的是( )
A.氯化钠的溶解度为
B.饱和溶液的质量分数一定比不饱和溶液的质量分数大。
C.在一定温度下,搅拌不能改变硝酸钾的溶解度。
D.固体物质的溶解度都是随着温度的升高而增大。
E.蒸发结晶食盐时,要等水分全部蒸发,才能停止加热
二、填空题:
1、把表面生锈的铁片漫入过量的盐酸中,首先观察到 ,过一会儿又观察到_ _ _ _ _ 。有关反应的化学方程式为
2、土壤中含有的少量硫酸为改良土壤应撒 ,反应的化学方程式
3、某河水的pH在1~4之间,该河水呈 性。如果让你测定该河水的酸碱度,你会怎么做? 。
4、为鉴别盐酸、氯化钠、氢氧化钠、氢氧化钙四种溶液,先向取出的少量四种溶液中分别滴加紫色的石蕊试液,先被鉴别出的两种溶液分别是 和_____。另取少量还未鉴别出的两种溶液,分别加入碳酸钠溶液,有白色沉淀生成的是 无现象的是 。
5、如果将咸菜放在空气中,过一段时间后咸菜表面会有一层白色晶体析出原因是
6、A图表示硝酸钾和氢氧化钙的溶解度随温度变化的情况。B图中甲、乙试管分别盛有硝酸钾、氢氧化钙的饱和溶液,试管底部均有未溶解的固体。向烧杯中加入氢氧化钠后,甲试管中固体 ,乙试管中的固体 ,(填增加或减少)。

7、海水制碱过程中,氨盐水吸收二氧化碳后先析出 晶体,原因是
8、钡餐透视时要用硫酸钡,若误服碳酸钡就会中毒生成可溶性钡盐,写出化学方程式
9、某化工厂用石灰石制取碳酸钙,流程图为

请写出上述方案中所依据反应的化学方程式:①
② ③
10、下图为硝酸钾和氯化钠的溶解度曲线.由图可知:
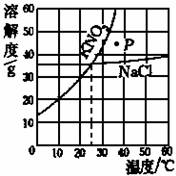
(1)当温度 时,硝酸钾与氯化钠的溶解度相等。
(2)当温度 时,氯化钠的溶解度大于硝酸钾的溶解度。
(3)图中P点表示KNO3的 溶液。
(4)当温度为
(5)固体硝酸钾中混有少量的固体氯化钠,欲从中提纯硝酸钾,常采用_______ _____的方法;
(6)生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”其中的原因是
鉴别物质时通常先用物理方法,后用化学方法。先需鉴别三包失去标签的白色固体粉末,它们可能是CaCO3、Na2CO3和Na2SO4,请按下表完成实验设计:
实验步骤
现象和结论
步骤一(物理方法)
步骤二(化学方法)
某同学实地考察后收集到了以下资料:
(1)某化工厂的污水主要成分是盐酸, pH=3;
(2)用石灰水将污水进行中和处理
四、计算题:
(3)处理后pH在7.0左右。根据上述资料,回答下列问题:
①该同学的这种考察属于 调查(“直接”或“间接”)
②已知污水中盐酸的质量分数为0.073%。假设中和池中有1.0×