2007-2008学年度潍坊市高密第二学期八年级期末考试
化学试卷
(时间:60分钟 满分:100分)
可能用到的相对原子质量:H-1,C-12,O-16,Cl-35.5,Ca-40
一.选择题(四选一,请把正确答案的序号填在下表内,每小题2分,共40分)
1.锂电池可用作心脏起搏器的电源。已知一种锂原子核内含有3个质子和4个中子,则该锂原子的核外电子数为( )
A.1
B.
2.据报道,某研究小组将二氧化碳与氢气按1:4比例在一定温度、压强下混合并以铑―镁为催化剂可生成X,其反应为CO2+4H2==X+2H2O,则X为( )
A.CO B.CH
3.某些食品包装袋内常有一小包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸剂”。下列物质属与“双吸剂”的是( )
A.炭粉 B.铁粉 C.氯化钠 D.生石灰
4.人体吸入的O2有2%转化为活性氧,它加速人体衰老,被称为“夺命杀手”。我国科学家尝试用Na2SeO3清除人体内的活性氧,Na2SeO3中Se(硒)元素的化合价是( )
A.+2 B.+
5.生活中的下列变化属于化学变化的是( )
①燃放烟花 ②蜡烛燃烧 ③汽油挥发 ④煤矿爆炸 ⑤钢铁生锈 ⑥食物变坏 ⑦水烧开 ⑧瓷碗摔碎
A.①②③④⑧ B.①③④⑤⑥⑦ C.全是 D.①②④⑤⑥
6.图1所示的结构示意图中表示阳离子的是( )
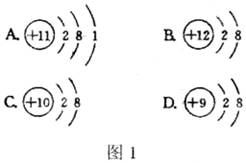
7.下列关于金属的说法错误的是( )
A.金属钨的熔点较高,用钨制成的灯丝不易熔化
B.铁的化学性质比较活泼,不能用铁桶盛放硫酸铜溶液
C.硬铝合金密度小、硬度大、抗腐蚀,可用于制造飞机、火箭和轮船
D.在自然界中,金属都是以化合物的形式存在
8.下列与燃烧或燃料有关的说法正确的是( )
A.家用煤制成蜂窝状的目的是延缓煤的燃烧时间,节约能源
B.露置在空气中的汽油没有燃烧是因为汽油是液态的
C.汽车使用乙醇汽油(掺有乙醇的汽油)可以减轻汽车尾气的污染,节约石油资源
D.太阳能热水器的主要工作原理是水在阳光的作用下发生了化学反应,该反应放出热量
9.将足量的铁粉投入到硫酸和硫酸铜的混合溶液中,充分反应后过滤,则滤液里含有的物质是( )
A.硫酸铁 B.硫酸铜 C.硫酸 D.硫酸亚铁
10.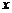 CO2+
CO2+ H2O,其中
H2O,其中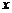 、
、 分别为( )
分别为( )
A.1 3 B.1
11.下列有关合金的叙述:①合金至少含两种金属;②合金中的元素以化台物形式存在;③合金中一定含有金属;④合金一定是混合物;⑤生铁是含有杂质较多(与钢相比)的铁合金;⑥生铁可完全溶解于稀盐酸之中。正确的是( )
A.①②③④⑤⑥ B.①② C.①③④⑥ D.③④⑤
12.饮料中的果味大多来自酯类。丁酸乙酯(C6H12O2)是无色具有菠萝香味的液体,常用作食品、饮料的调香剂。下列叙述中,正确的是( )
A.丁酸乙酯是由20个原子构成的
B.丁酸乙酯的相对分子质量为
C.丁酸乙酯中碳、氢、氧元素的质量比为18:3:8
D.一个丁酸乙酯分子中,碳、氢、氧原子的个数比为3:6:2
13.下列现象或事实,用分子的相关知识加以解释,其中不正确的是( )
现象或事实
解释
A
热胀冷缩
分子大小随温度改变而改变
B
酒香不怕巷子深
分子不断地运动
C
氧气可供人呼吸,一氧化碳有毒
构成物质的分子不同,物质的性质不同
D
水通电后生成氢气和氧气
在化学变化中分子可以再分
14.用灯帽盖灭酒精灯的灭火原理是( )
A.将可燃物撤离燃烧区,与火源隔离
B.使用大量冷却剂,使燃烧物冷却,让燃烧物温度降到着火点以下
C.将燃烧着的可燃物与空气隔离
D.降低着火点
15.下列反应属于置换反应的是( )
A.H2CO3==H2O+CO2↑ B.CaO+H2O==Ca(OH)2
C.Fe+CuSO4==FeSO4+Cu D.2NaOH+H2SO4==Na2SO4+2H2O
16.某化合物完全燃烧需要
A.含有C、H、O三种元素 B.含有C、O两种元素
C.含有C、H两种元素 D.无法确定
17.在反应
A.4:19 B.3:
18.如图2所示的实验方法或操作正确的是( )
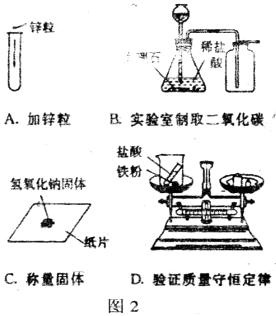
19.在一密闭容器中,盛放A、B、C三种物质各
物质
A
B
C
新物质D
反应前物质质量/g
30
30
30
0
反应后物质质量/g
待测
33
0
22
关于此反应,下列认识不正确的是( )
A.C物质中所含有的元素种类是A、B、D三种物质中所有元素种类之和
B.变化后待测的A质量为
C.该变化的基本反应类型是分解反应
D.A物质有可能是单质
20.两份质量相等的碳酸钙,一份与足量的稀盐酸反应,另一份高温煅烧,则所得二氧化碳的质量是( )
A.与盐酸反应产生的多 B.高温分解产生的多
C.一样多 D.无法判断
二.填空题(本题包括7小题,共31分)
21.(4分)
22.(2分)用化学用语表示:
(1)氮元素 (2)2个氢分子 (3)3个镁离子 (4)硫酸铁
23.(5分)已知A、B、C三种元素的粒子结构示意图(见图3)依次为
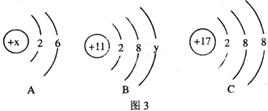
(1)当A、B为原子结构示意图时,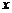 =________;
=________; =________。
=________。
(2)C表示的是________的结构示意图(填“阳离子”、“阴离子”、“原子”);该元素与B元素形成化合物的化学式为________________;该化合物是由________________(填“分子”、“原子”、“离子”)构成的。
24.(6分)根据下列要求,写出有关反应的化学方程式。
(1)有氧化物和单质参加的化合反应
(2)有氧化物和单质生成的分解反应
(3)有金属单质生成的置换反应
25.(4分)北京奥运火种采集工作于
26.(5分)某学生利用一支底部有破洞的试管和一个广口瓶组装成制取二氧化碳的发生装置(如图4所示):
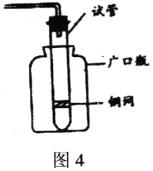
在铜网上应盛放____________________,广口瓶中应盛有____________________。若将铜网换成铁网,那么产生的后果是________________________________________,其原因是(用化学方程式表示) ________________________________________。
27.(5分)把点燃的镁条放入盛有二氧化碳的集气瓶里,可看到镁条剧烈燃烧,生成白色粉末和黑色固体。
(1)写出有关反应的化学方程式,并解释集气瓶底部放一些细沙的原因。
化学方程式_______________________;原因:____________________________
(2)从这个化学反应里,谈一谈你对燃烧和灭火有什么新的认识。
燃烧:___________________________;灭火:______________________________
三.实验探究题(本题包括3小题,共23分)
28.(6分)钢铁是人类生活和生产中非常重要的材料,但全世界每年都有约四分之一的钢铁因生锈而损失。某化学课外活动小组,对钢铁制品锈蚀的条件进行如下探究,设计了如图5所示的实验,据此回答下列有关问题:
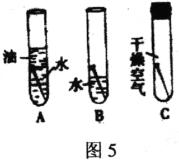
(1)一周后,观察到编号为__________的试管中的铁钉锈蚀严重。
(2)常温下,铁生锈的条件是铁跟__________和__________等物质相互作用的结果,铁锈的主要成分是____________________(均用化学式表示)。
(3)欲除去铁锈,同学们提出了三种不同的实验方法:①用砂布擦;②用稀盐酸洗;③用稀碱液泡。你认为最有效的方法是___________________ (填序号)。
(4)如何防止家庭中常用的铁制品生锈,简单易行的方法有(列举一种方法) _________
29.(6分)请你和小亮一起走进化学实验室,共同学习科学探究的方法。
小亮在实验室用一小块生铁与稀盐酸反应,观察到生铁表面出现__________________,同时发现反应后的液体中有少量黑色不溶物。
提出问题:这种黑色不溶物是什么呢?
猜想与假设:这种黑色不溶物中可能含碳。
设计方案:将此黑色固体燃烧,如果其中含碳,就会有__________________气体生成,要想进一步确定这种气体,可以用__________________来检验。
进行实验:小亮按设计方案进行实验,得到了预想的结果。
解释与结论:(1)生铁中______ (填“含”或“不含”)碳。(2)碳与稀盐酸____(填“能”或“不能”,下同)反应;铁与稀盐酸__________________反应。
30.(11分)某学生改进一氧化碳还原氧化铁的实验装置,如图6所示:
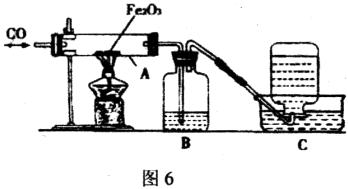
(1)若先给氧化铁加热,再通入一氧化碳,可能产生的后果是_____________________。
(2)写出A中发生化学反应的方程式:___________________________。
(3)根据B装置中所产生的现象可判断反应是否开始发生,则B中盛放的试剂是_________,化学反应的方程式为____________________________________。
(4)C装置的作用是____________________________________。
(5)C装置收集气体的方法叫做___________________________,收集到C瓶中的气体如何处理____________________________________。
(6)A、B两处的现象分别是_____________________、_______________________。
四.计算题(本题包括1小题,共6分)
31.(6分)工业上,高温煅烧石灰石(CaCO3)可制得生石灰(CaO)和二氧化碳。如果高温煅烧含碳酸钙80%的石灰石25吨(杂质不反应),最多可制得二氧化碳多少吨?