分类复习(四)
测试时间:100分钟 总分:100分
一、选择题(每题3分,共45分)
1.玻璃仪器洗干净的标志是 ( )
A.内壁上有少量水珠 B.内壁上的水成股流下
C.透明 D.内壁上附着的水均匀地形成水膜
2.检验某气体是否为二氧化碳,常用的方法是 ( )
A.将气体通入澄清的石灰水中 B.将气体通入紫色石蕊试液
C.将燃着的小木条放到气体中 D.称量气体的质量
3.实验室收集了一瓶二氧化碳,集气瓶口应 ( )
A.朝下 B.朝上 C.随意放置 D.以上都不对
4.下列有关实验操作的说法中,错误的是 ( )
A.给试管内的固体加热应该先进行预热
B.滴瓶上的滴管用后直接放回滴瓶
C.使用酒精灯前,必须向酒精灯里添满酒精
D.量筒不能用作反应容器
5.某同学进行过滤的实验操作,发现得到的滤液仍浑浊,可能的原因有 ( )
A.滤纸不够厚 B.液面低于纸边缘
C.滤纸破损 D.原滤液很浑浊
6.对电解水实验现象描述正确的是 ( )
A.接电流正极的试管内放出一种可燃性气体
B.与电源正极相连的试管内产生的气体体积是与电源负极相连的试管内气体体积的2倍
C.与电源负极相连的试管内产生的气体体积是与电源正极相连的试管内气体体积的2倍
D.与电源负极相连的试管内产生的气体能使余烬的木条复燃
7.实验室选择制取气体的仪器装置时,可以不考虑的因素是 ( )
A.反应物的性质和状态 B.所制气体的性质
C.所制气体的颜色 D.反应的条件
8.如下图所示,能说明CO2 ( )
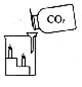
①不能燃烧 ②一般不支持燃烧 ③比空气重 ④不能供给呼吸
A.①②③④ B.①② C.①②③ D.②③
9.若将CO2通入紫色石蕊溶液,再加热溶液,颜色变化过程为 ( )
A.无色――红色――无色 B.紫色――红色――无色
C.紫色――红色――紫色 D.红色――蓝色――红色
10.鉴别空气、氧气和二氧化碳三瓶气体最简便的方法是 ( )
A.用燃着的木条分别伸入三瓶气体中
B.通过实验测定气体的密度
C.将少量澄清石灰水分别倒入三瓶气体中
D.用带火星的木条分别伸入三瓶气体中
11.点燃某气体后,在火焰上方罩一个干燥的烧杯,烧杯内壁有水珠出现。把烧杯迅速倒过来,立即向烧杯内注入少量澄清石灰水振荡,石灰水变浑浊。该气体可能是( )
A.氢气 B.甲烷 C.一氧化碳 D.氧气
12.欲鉴别H2、O2、空气、CO2、CH4五种气体,现有一盒火柴,还要用到实验用品的是 ( )
A.干燥而冷的烧杯 B.盛有蒸馏水的烧杯
C.盛有无色酚酞试液的烧杯 D.内壁涂有澄清石灰水的烧杯
13.某同学加热2~3mL的蒸馏水,操作的正确顺序应该是 ( )
①用试管夹夹好试管 ②点燃酒精灯 ③加热 ④往试管中加入2~3mL蒸馏水
⑤盖好试剂瓶,放回原处
A.④⑤①②③ B.①④⑤②③
C.②①④③⑤ D.④①②③⑤
14.已知实验室制取丙的化学方程式为:甲(固)+乙(固)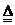 丙↑+丁,且气体丙易溶于水,密度比空气大,则应选用的装置和收集方法是 ( )
丙↑+丁,且气体丙易溶于水,密度比空气大,则应选用的装置和收集方法是 ( )
A.制CO2发生装置和排水法 B.制O2发生装置和向上排空气法
C.制CO2发生装置和向下排空气法 D.制O2发生装置和排水法
15.下图是收集干燥的R气体并对它进行吸收处理的正确装置。由图中实验装置推测该气体的有关性质,正确的一组是 ( )
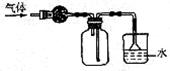
A
B
C
D
密度(与空气比较)
大于
大于
小于
小于
在水中的溶解性
难溶
极易溶
极易溶
难溶
二、填空题(24分)
16.(5分)如图,将滴有酚酞试液的滤纸条放入试管里,放在实验台上:

(1)用仪器A吸取浓氨水,滴在管口棉花上(10滴至l5滴),
A的名称是 ,该仪器的用途是 。
(2)实验中,往往在试管下放一张白纸,白纸的作用是 。
(3)实验中,观察到的现象是 ,这一实验说明了 。
17.(4分)现有无标记的四种无色气体A、B、C、D,按下表做实验,试根据所观察到的现象确定它们分别是空气、氮气、二氧化碳和氧气中的哪一种。
实验步骤
A
B
C
D
①将燃着的木条插入集气瓶内
燃烧更旺
不变化
熄灭
熄灭
②向装有C、D的瓶中倒入澄清的石灰水
无变化
变浑浊
确定物质
18.(4分)指出下图所示操作中的错误,并说明错误操作将引起的后果。
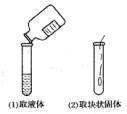
(1)操作中的错误是 ;
错误操作将引起的后果; 。
(2)操作中的错误是 ;
错误操作将引起的后果: 。
19.(4分)将下列数据填入适当的空格内。
①45° ②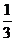 ③
③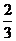 ④0.1 ④0.01
④0.1 ④0.01
(1)初中化学实验中所用的托盘天平一般准确到 g。
(2)给试管里的液体加热时,应使用试管夹,试管夹应夹在离试管口大约 处, 试管里液体的体积不能超过试管容积的 ,试管与水平面成 ,且试管口不要对着自己或他人。
20.(7分)如图所示,烧杯中盛有热水,内有白磷(乙)一块,在薄铜片上放有白磷(甲)和红磷。
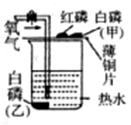
(1)上述实验中,可以观察到的现象:白磷(甲) ;白磷(乙) ;红磷 。
(2)由(1)的现象可以说明的问题是 。
(3)若沿导管向水中白磷表面通入氧气,可以观察到的现象及原因是
。
三、实验探究题(每空2分,共22分)
21.化学兴趣小组的同学设计了一个对比实验,探究燃烧现象。点燃三支蜡烛,在其中一支蜡烛上扣一只烧杯A,将另两支蜡烛放在烧杯中,然后向烧杯C中加适量碳酸钠和盐酸。
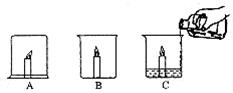
(1)请你帮助他们填写下表:
A
B
C
现象
烛焰燃烧
原因
接触空气
(2)从燃烧的对比实验中得到的初步结论:
① ;
② 。
22.某学生兴趣小组对过量炭粉与氧化铁反应产物中的成分进行研究。
(1)假设:该反应的气体产物全部是二氧化碳。
(2)设计方案:将一定量氧化铁在隔绝氧气的条件下与过量炭粉完全反应,测定参加反应的碳元素与氧元素的质量比。
(3)查阅资料;氮气不与碳、氧化铁发生反应,可用来隔绝氧气。
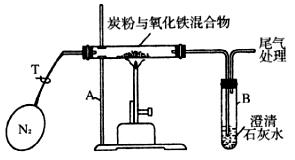
(4)实验:
操作步骤及实验现象
简答
①称取
写出装置中编号仪器的名称:
A B
②加热前,先通入一段时间纯净、干燥的氮气。
其目的是
③夹紧T处弹簧夹,加热一段时间,澄清石灰水变浑浊。
该现象说明
④完全反应后,冷却到室温,称得玻璃管和固体
的总质量为
(5)数据处理:经计算,参加反应的碳元素质量为0.
(6)结论:根据数据处理结果,得出原假设不成立,理由是 。
四、计算题(9分)
23.把
第一次
第二次
第三次
O2质量(g)
3
4
6
SO2质量(g)
6
?
?
请回答下列问题:
(1)第一次实验中,参加反应的S的质量、O2的质量与生成的SO2的质量比是 。
(2)请你通过计算求出第二次实验生成二氧化硫多少克?
(3)在表中填写第三次实验生成二氧化硫的质量。