2008年江苏省启东中学中考模拟考试(九)
化学试卷
可能用到的相对原子质量:C一12 H―l O一16 N一14 Mg一24 Cl一35.5
S一32 Na一23 Ca一40 Cu一64
一、选择题(本题包括l5小题,每小题2分,共30分。每小题只有一个选项符合题意)
1.生活与化学有着密切的联系,以下叙述中只发生物理变化的是 ( )
A.用稀盐酸除去热水瓶内壁上的水垢
B.吃进的食物一段时间后被消化了
C.淋雨后,自行车生了锈
D.水放进冰箱一段时间后结冰
2.暑假的一天,两位同学高兴地在一起吃西瓜,并围绕人体所需的营养素进行如下交流对话。你认为他们的说法不当的是 ( )
A.“西瓜中富含水分和维生素,能调节人体的新陈代谢、增强人体抗病能力。”
B.“西瓜中还含有糖类,能为人体提供能量。”
C.“不吃饭菜光吃西瓜就有足够的营养了。”
D.“除了维生素,油脂、淀粉、蛋白质也是人体必须摄人的。”
3.水与我们息息相关,下列关于水的认识正确的是 ( )
A.水电解产生氢气和氧气,说明水分子中含有氢分子和氧分子
B.物质溶解于水时都会放出热量
C.利用活性炭吸附水中的杂质可以使水软化
D.使用无磷洗衣粉有利于防止水体富营养化
4.“先锋Ⅵ”是一种抗生素,可用于肌肉注射。常用的“先锋Ⅵ”为粉末状固体,每瓶中有先锋素0.
A.2mL B.1mL C.3Ml D.4mL
5.下列关于化学反应的说法中正确的是 ( )
A.氧化反应一定属于化合反应 B.生成盐和水的反应一定是中和反应
C.置换反应一定有金属单质生成 D.分解反应一定只有一种反应物
6.下列粒子的结构示意图中属于阴离子的是 ( )

7.下列各组气体中,均能用固体氢氧化钠干燥的一组是 ( )
A.H2、O2、CO B.H2、O2、HCl C.H2、SO2、CO D.O2、CO、CO2
8.1777年舍勒在《火与空气》一书中指出:空气由两种性质不同的“火空气”和“浊空气”组成,其中“火空气”可以帮助燃烧,维持生命。下列物质不能与“火空气”发生反应的是 ( )
A.木炭 B.石蜡 C.烧碱 D.乙醇
9.过氧化氢(H2O2)是一种无色黏稠的液体,易分解为水和氧气,常用作氧化剂、漂白剂和消毒剂。为了贮存、运输、使用的方便,工业上将过氧化氢转化为固态的过碳酸钠晶体(2Na2CO3?3H2O2),该晶体具有碳酸钠和过氧化氢的双重性质。接触下列物质不会使过碳酸钠失效的是 ( )
A.二氧化锰 B.硫酸铜 C.盐酸 D.氯化钠
10.下列关于化学反应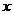 M+
M+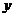 N==mP+nQ的说法中,正确的是 ( )
N==mP+nQ的说法中,正确的是 ( )
A.化学计量数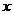 与
与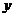 的和一定等于m与n的和
的和一定等于m与n的和
B.该反应为复分解反应,且在P和Q中一定有一种物质为水
C.反应物M和N的质量比一定等于生成物P和Q的质量比
D.若参加反应的M为 、N为
、N为 ,反应后生成的P和Q的质量总和一定不是
,反应后生成的P和Q的质量总和一定不是
11.在学习化学的过程中,总结规律要严谨、全面、科学。下列总结出的规律符合这一要求的是 ( )
A.质子数相同的粒子一定是同种元素的原子
B.酸性溶液中一定含有氢离子
C.一定温度下的浓溶液一定是饱和溶液
D.有单质生成的反应一定是置换反应
12.人吸入空气,排出CO2等气体。为了证明人呼出的气体中含有CO2且能有效排除空 气中CO2的干扰,某学生设计了如图9一1所示的实验装置,为了除去空气中的CO2和检验人呼出的气体中含有CO2,则锥形瓶Ⅰ、Ⅱ中加入的试剂为 ( )
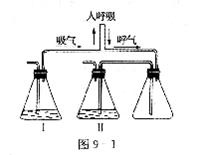
瓶 Ⅰ
瓶 Ⅱ
A
Ca(OH)2
NaOH
B
NaOH
Ca(OH)2
C
石蕊
酚酞
D
Na2SO4
CaCl2
13.2005年诺贝尔化学奖授予了三位科学家,以表彰他们在烯烃反应领域研究方面所取 得的成就。图9―2是他们研究烯烃反应的示意图。
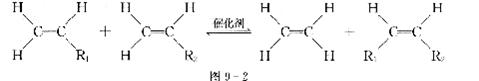
该反应属于四种反应类型中的 ( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
14.分离氯化钠、氯化铜、碳酸钡的混合物,在不引入新杂质的条件下,可以依次加入的一组试剂是 ( )
A.水、盐酸、氢氧化钡 B.水、氢氧化钠、盐酸
C.水、硫酸、氢氧化钙 D.水、氢氧化钡、盐酸
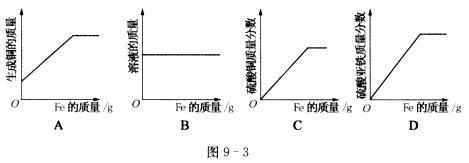
15.将足量的细铁丝放入一定量的硫酸铜溶液中,则图9―3中表示正确的是 ( )
二、选择题(本题包括5小题,每小题2分,共10分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给1分,选两个且都正确的给2分,但只要选错一个,该小题就为0分)
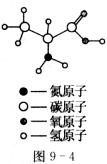
16.蛋白质是构成细胞的基本物质,蛋白质又是由多种氨基酸构成的复杂的、相对分子质量巨大的化合物。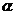 一丙氨酸是组成人体蛋白的氨基酸之一,图9―4是
一丙氨酸是组成人体蛋白的氨基酸之一,图9―4是 ―丙氨酸的分子结构模型图,下列对
―丙氨酸的分子结构模型图,下列对 一丙氨酸的叙述不正确的是 ( )
一丙氨酸的叙述不正确的是 ( )
A. ―丙氨酸属于氧化物
―丙氨酸属于氧化物
B.其化学式为C3H7O2N
C.分子中C、O原子个数比为3:2
D.在构成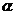 一丙氨酸的原子中,氢原子最小
一丙氨酸的原子中,氢原子最小
17.在氯化铜(CuCl2)和氯化镁(MgCl2)的混合溶液中加入一定量的铁粉,充分反应后过滤,取滤出的不溶物加稀硫酸无气泡产生。以下关于滤液中金属阳离子存在情况的推断中正确的是 ( )
A.可能含有Mg2+ B.可能含有Cu2+
C.一定不含Cu2+ D.一定含有Fe2+、Mg2+
18.下列各项实验中,所用试剂及实验操作均正确的是 ( )
19.不需其他试剂就能区别的一组溶液是 ( )
A.FeCl3、NaOH、KCl、Mg(NO3)2 B.NaCl、Na2CO3、KNO3、HCl
C.Na2SO4、BaCl2、K2CO3、KNO3 D.BaCl2、CuSO4、NaOH、NaCl
20.只含铜和氧两种元素的固体样品9.
A.固体样品的组成只有2种情况
B.固体样品一定是CuO和Cu2O的混合物
C.固体样品可能是Cu2O
D.若固体样品由两种物质组成,则其中一种质量分数为4/9
三、填空题(本题包括7小题,每空1分,共34分)
21.
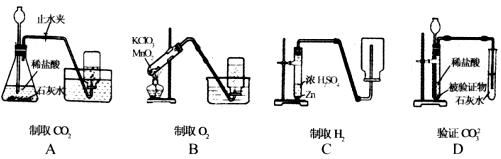
22.A、B两种物质的溶解度曲线如图9―5所示。
(1)A、B两种物质的溶解度相等时的温度为 ℃。
(2)B物质在t
(3)某温度下,当A、B两种物质形成的溶液均接近饱和状态时,通过增加溶质、蒸发溶剂或降低温度的方法,都可以达到饱和状态的是 物质形成的溶液。
23.五氯酚钠是一种水处理的杀菌灭藻剂,某五氯酚钠产品的说明书如图9―6所示。

请就你学过的化学知识回答下列问题:
(1)向五氯酚钠水溶液中滴加酚酞试液显 色。
(2)五氯酚钠中质量分数最大的元素是 。
(3)加酸酸化至pH为6.6~6.8时,发生 (“化学”或“物理”)变化。
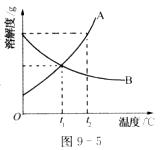
24.(1)锂是一种金属单质,化学式为Li,锂原子结构示意图为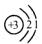 ,易失去最外层一个电子。则锂的氧化物的化学式为
。
,易失去最外层一个电子。则锂的氧化物的化学式为
。
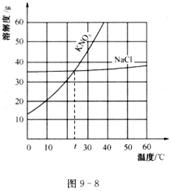
(2)化学反应A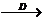 B+C,D在反应中作催化剂,
B+C,D在反应中作催化剂,
(3)工业酒精中常含有少量甲醇。甲醇有毒,易挥发。请你根据甲醇在氧气中完全燃烧 的产物是CO2和H2O,推断甲醇肯定含有 元素,还可能含有 元素。
25.利用如图9―7所示装置可进行气体性质的探究实验。甲的玻璃管中盛放黑色粉末(CuO或C),乙的洗气瓶中盛放无色溶液(澄清石灰水或NaOH溶液)。
(1)写出仪器的名称:a. ,b. 。
(2)根据要求填表:
实 验
甲
乙
实验一:探究CO与CuO
的反应。
反应的化学方程式:
氧化剂:
澄清石灰水的作用:
实验二:探究CO2与C的反应。
(b换成酒精喷灯)
反应的化学方程式:
反应类型:
NaOH溶液的作用:
(3)上述两个实验中,在导管c的尖嘴处都用火柴点燃,其目的是否完全相同?简述理由。
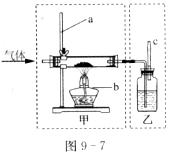
26.根据KNO3和NaCl的溶解度曲线(图9―8),回答下列问题:
(1)
(2)t℃时,将m g KNO3、n g NaCl分别溶解在20 mL水中恰好饱和,则m n(填“>”、“<”或“一”)。
(3)工业上采用如图9―9所示的流程从海水中提取精盐:

上述流程中I、Ⅱ、Ⅲ分别是 、 、 。
27.某化工厂排出的废水透明、澄清、略显蓝色。一同学取少量废水,加入过量的盐酸,有不溶于稀硝酸的白色沉淀生成。过滤,所得的滤液分成两份,一份滤液中加入稀硫酸,也有不溶于稀硝酸的白色沉淀生成;另一份滤液中加入氢氧化钠溶液,产生蓝色溶液。试回答:
(1)用化学式回答:加入过量的盐酸,生成的白色沉淀是 ;生成的蓝色沉淀是 。
(2)废水中一定含有的物质是 (填编号)
A.氯化物 B.硫酸盐 C.硝酸盐 D.碳酸盐
(3)该同学设计了一个从废水中除去重金属离子的实验方案如图9一10所示[已知白色的Fe(OH)2固体在潮湿的空气中可生成红褐色的Fe(OH)3]。
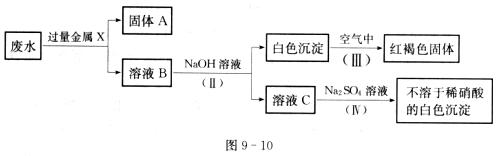
①金属X为 ,固体A中一定含有的物质为(写化学式) 。
②B溶液中的溶质一定含有 和 (填序号字母)。
A.K2CO3 B.Fe(NO3)
③第Ⅳ步反应的化学方程式为 .
四、实验题(本题包括3小题,每空1分,共15分)
28.某化学活动小组对实验室制取气体的发生装置进行探究。图9―11是改进后的实验 装置图:
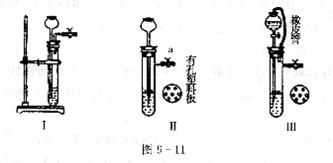
(1)检查装置Ⅱ气密性的方法是 。
(2)小松同学选用装置Ⅱ来制取CO2,现有①Na2CO3固体;②块状大理石;③稀盐酸;④稀硫酸,他应选用的试剂是 。(填序号)
(3)装置Ⅲ中橡皮管的作用是 .
29.小明和小芳在讨论“能否用蜡烛燃烧法来粗略测定空气中氧气的含量”这一问题时,小芳认为:通过图9―
,并用图9―

小明认真分析了小芳的实验结果后,进行了如下探究:
[提出问题]导致小芳这一实验结果还有其他原因吗?
[实验探究]小明设计了图9―12b装置,进行以下操作:
(1)取黄豆粒大小的白磷,用滤纸吸去表面的水分,放人捆在电烙铁下面铁片的凹槽内;
(2)将燃烧匙内的蜡烛点燃后迅速插入钟罩内,并立即塞紧橡皮塞;
(3)待蜡烛熄灭后(蜡烛有剩余),接通电烙铁电源,发现白磷先熔成液体,接着燃烧产生大量白烟,说明通电前钟罩内含有 ,产生白烟的化学反应方程式是 。
[得出结论]导致小芳这一实验结果的另一原因是 。
[交流与反思]小明和小芳分析了上述实验后,又提出了一个问题: 。
30.中和反应在日常生活和工农业生产中有广泛的应用。某化学兴趣小组的同学在老师的指导下对酸碱中和反应进行了探究。
[提出问题]能否用碳酸钾溶液验证硫酸与氢氧化钠溶液发生中和反应
[实验药品]稀硫酸、稀氢氧化钠溶液、碳酸钾溶液
[实验仪器]试管、滴管、10mL量筒等
[设计方案并实验]小江同学的实验:在试管中加入2 mL稀硫酸,逐滴加入 溶液,振荡后,再滴入V1mL 溶液,实验过程中无气泡逸出。反应的化学方程式为 。
小伟同学的实验:在试管中加入2 mL稀硫酸,逐滴加入氢氧化钠溶液,振荡后,再滴入碳酸钾溶液,有气泡逸出,继续滴加碳酸钾溶液至恰好无气泡时,共消耗碳酸钾溶液V2mL。
小明同学的判断:小江的实验说明能用碳酸钾溶液来验证;小伟的实验还不能,需再做一个实验才能说明。
实验并判断:另取一支试管,加入2 mL稀硫酸,
。(写出实验步骤、现象和判断依据)
[结论]能用碳酸钾溶液验证硫酸与氢氧化钠溶液发生中和反应。
[反思]在小江的实验中,碳酸钾溶液的作用是 (填字母)。
A.仅是反应物 B.相当于指示剂 C.作催化剂
五、计算题(本题包括2小题,共l0分)
31.苦卤是海水提取食盐后的残液,含有多种成分,在食品、化工等方面有重要应用。如图9―13是我国某盐场苦卤中各成分含量的柱形图。该盐场以苦卤和贝壳为原料按图9―14所示过程生产轻质氧化镁。假设生产过程中镁元素无损失,请计算
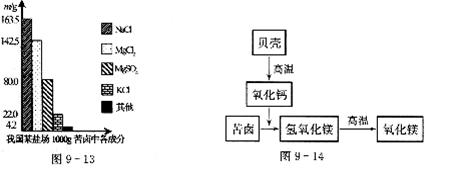
32.在一次课外活动中,先后有三组同学用含有碳酸钠的氯化钠固体进行了如下实验。
(1)为了得到纯净的氯化钠溶液,第一组同学取一定量的上述固体混合物,全部溶解于水,然后加入所选试剂,生成沉淀,恰好完全反应后过滤,所得滤液为氯化钠溶液。则该组同学选择的试剂是 (填写所选试剂编号)。
实验老师提供的试剂有:①盐酸,②氯化钙溶液,③氢氧化钡溶液。
(2)为测定该固体混合物中氯化钠的质量分数,第二组同学取该固体混合物26.
(3)第三组同学利用第一组同学除杂提纯氯化钠的方法,配制了