2008年聊城市阳谷县中考适应性训练(一)
化学试卷
(满分:50分 时间:50分钟)
相对原子量:H:
一、选择题(每小题只有一个选项符合题意,每小题2分,共20分)
1.在下列四组变化中,都属于化学变化的一组是 ( )
A.酒精燃烧 冰雪融化 B.蔬菜腐烂 菜刀生锈
C.榨取果汁 切削玻璃 D.粉碎废纸 燃放烟花
2.下列实验操作正确的是 ( )
A.胶头滴管用完后,将其横放在桌面上,以免试液流出
B.加热时,滴管中盛液体量不超过其容积的2/3
C.用剩的药品一定要放回原瓶,以免浪费
D.将试管夹从试管底部往上套,夹在试管中上部
3.下面是王小莉同学用连线的方式对某一主题内容进行归纳纳情况,其中有错误的一组是 ( )
A.元素与物质的组成

B.微观粒子与物质的构成

C.物质使用与安全常识

D.环境保护与物质使用

4.现有H2S、S、M、SO3,四种物质,是按硫元素的化合价由低到高排列的,其中M这种物质的化学式可以是 ( )
A.H2SO3 B.H2SO
5.分类的方法在化学学习中非常需要。现对 ①纯碱 ②生石灰 ③甲烷 ④烧碱 ⑤酒精⑥镁 ⑦金刚石 ⑧干冰 ⑨醋酸 ⑩维生素C等物质进行分类,不正确的是 ( )
A.属于有机物的有③⑤⑨⑩ B.属于氧化物的有②⑧
C.属于碱的有①④ D.属于单质的有⑥⑦
6.烧杯中盛有X溶液,逐滴加入(或通入)Y物质,烧杯内液体的pH变化如图所示。则符合该变化的一组物质是 ( )

X
Y
A
NaOH溶液
稀HCl(过量)
B
稀H2SO4
BaCl2溶液(少量)
C
Ca(OH)2
CO2(适量)
D
稀H2SO4
H2O
7.过氧化氢(H2O2)是一种无色粘稠液体,易分辩为水和氧气,常用作氧化剂、漂白剂和消毒剂,为了贮存、运输、使用的方便,工业上将过氧化氢转化为固态的过碳酸钠晶体(2Na2CO3?3H2O2),该晶体具有碳酸钠和过氧化氢的双重性质。接触下列物质不会使过碳酸钠失效的是 ( )
A.二氧化锰 B.硫酸铜 C.盐酸 D.氯化钠
8.下列物质的溶液长期放置在空气中,溶液质量因发生化学变化而减少的是 ( )
A.浓盐酸 B.石灰水 C.氯化钾 D.烧碱
9. Al2O3+2Fe这一反应生成液态铁进行焊接。下列说法不正确的是( )
Al2O3+2Fe这一反应生成液态铁进行焊接。下列说法不正确的是( )
A.Al2O3为氧化物 B.Fe2O3发生了氧化反应
C.该反应为置换反应 D.该反应放出大量热
10.用括号中的试剂除去下列物质中所含杂质,所用药品错误的是 ( )
A.NaOH溶液中混有Na2CO3(石灰水)
B.NaCl溶液中混有Na2SO4(BaCl2溶液)
C.KCl溶液中混有K2CO3(稀硫酸)
D.CO中混宥CO2(NaOH)溶液
二、填空与简答题(本题包括3小题。共l2分)
11.(5分)工业生产,人类生活与化学有着密切的关系,请你用C、H、O、Cl、Na、Ca六种元素中的一种或几种(可重复使用),写出符合下列要求的物质的化学式:
(1)为了减少燃煤造成的空气污染,大力推广使用天然气,它的主要成分是___________;
(2)一种有毒气体,可用于铁的冶炼___________;
(3)在焊接工艺等工业生产中,常用于除去金属表面的锈___________;
(4)生活中常用于调味和腌溃蔬菜,鱼、肉等食物的盐___________;
(5)在农业上常用来改良酸性土壤的一种碱___________。
12.(3分)下图是A、B、C三种物质的溶解度随温度变化的曲线图,根据图回答:

(1)S表示物质的溶解度,在___________℃时,SA=SB>SC;
(2)把t
(3)t
13.(4分)A、B、C、D、E、F、G为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,下图是它们之间的相互转化关系。请回答

(1)写出A物质的化学式:______________________________________________;
(2)写出反应②的化学方程式:__________________________________________;
(3)写出反应③中生成红色固体的化学方程式:____________________________;
(4)在物质转化中产生无色气体G的原因是_________________________________。
三、实验探究题(本题包括2小题。共l2分)
14.(5分)下图是制取并收集干燥二氧化碳气体的装置,试回答下列问题:
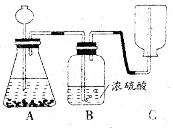
(1)请指出图中的一处错误_________________________________;
(2)在装置A中,若用浓盐酸和大理石反应制取CO2气体,并将制得的CO2通入澄清石灰水中,较长时间一直未观察到石灰水变浑浊,其原因可能是生成的CO2气体中混有___________气体(填物质名称);
(3)收集CO2时,验满的方法是_________________________________;
(4)公共场所常用的泡沫灭火器是用硫酸铝和碳酸氢钠两种溶液反应来产生CO2的,同时还生成氢氧化铝沉淀和硫酸钠,请写出此反应的化学方程式:______________________。
15.(7分)学校实验室的废液缸中收集了学生在实验室制取CO2后残留的废液。小红同学想探究废液中溶质的成分,请你一同参与探究并回答下列问题:
【提出问题】废液中的溶质是什么?
【作出猜想】小红认为废液中的溶质只有CaCl2。
你认为还可能含有的溶质是___________ (填化学式)。
【查阅资料】CaCl2溶液星中性。
【实验与结论】①小红取少量CaCl2溶液和废液分别加入到2支试管中,并向其中分别滴加无色酚酞试液作对比实验,结果两试管中溶液均无色,于是小红认为自己的猜想是正确的。
②你认为小红的实验___________ (填“能”或“不能”)证明她的猜想,理由是_______________________________________________________。
③如果要证明你的猜想是正确的,你选择的试剂是___________,实验中可能看到的现象是____________________________________________。
【拓展与应用】①若实验证明你的猜想是正确的,想要处理废液只得到CaCl2溶液,应向废液中加入过量的___________,反应完成后过滤。
②通过以上探究,你认为实验室的废液未经处理直接倒入下水道,可能造成的危害是______________________(只写一条)。
四、计算题(共6分)
16.学习了酸和碱的知识后,小松知道了白醋的主要成分是黪泼(CH3COOH)。为了测定自醋中醋酸的质量分数,他把4%的NaOH溶液漓加到
(1)已知反应的化学方程式为:
CH3COOH+NaOH==CH3COONa+H2O,该反应的基本类型是___________。CH3COOH的相对分子质量是________________。
(2)请计算白醋中醋酸的质量分数。