2007-2008学年度莱州市第一学期初三期末考试
化学试题
(考试时间:90分钟,满分:100分)
可能用到的相对原子质量:H―1 C―12 O―16
一、选择题(1~10小题每题只有一个正确答案,每题1分;11~20小题每题有一个或两个正确答案,少选得1分,错选不得分。每小题2分。共30分。请把正确答案序号填到卷首答题表中。)
1.化学――人类进步的关键。下列一般不属于化学研究范围的是
A.开发新材料 B.合成新物质
C.宏观物体的运动规律 D.寻找新能源
2.下列过程中不包含化学变化的是
A.纸张燃烧 B.水壶内水沸腾
C.葡萄酒变酸 D.白菜腐烂
3.汽车安全气囊内的物质在汽车受到碰撞时会迅速生成一种空气里含量最多的气体,从而保护驾乘人员减少损伤,该种气体是
A.氧气 B.水蒸气 C.二氧化碳 D.氮气
4.学习生活中接触到的下列物品是由天然材料制成的是
A.木质课桌 B.塑料三角板 C.橡皮 D.中性笔芯
5.厨房常用的下列物质与水混合,不能形成溶液的是
A.食盐 B.植物油 C.白糖 D.白酒
6.“雪碧饮料”、“生理盐水”和“矿泉水”均属于
A.化合物 B.纯净物 C.混合物 D.无法判断
7.夏天从冰箱中拿出一瓶饮料放在空气中,外壁会潮湿,这说明空气中含有
A.二氧化硫 B.稀有气体 C.二氧化碳 D.水蒸气
8.薯片等易碎食品宜采用充气袋包装,下列气体中最不适宜充入的是
A.O2 B.N
9.用托盘天平称量一个小烧杯的质量,记录结果正确的是
A.
10.高铁酸钠(Na2FeO4)是一种高效水处理剂,其中铁元素的化合价为
A. +1 B.+
11.下列错误的实验操作中,可能引起安全事故的是
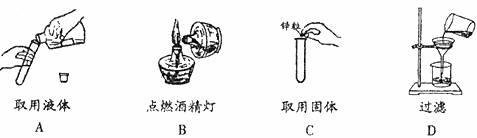
12.某无毒气体的密度约是空气密度的5/9,且极难溶于水,那么收集该气体可用的方法是
①向上排空气法 ②向下排空气法 ③排水法
A.① B.② C.③ D.①②③均可
13.下列有关氧气的说法中正确的是
A.工业上制氧气是利用了氧气的物理性质
B.氧气具有可燃性
C.物质跟氧气发生反应都是化合反应
D.相同情况下,氧气的密度比空气略大
14.有关溶液的叙述正确的是
A.溶液一定是无色透明的
B.溶液一定能导电
D.溶液不一定只由一种溶质和一种溶剂组成
C.均一、稳定的液体一定是溶液
15.如下图所示,导管内有一段红墨水,试管中盛有适量的冷水,容器的气密性良好。现往试管中加入下列某种物质,红墨水不会移动的是
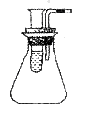
A.氯化钠 B.蔗糖 C.硝酸铵 D.氢氧化钠固体
16.要将
A.加人
C.蒸发掉
17.下图形象地表示了水在常温下的挥发和受热加速蒸发的情况,由此分析下列说法错误的是
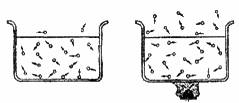
A.分子总是不断地运动
B.在受热的情况下,分子能量增大,运动速度加快
C.只要温度相同,任何物质的分子间间隔都是相同的
D.同一种物质在固态、液态和气态时分子间间隔是不同的
18.在进行“空气中的氧气会减少耗尽吗?”辩论中,某小组为正方(空气中的氧气会减少耗尽)。下列论点不应成为正方论据的是
A.汽车越来越多,消耗的氧气越来越多
B.有证据表明,在远古时代的原始空气中氧气含量高达30%
C.限制二氧化碳的排放是目前各国政府的重要环境政策
D.地球人口的增多,其呼吸和所用的燃料越来越多
19.维生素C(化学式为C6H8O5)主要存在于蔬菜和水果中,它能促进人体生长发育,增强人体对疾病的抵抗力。下列关于维生素C的说法中错误的是
A.维生素C的相对分子质量为176
B.维生素C是由碳元素、氢元素和氧元素组成的
C.维生素C中,C、H、O三种元素的质量之比为6┱8┱6
D.维生素C中有6个碳原子、8个氢原子、6个氧原子
20.科学家发现了新的氢微粒。这种氢微粒由3个氢原子核(只含质子)和2个电子构成。下列说法中正确的是
A.该微粒不显电性
B.该微粒比一个普通H2分子相对分子质量多
C.该微粒的组成可用H3表示
D.该微粒比一个普通H2分子多一个氢原子核
二、填空与简答题(本大题包括五个小题,共32分)
21.(5分)下列分别盛有不同物质的容器中,所盛物质属于单质的是 ,化合物的是 ,纯净物的是 ,混合物的是 ,氧化物的是 。(均填容器下的代号)
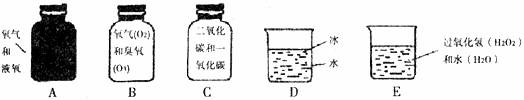
22.(8分)用化学知识解释或说明下列问题。
(1)餐具洗洁净可以洗去餐具上的油污,是因为洗洁净具有 作用。
(2)茶杯内的纱网可将茶叶与茶水分离,便于饮用。该设计利用的原理是 。
(3)膨化食品包装袋中充入氮气的目的是 。
(4)家庭养鱼的鱼缸内送气装置使用时会连续不断冒出气泡,目的是 ,这说明氧气的性质有 。
(5)酥脆的饼干在空气中敞口放置一段时间后会逐渐变软,原因是 。
(6)严寒的冬季,小河或水库里的水易结成冰,而海水却不易结冰,原因是 。
(7)不能用湿手接触电源开关或电器是因为和手干燥时相比 、 。
23.(6分)如下图所示A、B、C三种元素的粒子结构示意图依次为:

(1)当A、B为原子结构示意图时,x= ,y= 。
(2)C表示的是 的结构示意图(填“阳离子”“阴离子”或“原子”),它是一种元素(填“金属”或“非金属”);该元素与B元素形成化合物的化学式为,该化合物是由 (填“分子”、“原子”或“离子”)构成的。
24.(9分)只要你留心,生活中处处有化学。经常自己洗衣服的小静发现:
(1)用含钙、镁离子较多的硬水洗衣服时最好用 (填“肥皂”或“洗衣粉”)。
(2)在等量的水中放入等量的洗衣粉,夏天洗衣粉很快溶解了,冬天会有许多洗衣粉颗粒悬浮在水中,这说明洗衣粉的溶解速度与水温的关系是 。冬天,为加快洗衣粉的溶解,可以采取的措施是 或 。
(3)用湿手取少量的洗衣粉时感觉到手发烫,原因是洗衣粉溶解于水时扩散过程 (填“吸收”或“放出”)的热量比水合过程(填“吸收”或“放出”) 的热量 (填“多”或“少”)。
(4)洗完衣服后,为使衣服干得更快些,除脱水外,还可采取的做法是 ,其原因是 。
25.(4分)如下图所示,将一只小白鼠放在内壁涂有澄清石灰水的集气瓶中并密封,发现小白鼠仍可成活一段时间,且瓶壁逐渐变模糊。回答下列问题:

(1)小白鼠能成活一段时间的原因是 ;
(2)瓶壁变模糊的原因是 ;
(3)烧杯中导管内液面高度的变化是 ;
(4)最后瓶内剩余气体的主要成分是 。
三、实验与探究题(本大题包括个五小题,共32分)
26.(3分)实验室加热约150mL液体,应使用的仪器有铁架台(带铁圈)和 、 和 。
27.(5分)小强查阅资料得知;铝丝能在氧气中燃烧生成氧化铝,于是设计了如下图所示的装置进行实验探究,请你结合实验过程回答下列问题。
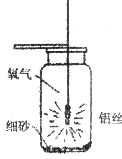
(1)集气瓶底预先铺少量沙子的目的是 ;
(2)铝丝在空气中不能被点燃,引燃铝丝的办法是 ;
(3)用正确方法引燃铝丝,伸入装有氧气的集气瓶中后,未观察到铝丝发生剧烈燃烧现象,可能的原因是 。
(4)写出铝在氧气中燃烧的文字表达式为 ,该反应的基本类型为 。
28.(8分)欲配制
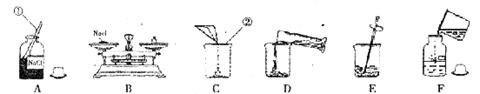
(1)写出标号仪器的名称:① ,② 。
(2)B操作中应称NaCl的质量是 g。若称量时错把氯化钠放到了右盘(
(3)所需量取水的体积为 (水的密度为lg/cm3),量筒的规格应为(填“10mL”或“50mL”)。
(4)D操作时有少量求溅出可能导致溶质质量分数 ,F操作中溶液洒落可能导致溶质质量分数 (填“偏高”、“偏低”或“无影响”)。
29.(9分)下图是实验室制取气体的部分装置,据图回答有关问题:
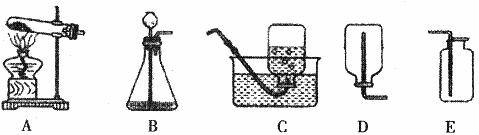
(1)用过氧化氢溶液和二氧化锰制取氧气,该反应的文字表达式 ,应选用的发生装置为 (填字母)。
(2)检验B装置气密性的方法为 。
(3)某同学观察到锥形瓶内有大量气泡时,开始用E装置收集氧气,过一段时间后用带火星的木条伸入瓶口、瓶中和瓶底,都末见木条复燃。其原因是 。
(4)小强想用加热高锰酸钾固体的方法制取并收集纯净的氧气,他应选择的装置为 (填字母)。当氧气收集满并取出集气瓶后,停止该实验的正确操作步骤是先 后 。他这样做的目的是 。
30.(7分)甲同学从课外资料得知,不少金属氧化物可做H2O2溶液分解的催化剂,那么,Fe2O3能否作为H2O2分解的催化剂呢?请你一起参与探究,并填写下列空白。
【猜想与假设】Fe2O3能作为H2O2分解的催化剂。
【实验验证】甲同学依次设计了三个实验:
实验一:取一定量的H2O2溶液于试管中,观察到有极少量气泡产生,伸入带火星的木条,没有复燃。说明H2O2溶液常温下缓慢分解。
实验二:在实验一的试管中加入WgFe2O3粉末,有大量气泡产生,然后伸入带火星的木条,木条复燃。说明 。
实验三:待反应结束后,将试管里的不溶物滤出,并洗涤干燥、称量,固体质量仍为Wg。说明 。进行过滤操作时,要用到的玻璃仪器有玻璃棒和 、 。为加快过密基速度,甲同学不断搅拌滤液,这样做是否正确,这什么? 。
【实验结论】甲同学认为,Fe2O3粉末可以作为H2O2分解的催化剂。
【反思与评价】乙同学认为要证明甲同学的结论正确,仅做这三个实验还不充分,需要再补充一个探究实验。探究 。
【拓展】下表是丙同学探究影响H2O2分解因素时所记录的部分数据,通过对数据分析,你能得出什么结论?
用足量等体积H2O2溶液制取相同体积O2所需的时间:
30%H2O2溶液
15% H2O2溶液
5% H2O2溶液
加入WgMnO2
0.2
0.8
2.0
加入WgFe2O3
7.0
9.0
16.0
四、计算题(6分)
31.(6分)下图为化学实验室中浓硫酸试剂瓶标签的部分内容,请根据标签计算。

(1)该瓶浓硫酸中含有的水和硫酸的质量分别为多少?
(2)实验室要配制