2008年5月无锡新区初中毕业升学二模试卷
化学
注意事项: ①答案全部填在答题卷上。 ②选用的相对原子质量在答题卷首。
一、单项选择(本题包括20小题,每小题1分,共20分。每小题只有l个选项符合题意)
1.下列成语或俗语涉及化学变化的是( )
A.花香四溢 B.百炼成钢 C.滴水成冰 D.积沙成塔
2.据报道:某地一名5岁的女孩子把涂改液当饮料吸食,食道被严重烧伤。经医院检测后发现,涂改液中含有苯、甲基环已烷等多种有毒物质。由此可知,涂改液是( )
A.混合物 B.纯净物 C.单质 D.化合物
3.下列安全常识不正确的是( )
A.逃离火灾现场――用湿毛巾捂住口鼻 B.在加油站附近――禁止吸烟
C.天然气等可燃性气体泄漏――严禁开关电器 D.稀释浓硫酸――将水倒入浓硫酸中
4.元素的化学性质主要取决于原子的( )
A.质子数 B.中子数 C.电子数 D.最外层电子数
5.酒精温度计中的液柱随温度的变化而升降,这主要是因为 ( )
A.分子是由原子构成 B.分子是构成物质的一种微粒
C.分子之间有间隔 D.分子保持物质化学性质
6.下列物质中,能除去铁制品表面铁锈的是( )
A.稀硫酸 B.水 C.氢氧化钠溶液 D.硫酸铜溶液
7.青色的生虾煮熟后颜色会变红。一些同学认为这种红色物质可能就像酸碱指示剂一样,遇到酸或碱会发生颜色的变化。就这些同学的“看法”而言,应属于科学探究中的( )
A.观察 B.实验 C.假设 D.做结论
8.物质的性质决定它的用途,还决定了它的保存方法。固体NaOH具有以下性质:①白色片状固体②有腐蚀性③易吸收水分而潮解④易溶于水,溶解放热⑤能与空气中的CO2反应。实验室中必须将它密封保存的原因是( )
A.①② B.①②③ C.②③④ D.③⑤
9.下列物质的名称、俗称、化学式完全一致的是( )
A.汞、水银、Ag B.氢氧化钙、石灰石、Ca(OH)2
C.氧化钙、生石灰、CaCO3 D.氢氧化钠、烧碱、NaOH
10.某微粒的结构示意图如下图所示,下列有关说法正确的是( )
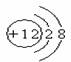
A.该微粒易失去电子 B.该微粒电子层结构属于稳定结构
C.该元素属于非金属元素 D.该元素的原子核外有10个电子
11.晓晓同学需配制
A.在托盘上垫纸称量12gNaOH固体 B.称量时发现指针向右偏,应调节游码至平衡
C.用100mL量筒量取88mL水 D.用药匙搅拌,加速NaOH溶解
12.下列说法不正确的是( )
A.自来水厂常用沉淀、过滤、吸附等方式净水 B.硬水和软水可用肥皂水来区分
C.爱护水资源可从节约用水和防止水体污染入手 D.用汽油或洗涤剂去油污的原理相同
13.亚硝酸钠(NaNO2)常被冒充食盐或被误作食盐食用,导致多起中毒事件发生。小杰同学根据下表资料及已有化学知识,设计了四种鉴别亚硝酸钠和氯化钠的方法,其中正确的是( )
项目
亚硝酸钠
氯化钠
溶解性
熔点
沸点
水溶液酸碱性
碱性
中性
①在同一块金属片上加热两种物质,先熔化者为NaNO2
②取少量分别溶于水,滴加酚酞试液,变红的是NaNO2
③分别溶于
④取少量分别溶于水,用pH试纸测定,pH大的是NaNO2
A.①②③④ B.①②④ C.①③④ D.②③④
14. 取少量X、Y、Z三种金属,分别加入到硫酸铜溶液中,发现X、Z表面出现红色物质,Y没有。再取大小形状相同的X、Z各三粒,分别加入到溶质质量分数相同的稀硫酸中,发现X表面产生气泡的速度明显比Z快。则三种金属的活动性由强到弱依次为( )
A. X>Y>Z B. Y>Z>X C. X>Z>Y D. Z>X>Y
15.“绿箱子环保计划――废弃手机及配件回收联合行动”已在全国40个重点城市中开展了近两年。下列有关废弃手机中的金属材料回收利用的说法不正确的是( )
A.可以节约金属资源 B.可以节约冶炼相关金属所消耗的能源
C.可以减少对环境的污染 D.回收废弃手机中的金属材料没有任何价值
16.医院里常用溶质分数为5%的双氧水(过氧化氢)溶液清洗受伤病人的伤口,若要配制5%的双氧水溶液
A.
17.能一次性鉴别空气、氧气和二氧化碳三瓶无色气体的方法是( )
A.分别加入澄清石灰水 B.分别将燃着的木条伸入瓶中
C.分别加入紫色石蕊试液 D.分别加入酚酞试液
18.下列说法错误的是( )
A.质子数相同的粒子不一定是同种元素的原子
B.由不同种元素组成的纯净物不一定是化合物
C.使用催化剂不一定都能加快其它物质的化学反应速率
D.有单质生成的反应不一定是置换反应
19.右上图是A、B两固体物质的溶解度曲线,分别得到的下列信息中,正确的是( )
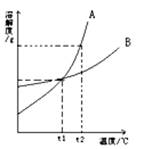
A. t
B. 与A相比,欲从B的溶液中获得B晶体,最好采用冷却结晶的方法
C. B物质的溶解度大于A物质的溶解度
D. t
20.在一密闭容器中,盛放A、B、C三种物质各
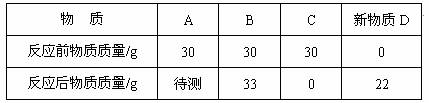
A.C物质中所含有的元素种类是A、B、D三种物质中所有元素种类之和
B.变化后待测的A质量为
C.该变化的基本反应类型是分解反应
D.A物质有可能是单质
二、不定项选择题(本题包括5小题,每小题2分,共10分。每小题有1―2个选项符合题意。按题意选对给2分;错选、多选不给分;少选且选对给1分)
21.2008年北京奥运会吉祥物――“福娃”向世界传递着友谊、和平、积极进取的精神。为儿童安全考虑,有一种“福娃”的外用材料为纯羊毛线,内充物为无毒的聚酯纤维。聚酯纤维的化学式为(COC6H4COOCH2CH2O)n 。下列说法不正确的是( )

A.羊毛属于合成纤维 B.聚脂纤维中C、H、O原子个数比为5┱4┱2
C.聚酯纤维是有机高分子化合物 D.可用燃烧的方法区分羊毛和聚酯纤维
22.分析推理是化学学习和研究中常用的思维方法,下列分析推理正确的是( )
A.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
B.有机化合物都含有碳元素,所以含有碳元素的化合物一定是有机化合物
C.燃烧都伴随着发光、放热,所以有发光、放热现象的就是燃烧
D.碱性溶液能使石蕊试液变蓝,所以能使石蕊试液变蓝的溶液呈碱性
23.下列实验现象描述错误的是( )
A.细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 B.红磷在空气中燃烧产生白雾
C.铝浸入硫酸铜溶液中有红色固体生成,溶液变蓝 D.纯碱溶液中滴入酚酞,溶液变红
24.下列各组物质的溶液,不加其它试剂就能区别的是( )
A.NaOH、HCl、CuSO4、MgSO4 B.Na2SO4、BaCl2、K2CO3、KNO3
C.NaCl、Na2CO3、KNO3、HCl D.(NH4)2SO4、H2SO4、NaOH、 MgCl2
25.将少量的生石灰加到一定质量的饱和石灰水中,溶液的温度升高,再恢复到室温(不考虑水的蒸发)。下列四位同学对变化后溶液的分析错误的是( )

三、(本题包括6小题,共28分)
26.用适当的数字和化学符号填空:水是由氢元素和氧元素组成的化合物,水中氧元素的化合价为?2价 ① 。水是地球上最重要的溶剂。正常的雨水偏酸性,这是因为它溶解了约占空气体积分数 ② 的二氧化碳而生成了 ③ 的缘故;雨水进入土壤,溶解了含有(填化肥中植物所需的一种营养元素) ④ 等元素的化肥及多种物质,利于植物的吸收。海水中溶解了许多物质,从中可提取食盐和多种化工产品,同时为海洋生物提供了营养成分。水在人体内形成溶液,输送生命活动所需的各种物质,如对维持体液恒定的pH起重要作用的钾离子和(填钠离子) ⑤ 。因此水对自然界的生命活动有着重大意义。
27.化学就在我们身边,它与我们的生活息息相关。请从“熟石灰、碳酸钙、硝酸钾、石油、盐酸、干冰、纯碱、生石灰”这八种物质中,选择适当的物质填空。
(1)人体胃液中含有的酸是 ① ;(2)农田施用的复合肥是 ② ;
(3)有“工业的血液”美誉的是 ③ ;(4)可做补钙剂的盐是 ④ ;
(5)常用来改良酸性土壤的碱是 ⑤ ;(6)常用作制冷剂的氧化物是 ⑥ 。
28.在C、H、O、Na、Cl五种元素中,选择适当元素,组成符合下列要求的物质,将其化学式填入空格中。
(1)食品中常用的一种甜味剂 ① ;(2)煤矿坑道常含有的可燃性气体 ② ;
(3)炼铁时具有还原性的气态氧化物 ③ ;(4)发酵粉的主要成分之一 ④ 。
29.某学校九年级同学到湖边野炊:负责烧饭的同学引燃枯枝后,迅速往灶里塞满枯枝,结果燃烧不旺,并产生了很多浓烟,原因是 ① ;活动结束后,应及时把火熄灭,可采用的方法是 ② ;活动中有位女同学不小心被黄蜂蛰了(黄蜂毒液呈碱性)。下列物质可用于减轻疼痛的是(填字母) ③ 。
A、食醋 B、食盐水 C、鸡蛋清(pH=8) D、肥皂水(pH=9) E、苹果汁(pH=3)
30. 化学与人体健康密切相关:
(1)市场有“铁强化酱油”、“含氟牙膏”、“高钙牛奶”、“加碘食盐”等商品,这里的铁、氟、钙、碘应理解为 ① (填编号)①元素②原子③分子④氧化物
(2)妈妈每天为小明准备的食品有:奶类、豆类、鱼肉类、水果、蔬菜、面食等,这些食品中含有 ② 、 ③ 等人体所需营养素(只需填写两种即可),可以保证营养均衡。
(3)同学们喜爱喝的酸奶,其配料表部分为:①纯净水②鲜牛奶③白砂糖④柠檬酸⑤食用香精⑥维生素E等多种维生素。其中能为人体提供能量的是 ④ (填编号)。
31.用化学方程式表示下列除杂过程(括号内为杂质),并在括号里注明反应的基本类型:
(1)铜粉(铁粉) ① ,( ② )反应
(2)一氧化碳气体(二氧化碳) ③ ;
(3)二氧化碳气体(一氧化碳) ④ ;
(4)氯化钙(碳酸钙) ⑤ ,( ⑥ )反应
四、(本题包括3小题,共13分)
32.有A、B、C、D四种元素,A元素组成的一种单质是自然界最硬的物质,B元素是空气中含量最多的元素,C元素的原子核外有二个电子层,最外层上有6个电子,D元素形成的阳离子是不同的酸溶液中都含有的离子。试回答:(1)A元素形成的这种单质的名称 ① ;B元素的符号 ② ;C属于 ③ 元素(填“金属”或“非金属”);D离子的符号 ④ 。(2)由B、C、D三种元素组成化合物的化学式: ⑤ 。
33.图示是北京奥运会火炬“祥云”的不同侧面示意图。

(1)火炬的外壳主要采用轻薄高品质的铝合金材料。铝是一种重要的轻金属,
自然界中铝元素常以氧化铝、硫化铝(Al2S3)等形式存在。则在Al2S3中,
铝元素的化合价为 ① 。
(2)“祥云”燃烧系统内装燃料是丙烷(C3H8),丙烷在空气中完全燃烧的
化学方程式为 ② ;作为燃料,丙烷与煤相比,其优点是 ③ 。
34. A、B、C、D、E、F都是初中化学常见的物质,其中B是常用于光合作用和灭火的气体,C是覆盖地球表面71%的物质。它们之间的关系如下图所示。(图中“―”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系。)
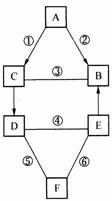
(1)B的化学式为 ① 。
(2)已知反应①、②、③的基本反应类型相同。反应①的化学方程式为 ② ,基本反应类型为 ③ 。
(3)已知反应④、⑤、⑥中,一个有沉淀生成,另一个有气体生成,还有一个没有明显现象。B、E不含相同元素,D、F只含一种相同元素。反应④的化学方程式为 ④ ,反应⑥的化学方程式为 ⑤ 。
五、(本题包括3小题,共21分)
35.请回答下列问题:(在下列(1)、(2)两小题中任选一题回答,若两小题都回答,则以第(1)小题的答案评定分数。)
(1)找出物质之间的相互联系和区别,从中发现规律,这是我们学好化学的一种基本方法。下面是五种含氮物质的化学式:①N2②NH3③N2O4④N2O⑤NaNO3
请回答:五种物质中氮元素的化合价由低到高的顺序是(填序号) ① ;仔细观察这五种物质,你还能发现其它规律,请你再写出一个,并排列成序(排序用序号表示) ② 。
(2)元素周期表是学习和研究化学的重要工具。请说说你从元素周期表上所获得的知识与信息(至少写两点)。
36. 化学是一门以实验为基础的科学,化学所取得的丰硕成果,是与实验的重要作用分不开的。结合下列实验装置图回答问题:
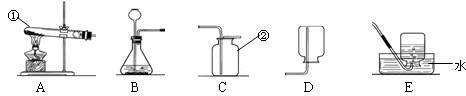
(1)写出指定仪器的名称:① ① ② ②
(2)下边四种途径都可以得到氧气:
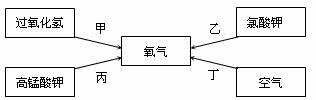
写出实验室中通过甲、乙两种途径制取氧气的化学方程式:
甲 ③ ;乙 ④ 。
化学实验的绿色化就是以绿色化学的理念和原则来指导实验工作。从实现原料和反应过程的绿色化考虑,你认为在中学化学实验室中,甲、乙、丙三种制取氧气的途径中, ⑤ (填“甲”、“乙”或“丙”)途径更体现化学实验的绿色化追求。
(3)实验室用高锰酸钾制取并收集氧气时,可选用的装置组合是 ⑥ (填字母代号),用排水法收集氧气完毕后,停止加热时的操作顺序是先 ⑦ ,然后 ⑧ ,以防止水倒吸进入热的试管中,造成试管破裂。
(4)实验室制取二氧化碳时,可选用的发生装置是 ⑨ (填字母代号),收集二氧化碳常用C装置,而不选用D或E装置,试从二氧化碳性质的角度来分析其原因 ⑩ 。
37.小明家购买了一瓶白醋,标签上注明醋酸的质量分数≥5%。小明想,这瓶白醋中醋酸的含量是否与标签的标注相符?请你与小明一起,用有关化学知识,定量测定白醋中醋酸的含量。
【提出问题】这瓶白醋中醋酸的含量是否与标签的标注相符?
【实验原理】
(1)醋酸属于 ① (“有机”或“无机”)酸,能与 ② (填物质类别)发生中和反应。
(2)用已知浓度的氢氧化钠溶液和醋酸反应,反应的化学方程式为:
CH3COOH + NaOH = CH3COONa + H2O。
(3)在混合溶液中,当醋酸和氢氧化钠完全中和时,再增加1滴氢氧化钠溶液,溶液就呈碱性,而1滴氢氧化钠溶液约为0.05 mL,对测定结果的影响很小,可忽略不计。
【实验步骤】
(1)用 ③ 取12.0 mL白醋(密度近似为
(2)量取45.0 mL溶质质量分数为1.0%的氢氧化钠溶液(密度近似为
【交流反思】
(1)在实验步骤(1)中,加适量水稀释白醋,对实验结果 ④ (“有”或“无”)影响?为什么? ⑤ 。
(2)在实验步骤(2)中,小明如何确定醋酸和氢氧化钠已完全中和?
实验操作
实验现象
结论
⑥
⑦
⑧
【解释与结论】
根据实验数据,通过计算,判断这瓶白醋中醋酸的含量 ⑨ (“是”或“否”)与标签的标注相符。
六、(本题包括2小题,共8分)
38. 去年发生在某市的假药案已致使多人死亡。经查实,该假药中含有损害人体肾脏的成分“二甘醇”(化学式为C4H10O3),“二甘醇”在人体内可发生如下反 C4Hl0O3+4O2=2X+3H2O,而导致人中毒。请填空:
(1)一个“二甘醇”分子中共有 ① 个原子。
(2)x的化学式为 ② 。
(3)“二甘醇”中各种元素的质量比为 ③ 。
39. 家里蒸馒头用的纯碱中含有少量的氯化钠,课外探究小组的同学欲测定纯碱中碳酸钠的含量。他们取该纯碱样品
(1)纯碱样品中碳酸钠的质量;
(2)反应后所得滤液中溶质的质量分数。