2008年4月曲阜市九年级复习质量监测
化学试题
注意事项:
1.本试题分第Ⅰ卷和第Ⅱ卷两部分,第Ⅰ卷为选择题,l6分;第Ⅱ卷为非选择题,34分;共50分。物理、化学、生物三科考试时间共150分钟。
2.答第Ⅱ卷时,将密封线内的项目填写清楚,用钢笔或圆珠笔直接答在试卷上。
可能用到的相对原子质量:H一
第Ⅰ卷(选择题 共l6分)
一、选择题(下列各题只有1个正确选项。其中1~4小题各1分,5~10小题各2分,本大题共16分)
1.日常生活中的下列变化,只发生了物理变化的是( )
A.灯泡通电后发亮 B.面包发霉 C.菜刀生锈 D.蔬菜腐烂
2.下列做法或认识科学的是( )
A.厨房煤气泄漏,立即打开排气扇电源
B.煤气中毒应大量喝牛奶
C.淀粉没有甜味,因此不属于糖类
D.垃圾经分类回收处理可转化为资源
3.水是人类生活不可缺少的物质。下列有关水的叙述不正确的是( )
A.水是氢元素和氧元素组成的氧化物
B.用肥皂水可以区分硬水和软水
C.氢气燃烧生成水和电解水的基本反应类型相同
D.净化水的常用方法有吸附、沉淀、过滤和蒸馏
4.下列对一些事实的解释合理的是( )
A.铁生锈后质量变大,是因为该反应不遵循质量守恒定律
B.洗涤剂能除去油污,是因为它具有乳化作用
C.浓硫酸和浓盐酸敞口放置后溶质质量分数均变小,是因为它们都有吸水性
D.
5.下列符号中,既能表示―个原子,又能表示一种元素,还能表示一种物质的是( )
A.He B.O
6.下列实验能利用厨房中的食盐、食醋、纯碱三种物质做成功的是( )
①检验自来水中是否含有氯离子;②检验鸡蛋壳能否溶于酸;③除去热水瓶中的水垢。
A.①②③ B.①② C.①③ D.②③
7.为了检验长期暴露在空气中的氢氧化钠固体是否变质,下列方法正确的是( )
A.放入水中,看是否全部溶解 B.滴加稀盐酸,看是否有气泡产生
C.滴加酚酞,看是否变色 D.用手接触,看是否有滑腻感
8.下表是
主要污染物
污染指数API
等级
可吸入颗粒物
208
Ⅳ
M40
1
一氢化氟
231
空气污染级别
Ⅳ
空气质量状况
中度污染
A.这天污染最严重的污染物是可吸入颗粒物
B.M是引起酸雨的主要物质
C.M是一氧化碳
D.M主要是由燃烧含硫燃料产生的
9.某化学兴趣小组为测定Fe、Cu、Ag三种金属的活动顺序,设计了四种方案,你认为不可行的是( )
A.在两支试管中各装入少许CuSO4溶液,分别加入铁片和银片
B.在两支试管中各装入少许FeSO4溶液,分别加入铜片和银片
C.向盛有FeSO4溶液和AgNO3溶液的两支试管分别加入铜片
D.向盛有稀硫酸的两支试管中,分别加人铁片和铜片,再向盛AgNO3溶液的试管中加入铜片。
10.下列图像能正确反映所对应叙述关系的是( )
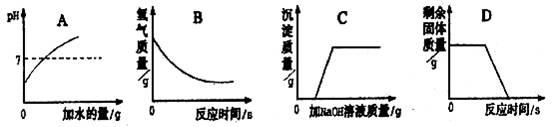
A.向pH=3的溶液中不断加水
B.一定量的稀硫酸与锌粒反应
C.向H2SO4和CuSO4混合液中滴加NaOH溶液
D.煅烧一定质量的石灰石
第Ⅱ卷(非选择题 共34分)
二、填空与简答(共17分)
11.(2分)用化学符号填空
(1)两个氮分子 (2)+5价的磷元素
(3)3个氢氧根离子
(4)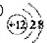
12.(4分)请判断下面四个观点是否正确,如不正确,请举例说明(用化学方程式表示)
(1)凡有化合物生成的反应都是化合反应。
(2)分解反应一定有单质生成
(3)有单质和化合物生成的反应一定是置换反应
(4)有盐和水生成的反应一定是中和反应
13.(3分)为防止煤气泄漏,使人中毒,常在煤气中加入少量有特殊气味的乙硫醇(C2H5SH)
(1)乙硫醇由 元素组成,其中各元素的质量比为
(2)乙硫醇在煤气燃烧过程中也可以充分燃烧,其化学方程式为
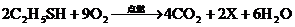 ,则X的化学式为
。
,则X的化学式为
。
14.(3分)下图是a、b两种固体物质的溶解度曲线图,据图回答:

(1)t
(2)t
(3)从图中你还可获得哪些信息(任意写一条)
15.(5分)有一包固体粉末可能由CaCO3、Na2SO4、Na2CO3、CuSO4、BaCl2中的一种或几种组成,为确定其组成,现做如下实验:
(1)将此固体加到水中,得到白色沉淀,上层清液为无色。由此判断,该粉末一定不含有
(2)若向上述白色沉淀中滴加足量的稀硝酸,沉淀部分溶解。由不溶解的沉淀可判断出,该粉末中一定含有
(3)该固体粉末中还含有的物质可能有哪几种情况(每种情况用化学式表示)
① ② ③
三、实验与探究(共11分)
16.(1)(3分)用下图回答
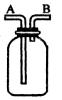
①洗气:除去CO2中的水蒸气,装置内应盛的物质是 气体应从 端通入。
②检验:证明CO中含有CO2,装置里应感 ,要除去CO2,最好盛 。
③贮气:排空气法收集H2时,气体从 端通入,若要用水将装置中的O2排出进行实验,水应以 端通入
(2)(8分)某化学兴趣小组知道实验室也可用氯酸钾受热分解制取氧气,常使用MnO2作催化剂,该反应的化学方程式为:2KClO3 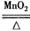 KCl+3O2↑。
KCl+3O2↑。
很想探究其他一些物质(如Fe2O3)是否也可以做KClO3分解的催化剂。请参与他们的探究过程,并填空。
①[提出问题]Fe2O3能不能做KClO3分解的催化剂?
②[猜想]Fe2O3能做KClO3分解的催化剂
③[实验验证]
实验步骤
实验现象
实验结论
实验一
取少量KClO3固体于试管中加热至溶化后,用带火星的木条伸入管口
加热KClO3需要很高的温度才能缓慢分解,产生O2
实验二
取少量Fe2O3粉末于试管
中,加热较长时间后,用带
火星的木条伸入管口
木条不复燃
实验三
①取少量KClO3固体于试管中,稍稍加热片刻,用带火星的木条伸入管口
木条不复燃
把试管移开火焰,迅速撒入Fe2O3粉末,并用带火星的木条伸人管口
木条复燃
④[讨论与思考]经过讨论,有的同学认为只有上述几个实验证据还不能证明Fe2O3是KClO3分解的催化剂,需要补充一个探究实验,即将探究Fe2O3 。
(实验步骤)a.准确称量Fe2O3的质量。b.完成实验三。c.等试管冷却后,应进行的操作有 、 、洗涤、 、称量。d.对比反应前后Fe2O3的质量。
(讨论)多数同学认为,通过实验证明Fe2O3可以做KClO3分解的催化剂。但个别同学认为:要证明猜想,上述实验还不够,还需要增加一个探究实验,即探究Fe2O3的
.
四、计算与应用(共6分)
18.(2分)有一不纯硝酸铵(NH4NO3)氮肥样品,经分析测定,该样品中含氮元素的质量分数为31.5%,则该样品中含硝酸铵的质量分数是 。
19.(4分)某学校的学习小组对当地的石灰石矿区进行调查,测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品
序号
加入稀盐酸的质量/g
剩余固体的质量/g
第1次
20
11
第2次
20
6
第3次
20
2.8
第4次
20
n
(1)上表中n有数值是 。
(2)样品中碳酸钙的质量分数是 。
(3)求盐酸中溶质的质量分数。