2007-2008学年度淄博市沂源县第一学期初三年级期末考试
化学试题
(时间:90分钟 满分:120分)
友情提示:慎重思考 认真书写 规范答卷
一、单项选择题(本题包括20个小题,共60分;将每个小题的正确答案字母序号填在下表相应的题号下)
1.世界是物质的,物质又是不断运动变化的。下列变化属于化学变化的是
A.玻璃破碎 B.蜡烛受热熔化 C.汽油挥发 D.木柴燃烧
2.学生具备基本的化学实验技能是进行科学探究活动的基础和保证。下列实验操作正确的是
A.倾倒液体,标签对着手心
B.称量固体,固体放在托盘天平的右盘上
C.量取液体,俯视读数
D.给试管内液体加热,试管口对着别人
3.下列图示表示的是四种实验基本操作,其中不正确的是

4.“墙角数枝梅,凌寒独自开,遥知不是雪,为有暗香来”(王安石《梅花》)。诗人在远处就能闻到梅花香味的原因是
A.分子很小 B.分子是可分的
C.分子之间有间隔 D.分子在不断地运动
5.下图是“水电解实验”的简易装置图,根据图结合所学知识,你认为下列说法中不正确的是
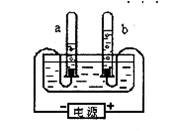
A.水是由氢元素和氧元素组成的
B.试管b中的气体可用带火星的木条检验
C.试管a中所得气体是氢气
D.试管a、b中所得气体的质量比约为2┱1
6.最近俄罗斯科学家利用第72号元素铪和74号元素钨,精确测定出月球至少比地球早700万年形成。铪和钨两种元素原子的本质不同是
A.质子数 B.中子数 C.电子数 D.最外层电子数
7.关于相对原子质量,下列说法正确的是
A.相对原子质量就是原子质量
B.由于相对原子质量数值比较小,使用不方便,所以采用相对原子质量
C.相对原子质量是原子质量与C-12原子质量的比值
D.碳原子相对原子质量是
8.铀-235是制造原子弹的一种原料。这种铀原子的相对原子质量为235,中子数为143,则铀原子的核外电子数是
A.235 B.92 C.143 D.378
9.元素周期表是学习化学的重要工具,下图是元素周期表中的一格,下面是从该图中获取的信息,其中正确的是

A.该元素的原子序数为52
B.该元素属于非金属元素
C.该元素在地壳中的含量为52.00%
D.该元素的原子核外有24个电子
10.下面是四个家庭小实验.其中不能制得溶液的是

11.下列关于溶液的叙述正确的是
C.溶液各部分的性质、质量分数都相同 D.溶液中只有一种溶质
A.凡是均一、稳定、透明的液体就是溶液 B.溶液都是无色的
12.在严寒的冬季,水易结冰,而海水却不易结冰,这是因为
A.海水的温度比水的温度低 B.海水的凝固点比水的凝固点低
C.海水的导电性比水的导电性强 D.海水的密度比水的密度大
13.对于“10%的食盐溶液”的含义,解释不正确的是
A.
B.食盐溶液中溶质和溶剂的质量比是1┱9
C.将
D.
14.酥脆的饼干在空气中逐渐变软,这说明空气中含有
A.氧气 B.稀有气体 C.二氧化碳 D.水蒸气
15.我们每时每刻都离不开空气,空气成分的微小变化都会直接影响人类的生存,你关注每天的空气质量报告吗?在空气质量报告中一般不涉及
A.二氧化硫 B.二氧化碳
C.氮氧化合物(NOx) D.可吸入颗粒物(TSP)
16.研究物质时,常常先把物质进行分类。下列物质中属于化合物的是
A.氢气(H2) B.二氧化碳(C02) C.蔗糖水 D.碘酒
17.以下是空气污染指数与质量级别、质量状况的对应关系:
空气污染指数
0~50
51~100
101~200
201~300
>300
空气质量状况
优
良
轻度污染
中度污染
重度污染
空气质量级别
Ⅰ
Ⅱ
Ⅲ
Ⅳ
Ⅴ
A.Ⅰ级 优 B.Ⅱ级 良
C.Ⅲ级 轻度污染 D.Ⅴ级 重度污染
18.某化学小组用如下图所示的装置测定空气中氧气的含量,硬质玻璃管内装有细铜丝,且两个注射器组成的密闭系统内留有30mL室温下的空气。对该实验的认识不正确的是
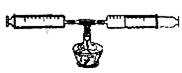
A.若实验很成功,出现的现象是细铜丝由紫红色变为黑色
B.若实验很成功,冷却后,密闭容器内气体的体积约为24mL
C.该实验不能证明空气是混合物
D.加热过程中,交替缓慢推动两注射器的目的是使空气中的氧气与铜充分反应
19.下列说法中正确的是
A.混合物中各种成分不能保持着原来的性质
B.稀有气体不能与其它任何物质发生化学反应
C.氮气可用作食品包装时防腐剂,因为氮气化学性质比较稳定
D.有一种元素组成的物质叫单质
20.下列有关分子、原子、离子的叙述中,正确的是
A.分子是保持物质性质的最小粒子
B.原子是最小的粒子,不能再分
C.分子、原子、离子都是不断运动的粒子
D.分子、厦子、离子都是显中性的粒子
二、理解与应用(本题包括6个小题,共31分)
21.(5分)通过探究物质构成的奥秘,我们知道,物质是由原子等粒子构成的。请在下图方框中填写粒子名称,表示各种粒子是怎样构成物质的。

22.(6分)某元素原子结构示意图如下图所示:

该元素原子核内有 个质子,核外由 层电子层,最外电子层上有 个电子,在化学反应中容易 个电子,达到稳定结构,该元素属于(填“金属”或“非金属”) 元素,该元素的离子结构示意图是 。
23.(7分)(用化学符号填空)地壳中含量位于前两位的元素是 、 ,含量最多的金属元素是 ;空气中含量最多的元素是 ;最原始的元素是 ;构成氯化钠的离子是 、 。
24.(2分)仔细观察下图,写出从图中获得的信息。

(1) ;
(2) 。
25.(3分)某些物质溶于水后,形成的水溶液与水相比,某些性质会改变的。这一现象常为人们在日常生活、生产中利用,例如寒冷的冬天,一场大雪过后,公路上积雪覆盖,为防止下坡时路滑。可向积雪上洒些少量 ;防止冬天汽车的水箱中水结冰,常在水箱中加入少量 等物质;做水的电解实验时,在水中常加入一些稀硫酸,增强水的 性。
26.(8分)无土栽培是一种在营养液中培育植物的农业高新技术,有良好的发展前景。某课外实验小组要配制
(1)需要硝酸钾 g,需要水 mL。
(2)配制硝酸钾溶液一般要经过 、 、 和 等步骤;
现有下列仪器:①托盘天平②胶头滴管③烧杯④量筒⑤漏斗⑥玻璃棒⑦酒精灯,其中用于配制此硝酸钾溶液的是(填序号) 。
(3)若在量取水时仰视凹液面最低处,其它操作正确,则配制得溶液中溶质的质量分数(“=”或“?”或“?” 5%。
三、实验与探究(本题包括2个小题,共19分)
27.(11分)某化学兴趣小组在学习溶液这一部分时,对“物质溶解时溶液的温度的变化”进行如下探究学习:
【提出问题】化学反应过程中伴随着能量变化,那么物质的溶解是否也伴随着能量的变化呢?
【设计并进行实验】
实验一:取一个小烧杯,放在一块刨光的木板上,木板上加一些水。然后在烧杯中注入100mL水,再加入
实验二:取一个小烧杯,用熔化的蜡烛粘结在一块小木板上,当粘结好后,在烧杯中加入100mL水,再慢慢地注入40mL浓硫酸,并且边注入边用玻璃棒搅动,发现烧杯底下的蜡被熔化,拿起烧杯时,木板就掉下来了。
【实验结论】
(1)“实验一”的现象说明了 ;
(2)“实验二”的现象说明了 ;
(3)结合上述“两个实验”的现象,你能得出什么结论?
【交流反思】
(1)“实验一”中为了加快氯化铵迅速溶解,你可以采用的方法是:
① ;② 。
(2)有没有物质溶解在水中,溶液的温度不变呢?若有,请你举出一例: ,并设计一个实验证明。 。
【实践应用】
(1)请你解释为什么葡萄糖粉放在嘴里,在甜丝丝的同时,还有一种清凉的感觉? 。
(2)市场上有一种罐装饮料,在饮料罐的夹层中分别装入一种固体物质和水,饮用前摇动罐头使它们混合,罐内饮料温度就会降低(俗称“摇摇冰”),则固体物质是(填字母序号) 。
A.氢氧化钠 B.硝酸铵 C.食盐 D.蔗糖
28.(8分)人们为了揭示原子结构的奥秘,经历了漫长的探究过程。
1808年,英国科学家道尔顿提出了原子论.他认为物质是由原子直接构成的:原子是一个实心球体,不可再分割;同一类原子性质相同;不同的原子以简单的整数比相结合。
1897年,英国科学家汤姆生发现原子中存在电子。1904年汤姆生提出了一个被称为“西瓜式”结构的原子结构模型,电子就像“西瓜子”一样镶嵌在带正电的“西瓜瓤”中。电子的发现使人们认识到原子是由微小的粒子构成的。
1911年,英国科学家卢瑟福进行了下面的实验。他们用一束带正电的、质量比电子大得多的高速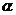 粒子轰击金箔时,发现:①大多数
粒子轰击金箔时,发现:①大多数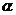 粒子能穿过金箔且不改变原来的运动方向; ②一小部分
粒子能穿过金箔且不改变原来的运动方向; ②一小部分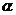 粒子改变原来的运动方向;③极少数
粒子改变原来的运动方向;③极少数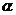 粒子被反弹了回来。据此他提出了带核的原子结构模型:原子是由原子核和核外电子构成的。……
粒子被反弹了回来。据此他提出了带核的原子结构模型:原子是由原子核和核外电子构成的。……
根据以上材料,请回答下列问题:
(1)道尔顿提出了原子论,汤姆生发现了原子中的电子,这在当时是件很了不起的事,但由于受到那时科学技术水平的限制,他们的理论中存在一些缺陷甚至错误,按照你学的原子结构的理论,你认为道尔顿的原子论存在的错误或缺陷是 、 、 、 、 。
(2)请你根据对原子结构的认识,分析出现上述卢瑟福实验现象的原因:
现象①: ;
现象②: ;
现象③: 。
(3)通过人类认识原子结构的历史,你对科学的发展有哪些感想? 。
四、分析与计算(本题包括2个小题,共10分)
29.(2分)每天补充适量的维生素C,有利用提高人体免疫力。某维生素C泡腾片,每片含
30.(8分)汽车、电动车一般要使用铅酸蓄电池。某铅酸蓄电池用的酸溶液是溶质质量分数为28的稀硫酸,若用质量分数为98%的浓硫酸100g配制该稀硫酸时,配得稀硫酸的质量是多少克?需要蒸馏水多少克?