2006-2007学年日照市莒县中考模拟考试(一)
化学试卷
(时间:45分钟 分值:45分)
1、可能用到的相对原子质量:
H 1; C l2; N l4; O l6; K 39;Cl 35.5 Mg 24;Fe 56;Cu 64.
2、请把第Ⅰ卷试题答案填写在第Ⅱ卷答题卡中
第Ⅰ卷(选择题,共16分)
一、选择题:(本题包括l―8小题,每小题2分,共16分。在每小题给出的四个选项中,只有一项是符合题目要求的。)
1、下列变化中,属于物理变化,且对其解释正确的是( )
A.二氧化碳气体制成干冰体积变小,是因为二氧化碳分子变小
B.水结成冰体积变大,是因为水的密度比冰的大
C.碳酸钠晶体在干燥空气里变成粉末.是因为此时它易失去结晶水
D.活性炭吸附有毒气体,是因为活性炭与有毒气体发生化学反应
2、下列各组物质中,按单质、化合物、混合物的顺序排列的是( )
A.水银、干冰、尿素 B.蒸馏水、自来水、矿泉水
C.金刚石、生石灰、石油 D.乙醇、乙酸、胆矾
3.中国科学技术大学钱逸泰教授等以CCl4和金属钠为原料,在
A.金刚石属于金属单质 B.制造过程中元素种类没有变化
C.CCl4是一种化合物 D.这个反应是置换反应
4、下列关于Fe、Fe2+、Fe3+的说法中,正确的是( )
A.它们结合其他原子的个数相同 B.它们的质子数不同
C.它们的最外层电子数相同 D.它们的核外电子数不同
5、下列各组物质在水中能共存的是( )
A.NaCl、AgNO3、H2SO4 B.BaCl2、Na2CO3、KNO3
C.NaOH、FeCl3、HCI D.NaNO3、KOH、Na2SO4
6、在一个密闭容器内有四种物质,在一定条件下充分反应后,测得反应前后各物质的质量如表所示:已知X的相对分子质量为n,Q的相对分子质量为2n,下列推理正确的是( )
物 质
X
Y
Z
Q
反应前质量/g
4
10
1
21
反应后质量/g
0
12
15
待测
A、反应后Y与Z的质量之比是1:7
B、反应后生成
C、反应中Y与Q发生改变的质量之比为1:1
D、该反应的化学方程式中X与Q的化学计量数之比为2:3
7.已知在相同温度和相同压强的条件下,相同体积的任何气体都含有相同数目的分子在上述条件下,测得1体积甲气体(化学式X4)和6体积乙气体(化学式Y2)完全反应生成了4体积丙气体。则丙的化学式为( )。
A.X3Y B
XY
8.在AgNO3、Cu(NO3)2和Zn(NO3)2混合溶液中,加入一定量的铁粉,充分反应后过滤,在滤渣中加入稀盐酸.有气体产生 则下列结论正确的是( )
A.滤液中一定有Fe(NO3)3
B.滤渣只含Ag和Cu,一定无Zn
C.滤渣中一定有Ag、Cu和Fe,一定无Zn
D.滤渣中一定有Ag、Cu、Fe和Zn
第Ⅱ卷(非选择题,共34分)
二、填空与简答题(本题包括9―13小题,共11分。)
9、(2分)石油资源紧张是制约中国发展轿车工业,尤其是制约轿车进入家庭的重要因素。为此.我国开始推广“车用乙醇汽油”,即在汽油中加少量乙醇.写出乙醇完全燃烧的化学方程式 车用乙醇汽油的推广还有 优点。
10.(3分) 已知+3价铁盐与铁粉在溶液中能发生化合反应,生成亚铁盐.现往生锈的铁粉中加入稀盐酸,过一会儿有气泡产生,反应后铁粉有剩余,最终得到一种浅绿色溶液.写出整个实验过程中所发生的有关反应的化学方程式。
11.(4分)有一种气体,可能由H2、CO、CO2和HCl中的一种或几种组成,将此气体通入澄清石灰水中,未见浑浊,但气体总体积明显减少;再将剩余的气体干燥后在氧气中燃烧,燃烧产物能使无水硫酸铜变蓝。则原气体可能的组成有:
12.(2分)有一混合溶液是由稀硝酸、碳酸钾、稀硫酸、氯化铜四种物质中的两种混合而成。向该混合溶液中滴入氢氧化钡溶液,产生沉淀的质量与加入氢氧化钡溶液体积的关系如图。 该混合物是由 和 组成。

三、实验题(本题包括2小题,共l2分)
13.(3分)我国著名化学家侯德榜发明的联合制碱法的主要原理是:将足量CO2通入溶有氨气的水中,生成NH4HCO3(碳酸氢铵)溶液。然后加入食盐充分搅拌,两者发生复分解反应.由于碳酸氯钠的溶解度很小,便呈晶体析出,将析出的碳酸氢钠滤出后加热制得纯碱,又生成二氧化碳和水,回收利用。请写出上述原理的三个化学方程式:
① ;② ;
③ 。
14.(9分)“有其他物质生成”是判断物质发生化学变化的依据。在探究物质之间能否发生化学反应时,我们常常根据反应伴随的现象来判断。以下是某同学在探究二氧化碳和氢氧化钠是否发生化学反应时设计的四种实验装置:
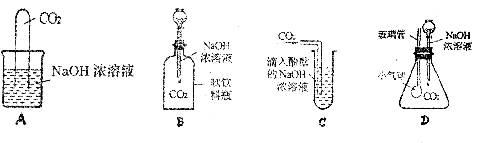
请回答下面的有关问题:
(1)按以上四种实验装置分别进行实验,能证明CO2和NaOH发生了化学反应的装置是(填写字母标号) 。在实验中你观察到的实验现象是: 。
(2)有同学说,仅仅通过观察以上实验现象就确定CO2和NaOH发生了化学反应是缺乏依据的,请你进一步设计实验来证明以上四个实验中均有新物质生成(简述实验操作步骤、现象及结论,并写出相关反应的化学方程式)。
四,计算题(本题共6分)
15.在实验室用氯酸钾和二氧化锰混合物加热制取氧气的反应过程中,若二氧化锰在混合物中的质量分数由20%提高到25%,求氯酸钾的分解率。