2007年枣庄市滕州初中毕业考试化学试题
第Ⅰ卷
一、选择题:本题共8个小题,每题2分,共16分。在下列各题的四个选项中,只有一个是符合题目要求的。请将正确选项的字母代号填在表内。
1.有人在洗菜时常将蔬菜切碎后再洗,这样做,易损失的营养素主要是
A.脂肪 B.蛋白质 C.糖类 D.维生素
2.1985年美国科学家斯莫利发现了C60,获得了1996年诺贝尔化学奖。据《厦门日报》报道:厦门大学郑兰荪院士的研究小组成功地获得了C50颗粒。下列说法正确的是
A.C50是一种新型的化合物
B.C50如果完全燃烧,生成物是一氧化碳。
C.C50与C60都是由碳原子构成的,它们是相同的一种物质
D.C50的发现说明还有可能发现碳元素的其他未知单质
3.下列实验记录合理的是
A.用托盘天平称取
B.用100mL烧杯量取75mL蒸馏水
C.用pH试纸测出某碱溶液的pH约为12
D.150mL酒精和50mL蒸馏水混合后得到200mL医用消毒酒精
4.为落实“十一五规划”主要污染物减排目标。我国确定
A
B
C
D
环境问题
温室效应
酸雨
赤潮
沙尘暴
防治措施
使用乙醇汽油
工厂废气处理达标后排放
使用无磷洗衣粉
植树造林
5.下图是某物质的溶解度曲线图,关于该物质下列说法不正确的是
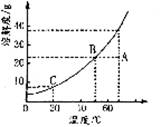
A.A点的溶液是不饱和溶液
B.
C.将A点溶液降温到
D.A、B两点比较,B点溶液的溶质质量分数较大
6.下列设计方案可行,且化学方程式书写正确的是
A.用NaOH溶液治疗胃酸过多症:NaOH + HCl===NaCl+H2O
B.实验室用稀硫酸与大理石反应制取CO2:H2SO4+CaCO3===CaSO4+CO2↑+H2O
C.用适量的稀盐酸除去铁表面的锈迹:Fe2O3+6HCl===2FeCl3+3H2O
D.用点燃的方法除去二氧化碳气体中混有的少量一氧化碳:2CO+O2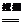 2CO2
2CO2
7.“NaCl+CO2+NH3+H2O===NaHCO3↓+NH4Cl”是著名的“侯氏制碱法”的重要反应。下图是4位同学对该反应涉及的有关知识发表的部分见解。其中不正确的是

8.目前世界上已证明“达菲”(化学式为C16H31N2PO8)是治疗禽流感的唯一良方,其生产原材料是作为中国传统香料和中药的八角中所含的一种重要成分――莽草酸(化学式为C7H10O5),据统计,全球90%的八角产于中国。下列叙述中不正确的是
A.莽草酸的相对分子质量是174
B.一个“达菲”分子中含有5种元素的58个原子
C.莽草酸分子中C、H、O三种元素的原子个数比为7∶10∶5
D.莽草酸和“达菲”分子中所含氧元素的质量分数之比为5∶8
二、非选择题:本大题包括5小题.共34分。
9.(3分)物质的分类标准有多种,请自拟三个分类标准,将甲烷、氧气、水、二氧化碳四种物质中的三种包括在某一标准内,而另一种不在该标准内。
标准一:__________________________________________________________________________;
标准二:__________________________________________________________________________;
标准三:__________________________________________________________________________。
10.(8分)某校兴趣小组同学对氢氧化钠溶液和稀盐酸混合后的有关问题,进行了如下探究。
(1)甲同学为了证明NaOH溶液与稀盐酸能够发生化学反应,设计并完成了如下图所示实验。
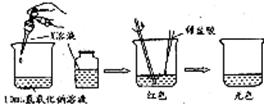
X溶液是____________,滴入的量一般为____________。
(2)乙同学也设计完成了另一个实验,证明氢氧化钠溶液与盐酸能够发生反应。在盛有氢氧化钠溶液的试管里,用胶头滴管慢慢滴入稀盐酸,不断振荡溶液,同时用pH试纸测定溶液的pH,直到盐酸过量。
①写出测定溶液pH的方法:________________________________________________________________________________________________________________________________。
②下图中哪个图像符合该同学的记录( )
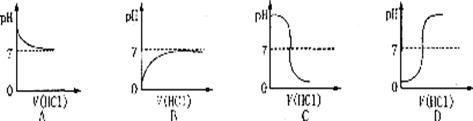
(3)你认为甲、乙两位同学的实验中,____________的实验能充分证明氢氧化钠与盐酸发生了反应,请说明理由:______________________________________________________________________________________________________________________________________________。
11.(10分)请你参与某学习小组进行研究性学习的过程,并协助完成相关任务。
【研究课题】探究热水壶底部水垢的主要成分。
【查阅资料】该小组同学通过查阅资料知道,天然水中一般都含有Ca2+、Mg2+、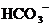 等离子,在加热条件下,这些离子趋于生成溶解度更小的物质―水垢(主要成分为碳酸盐、碱等的混合物)。同时,他们还查阅到下列有关物质的溶解性。
等离子,在加热条件下,这些离子趋于生成溶解度更小的物质―水垢(主要成分为碳酸盐、碱等的混合物)。同时,他们还查阅到下列有关物质的溶解性。
物质
Ca(HCO3)2
Mg(HCO3)2
Ca(OH)2
Mg(OH)2
CaCO3
MgCO3
溶解性
可溶
可溶
微溶
不溶
不溶
微溶
【提出猜想】水垢的主要成分一定含有Mg(OH)2和____________,可能含有Ca(OH)2和____________。
【设计方案】(1)甲同学在烧杯中放入少量研碎的水垢,加入适量蒸馏水充分搅拌,取上层清液加入碳酸钠溶液,没有白色沉淀,说明水垢中无Ca(OH)2。
(2)乙同学设计了下列实验装置,进一步确定水垢中含有碳酸盐的成分。其主要实验步骤如下:
①按下图组装仪器,将
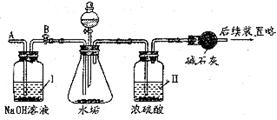
②测量一定时间内干燥管内物质增加的质量(见曲线图);
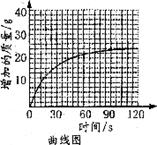
③待锥形瓶中不再产生气泡时,打开活塞B,从导管A处缓缓鼓人一定量的空气;
④再次称量干燥管内物质增加的质量;
⑤重复③和④的操作,直至干燥管内物质质量不变。
【讨论】a.步骤①加入样品前还应检查____________,所加的酸溶液是____________。
b.装置Ⅱ的作用是____________________________________;从导管A处缓缓鼓入一定量的空气时,装置I的作用是____________________________________。
c.研究性小组的同学通过简单计算,认为水垢中一定含有MgCO3,理由是__________________________________________________________________。
【实验结论】通过上述探究可知:水垢的主要成分有_____________________________。
12.(7分)孔雀石能发生如下图所示变化。
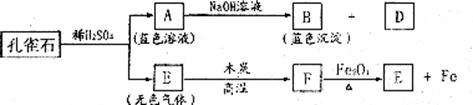
(1)推断A、B、D、E是何种物质,写出它们的化学式:
A.____________,B.____________,D.____________,E.____________。
(2)从图中转化关系可以初步判断,孔雀石中含有的元素是____________。
(3)F跟Fe2O3反应的化学方程式是________________________________________________,该反应中具有还原性的物质是____________。
13.(6分)某钙片的标签如图,且知此钙片成分中只有碳酸钙含有钙元素。
执行标准:GBl413―99
主要成分:碳酸钙