2007届济宁市薛城区第一次调研考试九年级化学试题
答题时需用的元素符号、原子序数和相对原子质量,请从下面的元素周期表(部分)中查找。解答第2题时,也要用到此表。


一、选择题(每小题只有一个选项符合题意.把正确答案序号填入下列表格中。每小题2分,共16分。
1.下列各级连线都正确的是( )
A.物质与用途的连线情况 B.物质与变化关系连线情况



 氢气
能燃烧,做燃料
矿石粉碎 化学变化
氢气
能燃烧,做燃料
矿石粉碎 化学变化
 氧气
人工降雨
铁生锈 物理变化
氧气
人工降雨
铁生锈 物理变化
 干冰
能助燃
冰溶化 物理变化
干冰
能助燃
冰溶化 物理变化
C.化学反应与反应类型连线情况 D.仪器与用途的连线


 高温煅烧石灰石
化合反应
胶头滴管 做反应容器,加热固体,液体等
高温煅烧石灰石
化合反应
胶头滴管 做反应容器,加热固体,液体等

 碳在氧气中燃烧
复分解反应
量筒 吸取、滴加少量液体
碳在氧气中燃烧
复分解反应
量筒 吸取、滴加少量液体
铁丝进入硫酸铜溶液中 分解反应 试管 度量液体体积
2.小明查得资料:在元素周期表中,同一纵行的元素具有相似的化学性质。则具有相似化学性质的一组元素是
A.钠和硫 B.硅和Ge C.Rb和Te D.Sr和Se
3.化学知识中有很多的“相等”。下列说法中不正确的是
A.参加化学反应的物质的总质量等于反应后生成的物质的总质量
B.化合物中元素化合价的正价总数与负价总数的数值相等
C.溶液稀释前后溶质的质量相等
D.在原子中原子核内的质子数都等于中子数
4.2005年lO月以来,禽流感呈现出在全球蔓延的趋势。国际卫生组织推荐“达菲”作为治疗禽流感的药品之一。在中国,“达菲”也已被列为《人禽流感诊疗方案(2005版)》的治疗用药。该药物的主要成分是一种化学式为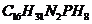 (相对分子质量是410)的物质。关于该物质的说法不正确的是
(相对分子质量是410)的物质。关于该物质的说法不正确的是
A.该物质中碳、氧元素的质量之比是3:2
B.该物质中磷元素的质量分数约为7.56%
C.该物质中只含有4个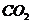 分子
分子
D.该物质的一个分子中含有58个原子
5.有六种物质能按下列顺序排序:(1)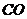 ,(2)
,(2) ,(3)
,(3) ,(4)
,(4) ,(5)
,(5) ,(6)
,(6) 。根据它们的组成和排列的规律,
。根据它们的组成和排列的规律, 可能是
可能是
A. B.
B.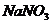 C.
C. D.
D.
6.欲除去下列物质中的少量杂质,所用试剂或方法正确的是
物质
杂质
试剂或方法
A
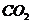
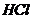 气体
气体
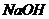 溶液
溶液
B


稀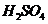
C
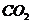
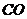
点燃
D
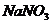 溶液
溶液
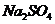 溶液
溶液
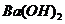 溶液
溶液
7.甲、乙两物质的溶解度曲线如图所示,下列叙述中正确的是
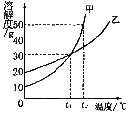
A.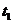 ℃时,甲和乙的溶解度均为30
℃时,甲和乙的溶解度均为30
B.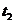 ℃时,甲和乙的饱和溶液中溶质的质量分数相等
℃时,甲和乙的饱和溶液中溶质的质量分数相等
C.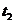 ℃时,在100 g水中放入60 g甲,其溶质的质量分数为37.5%
℃时,在100 g水中放入60 g甲,其溶质的质量分数为37.5%
D.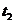 ℃时,分别在100 g水中各溶解20 g甲、乙,同时降低温度,甲先达到饱和
℃时,分别在100 g水中各溶解20 g甲、乙,同时降低温度,甲先达到饱和
8.下列四个示意图分别表示对应的四种操作过程,其中正确的是
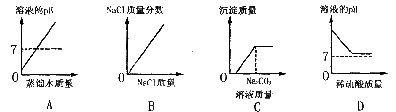
A.向一定量的稀盐酸中不断滴入蒸馏水
B.在一定条件下,向一定量的水中不断加入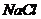 固体
固体
C.向一定量的硝酸和硝酸钙混合溶液中不断滴入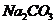 溶液
溶液
D.向一定量的氢氧化钠中不断滴入稀硫酸
二、填空与简答题(共21分)
9.(6分)为了获得人类生活和发展需要的各种物质,并更好地利用这些物质,化学家们通常按照某种标准,将众多的化学物质进行分类。根据你学过的初中化学知识,按照物质的组成。将空气、硫酸铵、石墨、铜、氢气、纯碱、氧化镁、烧碱、乙醇、食盐水进行分类。(要求用框图的形式表示,层次分明,分类精细)
10.(13分)水是宝贵的自然资源,在工农业生产和日常生活中有着极其广泛的应用。
自来水的生产过程大体如下图
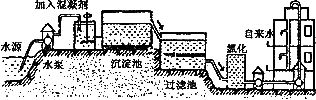
(1)上图过滤池中有活性炭层,活性炭起____作用,该过程中发生________变化。氯化时,通常通入一定量氯气,它与水反应生成盐酸和次氯酸。实验室配制 溶液时不宜使用自来水。其原因是(用化学方程式表示)_____________________。高铁酸钾(
溶液时不宜使用自来水。其原因是(用化学方程式表示)_____________________。高铁酸钾(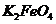 )是一种理想的水处理剂,高铁酸钾中铁元素的化合价是__________。
)是一种理想的水处理剂,高铁酸钾中铁元素的化合价是__________。
(2)电解水时,加入少量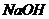 可以增强水的导电性。现将O.1
可以增强水的导电性。现将O.1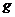
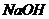 溶解在99.9
溶解在99.9 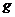 水里。接通直流电源后,与电源正极相连的一端放出的气体是________,当溶液中
水里。接通直流电源后,与电源正极相连的一端放出的气体是________,当溶液中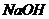 的质量分数变为0.2%时,有_______水被分解。
的质量分数变为0.2%时,有_______水被分解。
(3)在河旁有甲、乙、丙、丁四座工厂(位置如下图所示),每个工厂排出的废液含有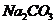 、
、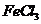 、
、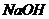 、
、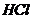 中的一种。某环保小组对河水监测时发现:甲处河水呈无色;乙处河水呈红褐色;丙处河水由浑变清;丁处产生气泡,河水澄清。请回答:
中的一种。某环保小组对河水监测时发现:甲处河水呈无色;乙处河水呈红褐色;丙处河水由浑变清;丁处产生气泡,河水澄清。请回答:
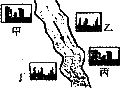
①甲工厂排出的废液是一种碱性物质,检验该物质呈碱性可选用的试剂是_____。
②乙处河水呈红褐色的化学方程式是______________
③丁处产生气泡的化学方程式是______________
④保护水资源,我们应该采取的措施是_______________。
11.(2分)维生素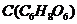 主要存在于蔬菜、水果中。它能增强人体对疾病的抵抗能力。
主要存在于蔬菜、水果中。它能增强人体对疾病的抵抗能力。
(1)取3片维生素C,压碎后溶于10 mL水中过滤。取少量滤液向其中滴加几滴紫色石蕊试液,试液变红,说明维生素C的水溶液呈_________性。
(2)维生素C在酸性环境中比较稳定,在高温时易被破坏。请你想一想,如何食用黄瓜,才能充分利用黄瓜中丰富的维生素C________________________________.
三、实验题(8分)
12.(8分)下表列出了空气、氧气、二氧化碳、氨气在标准状况下的密度和溶解性。
物质
空气
氧气
二氧化碳
氨气
密度(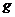 /L)
/L)
1.293
1.429
1.977
0.771
溶解性
/
不易溶
能溶
极易溶
实验室制取氨气方程式为:2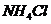 (固)+
(固)+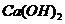 (固)
(固)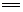
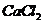 +2
+2 ↑+2
↑+2
(1)根据上述信息,选择实验室制取和收集氧气、二氧化碳、氨气的装置,请在相关空格处打“ √”。
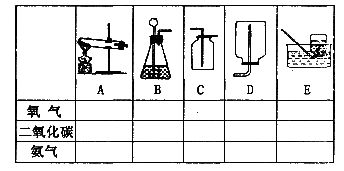
(2)若用A装置进行木炭还原氧化铜实验并检验气体产物,还需补充部分装置。补充装置中所需的仪器是_______________,所需的化学药品为________________.
四、计算题(5分)
13.(5分)某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成。分四次取样品与稀硫酸反应,其实验数据记录如右表:
1
2
3
4
’
取样品质量(g)
50.0
50.O
50.O
0.O
取稀硫酸质量(g)
40.0
80.0
120.0
160.0
产生气体质量(g)
O.4
0.8
1.0
1.O
试计算:
(1)黄铜中锌的质量分数。
(2)所用稀硫酸中溶质的质量分数。(锌的相对原子质量为65)