2006-2007学年度上学期期末质量调查
初四化学试题
(60分钟 满分100分)
可能用到的相对原子质量:H1 O16 Mg24 S32 Cl35.5
一、选择题:(本题包括16小题,每小题3分,共48分。每小题只有一个选项符合题意,请将正确选项填在下面的表格内)
1.我国是最早使用铁器的国家之一,下列关于铁的知识叙述正确的是
A.钢就是纯铁 B.铁锈的主要成分是四氧化三铁
C.用铁锅炒菜可使食物中增加微量铁元素 D.铁桶可用来装波尔多液
2.选用金、银、铜等金属制作钱币,从化学角度分析,其主要原因是
A.硬度大 B.化学性质比较稳定
C.密度大 D.有比较漂亮的色泽
3.下列有关实验操作中,正确的是
A.稀释浓硫酸时,将浓硫酸慢慢注入盛水的量筒内,并用玻璃棒不断搅拌
B.用胶头滴管向试管中加液体时,滴管要在试管口的竖直正上方悬滴
C.用PH试纸测溶液PH值前,要用少量蒸馏水将PH试纸润湿
D.把氢氧化钠固体放在天平右盘上的玻璃器皿中称量
4.小明家地处少雨的山区,种的庄稼生长不茂盛,叶色偏黄,且籽粒不饱满,小明学了化学知识后,帮助父母科学种田,建议父母买化肥改善现状,以获得好收成,他应向父母提出买的化肥是
A、CO(NH2)2 B、KNO
5.对于某物质的溶液,可提供以下数据:①溶液的质量 ②溶剂的质量 ③溶质的质量 ④溶液的体积 ⑤溶质的相对分子质量 ⑥溶液的密度,其中不能用来计算该溶液溶质质量分数的一组数据是
A.①② B.②③ C.①⑤ D. ②④⑥
6.在①酸性氧化物、②碱性氧化物、③酸、④碱等四类物质中,经一步反应可以生成盐的是
A.只有①②③ B.只有②③④ C.只有①②④ D.①②③④
7.久置于空气中的石灰水,其表面会形成一层白膜。此时溶液的pH与变化前溶液的pH相比
A.偏大 B.偏小 C.一样 D.无法比较
8.若用实验证明Fe2(SO4)3溶液显黄色不是由SO42-造成的,下列实验无意义的是
A.观察Na2SO4溶液的颜色
B.向Fe2(SO4)3溶液中滴加适量氢氧化钠溶液,振荡后静置,溶液黄色消失
C.向Fe2(SO4)3溶液中滴加适量无色氯化钡溶液,振荡后静置,溶液黄色未消失
D.加水稀释Fe2(SO4)3溶液后,溶液黄色变浅
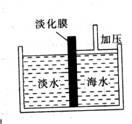 9.右图是采用膜分离技术的海水淡化装置。对海水加压后,
9.右图是采用膜分离技术的海水淡化装置。对海水加压后,
只有水分子可以通过淡化膜,离子等其它粒子不能通过淡化膜。
加压前后,装置右侧海水什么增加?
A.溶质质量分数 B.溶剂质量 C.溶液质量 D.溶质质量
10.亚硝酸钠外观酷似食盐,有咸味,加热会分解,放出有臭味的气体。一些不法商贩有时用亚硝酸钠冒充食盐出售,造成中毒事件。请结合下表信息判断,下列区别亚硝酸钠和氯化钠的方法中,错误的是
亚硝酸钠
氯化钠
跟稀盐酸作用
放出红棕色的气体
无反应
跟硝酸银溶液作用
生成浅黄色沉淀
生成白色沉淀
A.加热 B.滴加稀盐酸 C.滴加硝酸银溶液 D.品尝味道
11.某工厂排出的酸性污水中,含有有毒的Cu2+,欲除去Cu2+并降低污水的酸性,加入下列适量的物质时,不能达到目的的是
A.食盐 B.纯碱 C.烧碱 D.熟石灰
12.t℃时,有两瓶硝酸钾溶液,一瓶是饱和溶液,另一瓶是不饱和溶液。下列实验操作中,无法区分这两种溶液的是
A.降低温度 B.升高温度 C. t℃时蒸发少量水 D.加入少量硝酸钾固体
13.某溶液中含有AgN03、Cu(N03)2、Ba(N03)2三种溶质,用①NaCl②Na
A.①②③ B.③②① C.②③① D.①③②
14. 配制一定溶质质量分数的氯化钠溶液的一些操作步骤见下图,正确的操作顺序是
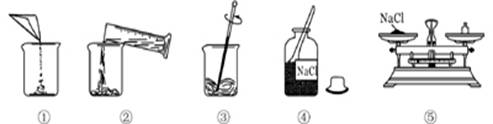
A.④⑤①②③ B.①②③④⑤ C.③④①②⑤ D.②①④③⑤
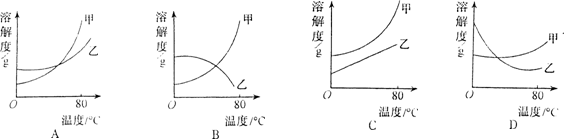 15.甲、乙两种物质在
15.甲、乙两种物质在
16.化学中常常出现“1+1≠
A
B
C
D
二、填空与简答题:(本题包括6小题,共42分)
17.(4分) H、O、C、Cl、Na、Ca元素中,选择适当的元素组成符合下列要求的物质,将其化学式填入空格内:
(1)常用于检验碳酸根离子的一种酸 ;(2)常用于改良酸性土壤的一种碱 ;
(3)常用于家庭蒸馒头发酵的一种盐 ;(4)常用于人工降雨的一种氧化物 。
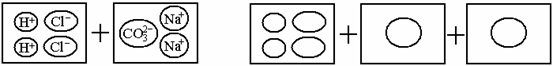
18. (3分)2005年度诺贝尔化学奖授予了在有机化学的烯烃复分解反应方面作出了杰出贡献的三位科学家。我们现阶段所学的复分解反应的实质是反应物中的一些阴、阳离子相互结合生成水、气体或沉淀。如BaCl2溶液和Na2SO4溶液反应,实际参加反应的是Ba2+和SO42-结合生成BaSO4沉淀,而Cl-和Na+则是“旁观者”,并没有参加反应,仍然在溶液中。请在下图右边的圆圈中填入适当的分子或离子符号,来体现稀盐酸和碳酸钠溶液反应的实质:

 19.(4分)实验室中有些药品需密封保存,某同学将其原因归纳为下列两种情况:①药品易挥发;②药品能与空气中的某些成分发生化学反应。
19.(4分)实验室中有些药品需密封保存,某同学将其原因归纳为下列两种情况:①药品易挥发;②药品能与空气中的某些成分发生化学反应。
(1)写出一个符合情况②的化学方程式: 。
(2)该同学的归纳并不完整,请你再补充一种情况 。
20.(12分)向一盛有无色溶液的试管中加入另一种无色溶液,生成了一种白色沉淀。试根据你学过的酸、碱、盐的知识和题目要求,推测生成的白色沉淀,按要求写出相应的化学式或化学方程式。
(1)可能一:如果沉淀不溶于稀硝酸,沉淀可能是 ,两种无色溶液中的溶质分别是 。
(2)可能二:如果沉淀溶于稀硝酸且有气体产生,沉淀可能是 ,沉淀与硝酸反应的化学方程式为 。
(3) 可能三:如果沉淀溶于稀硝酸但不产生气体,沉淀可能是 ,两种无色溶液反应的化学方程式为 。
21.(10分)以下是某实验小组在探究金属化学性质过程中的部分实验记录,请你根据实验记录回答下列问题:
(1)大小、形状都相同的金属与溶液质量、溶质质量分数都相同的稀盐酸反应的记录
金属
铝片
锌片
铁片
铜片
银片
反应现象
开始无气泡,过一段时间后缓慢出现气泡
产生气泡且速度较快
产生气泡但速度缓慢
无气泡
无气泡
①根据金属活动性顺序和以上记录可知,能与稀盐酸反应的金属应具备的条件是:
。
②根据金属活动性顺序,铝片应比锌片活泼。但实验记录中铝与稀盐酸的反应速度比锌的更______(填“快”或“慢”)。你认为上述实验记录中出现与金属活动性顺序相违背的现象的原因是 。
(2)实验小组继续探究铜与银的金属活动性强弱。小组设计的实验方案是:铜片与AgNO3溶液反应。请你写出反应现象和反应的化学方程式。
。有同学提出用银片与Cu(NO3)2溶液也能达到实验目的,你同意此同学的方案吗? (填“是”或“否”)
22.(9分)水蒸气通过炽热的焦炭所产生的一氧化碳和氢气的混合气体叫水煤气。所制取的水煤气还含有二氧化碳和水蒸气。请选用如下装置设计实验,确认水煤气中含有氢气和一氧化碳。
(1)水煤气通过实验的正确连接顺序是 (用字母表示);
(2)描述能确认水煤气中含有H2的现象: ;
含有CO的现象: 。
(3)该实验尾气的处理方法是 。
三、计算题(本题包括1小题,共10分)
23.(10分)某实验小组需要用锌和稀盐酸制取氢气,但实验室没有稀盐酸,只有36.5%的浓盐酸
(1)将
(2)用(1)中所配制的稀盐酸与足量锌反应能得到氢气多少升? ( H2的密度为
(计算结果保留一位小数)