2005年大连市初中毕业升学统一考试化学
本试卷满分100分,考试时间100分钟.
相对原子质量: C:12 N:14 O:16 K:39 Fe:56
一、 选择题(本题共18小题,每小题1分,共18分)说明:每小题只人一个选项符合题意。
1、下列变化中,属于化学变化的是
A空气液化 B矿石粉碎 C高粱酿酒 D海水晒盐
2、油脂是人体重要的营养物质。下列食物中,富含油脂的是
A豆腐 B花生 C面包 D草莓
3、下列物质中,属于溶液的是
A牛奶 B蒸馏水 C石灰乳 D生理盐水
4、磷酸二氢铵(NH4H2PO4)是一种复合肥料,它属于
A单质 B氧化物 C化合物 D混合物
5、下列做法中,不会造成环境污染的是
A利用风力发电 B焚烧废弃塑料
C 使用含磷洗衣粉 D建筑垃圾云填海造地
6、下列气体与空气混合后,遇明火可能发生爆炸的是
A氮气 B二氧化碳 C氧气 D甲烷
7、天然水分别经过下列净化操作后,一定能得到软水的是
A沉淀 B过滤 C吸附 D蒸馏
8、下列实验操作中,正确的是
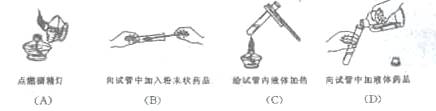
9、人体缺少某种元素,会引起甲状腺肿大,该元素是
A 钙 B碘 C锌 D 铁
10、下列关于物质用途的说法中,错误的是
A 碳酸钙用作补钙剂 B碳酸氢钠用于焙制糕点
C 纯碱溶液用于除水垢 D食盐用作调味品
11、下列各组物质中,都是由分子构成的是
A 水、氢气 B铁、氧气 C氯化钠 、铜 D氯化钠、水
12、某洗涤剂的PH为12,向其中滴入2滴酚酞试液,溶液的颜色呈
A红色 B紫色 C蓝色 D 无色
13、下列化学方程式中,书写正确的是
A Mg+O2 MgO2
MgO2
B H2O=H2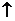 +O2
+O2 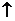
C 2Fe+6HCl=2FeCl+3H2 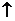
D Na2CO3+Ca(OH)2=CaCO3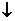 +2NaOH
+2NaOH
14、氢氧化钠和氢氧化钙都是常见的碱。下列关于它们的说法中,正确的是
A都能用作建筑材料 B都能用作某些气体的干燥剂
C它们的溶液都能用于检验二氧化碳气体
D它们的溶液都能用于吸收二氧化硫气体
15、硬铝的下列性质中,与制造飞机外壳无关的是
A导电性较好 B密度较小 C耐腐蚀性较强 D硬度较大
16、下列做法中,能减缓化学反应速率的是
A面团发酵时放在温热处 B人在进食时细细嚼食物
C 在食品密封包装时充入氮气 D煤燃烧时向煤炉中鼓入空气
17、硝酸铵受热到300OC以上时,在有限的空间内能引起爆炸,发生的反应之一表示为:2NH4NO3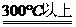 O2
O2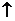 +2X
+2X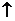 +4H2O,则X的化学式为
+4H2O,则X的化学式为
A N2O B N
18、下列做法中,有益于人体健康的是
A为了杀菌和保鲜,用甲醛溶液浸泡海产品
B为了提高牛奶中的含氮量,向牛奶中添加尿素
C 为了给人体补充铁元素,在麦片中加入少量铁粉
D 为了使熟肉制品保鲜,加工时加入较多的亚硝酸钠
二、填空题(本题共10小题,共25分)
19、从H、O、S、Ca四种元素中,选择适当的元素,各写一个符合下列要求的化学式
物质类别
酸
碱
盐
化学式
20、现在下列三种化肥:磷矿粉[主要成分是Ca3(PO4)2]、氯化铵(NH4Cl)、D 硫酸钾(K2SO4)其中属于钾肥的是___________;与熟石灰混合研磨后,能产生刺激性气味气体的是____________________
21、请写出实验室里用高锰酸钾制氧气的化学方程式:____________________________。该反应中,锰元素的化合价由反应前的+7价,变为反应后的+6价和______价。
22、氢气是一种清洁能源,以氢燃料电池为动力的汽车已在北京市试运行。(1)氢气燃烧的化学方程式为_________________________(2)从质量守恒观点看,水可以作为制取氢气的原料,其原因是________________________________(3)目前,开发利用氢能源的困难之一是____________________________.
23、人皮肤的pH一般在4.5~6.5之间,则皮肤表面显(填“酸”、“中”或“碱”)____性。如果某人皮肤的pH为8.2,现有下列四种pH不同的洗面奶供选购a 4.5 b
24、汽车的主要燃料是汽油和柴油,在排放的尾气中除二氧化碳和水蒸气外,不含有少量的一氧化碳。(1)汽油和柴油都是_____中工的产物,分离时根据它们的_____不同而制得。(2)汽车尾气中含有少量一氧化碳的原因是______________________________(3)一氧化碳有很多用途,用化学方程式表示其中一例:____________________________
25、在非供暖期,铁制供暖设施中仍需要充满水,目的是防止铁生锈,其原理是_____________,请再写出一种日常生活中防止铁制品生锈的做法_________________________.
26、空气污染会给人类带来危害,目前列入空气污染物的有:二氧化硫、一氧化碳、二氧化碳、臭氧,可吸入颗料物等。在治理环境污染时,通常考虑的是污染源、污染物质、造成后果、解决措施等一系列问题(1)产生二氧化硫的污染源是_____________(2)二氧化氮造成的后果是__________________(3)减少空气中可吸入颗料物的措施是________。
27、“原子经济化”是现代化学工业的发展方向,它的优点是最大限茺地利用原料,使原料全部转化成某种产物。符合这一观点的化学反应的基本类型是____________,请你写出一个能够实现“原子经济化”的化学方程式____________________________
 28、某同学在总结实验室有些药品需密封保存的原因时,归纳了下列两种情况:1药品能吸收空气中的水蒸气 2 药品能与空气中的某些成分发生化学反应(1)写出一个符合情况2的化学方程式:(2)该同学的归纳不完整,你还能补充的一种情况是____________________________________
28、某同学在总结实验室有些药品需密封保存的原因时,归纳了下列两种情况:1药品能吸收空气中的水蒸气 2 药品能与空气中的某些成分发生化学反应(1)写出一个符合情况2的化学方程式:(2)该同学的归纳不完整,你还能补充的一种情况是____________________________________
三、回答下列问题(本题共8小题,共24分)
29、维生素C的化学式为C6H8O6,关于“C6H8O
(1)请你将说法3、说法4省略的部分埴写在横线上。说法3:表示维生素C由____________________,说法4:表示每个维生素C分子由____________。
(2)维生素C是人体必需的营养物质。为了保持体内维生素C的拥有量,请写出一种能补充人体维生素C的具体做法。
30、写出下列反应的化学方程式,并注明基本反应类型
(1)工业上煅烧石灰石制生石灰
(2)用氢氧化钠溶液中和含盐酸的废水

(1)大连水资源紧缺程度为________________
(2)为缓解我市水资源的紧缺状况,结合你的生活实际,写出两点具体做法。
32、流感发生时,可用醋对室内空气进行消毒,为了迅速增加室内空气中醋的含量,常采用给醋加热的方法。
(1)通过对上述事例的分析,关于温度与分子运动速率的关系你能得出什么结论?
(2)请你从生活或生产实际中,再举出一个符合上述结论的事例。
 33、在使用二氧化碳灭火器灭火时,喷射出的液态二氧化碳使火焰熄灭。请解释其中的灭火原因。
33、在使用二氧化碳灭火器灭火时,喷射出的液态二氧化碳使火焰熄灭。请解释其中的灭火原因。
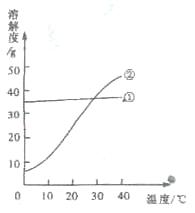
34、我国北方有许多盐湖,湖水中溶有大量的碳酸钠和氯化钠,那里的农民冬天捞碱(碳酸钠),夏天晒盐(氯化钠)。
(1)右图是碳酸钠和氯化钠在不同温度下的溶解曲线,其中表示碳酸钠溶解度的曲线是(填序号)_________________
.(2)从湖水中得到碳酸钠常含有少量的氯化钠,可以用____________的方法得到纯净的碳酸钠。
35、A、B、C、D是四种常见的物质,在自然界中能相互转化;A和B在一定条件下可以转化成C和D,C和D在一定条件下也可以转化成A和B,A在自然界中含量升高能引起温室效应;C是一种糖类,在人体内经缓慢氧化提供能量。请你判断A、B、C、D各是什么物质。A B C D
36、近下列要求各举一个化学反应实例,并加以具体说明。(原扫描图缺此题)
四、实验题(本题共4小题,共20分)
37、实验室里制取二氧化碳气体,有下列仪器可供选用
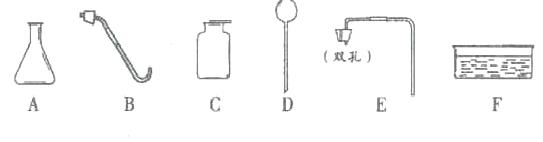
请你回答下列问题:
(1) 制取二氧化碳气体所需的药品是_________________________(2)收集二氧化碳气体的方法是____________________(3)制取并收集二氧化碳气体所需的仪器是(用仪器的序号回答)____________________(4)难二氧化碳气体是否收集满的方法是__________________________(5)利用实验室里抽取二氧化碳气体的发生装置,还能制取另一种气体,写出制取该气体的化学方程式:______________________
38、请你从下列所给药品中,选择合适的物质,用两种方法证明稀硫酸与氢氧化钠溶液反应后,硫酸有剩余。请你将有关内容填在下表中。
所给药品:酚酞试液、石蕊试液、稀盐酸、铁粉、铜粉、碳酸钠粉末,氯化钠固体、氧化铜粉末。
实验操作
实验现象
方法1
方法2
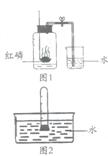 39、下面是测定空气中氧气体积含量的两个实验。
39、下面是测定空气中氧气体积含量的两个实验。
实验1:在集气瓶内预先装少量水,余下的容积5等分,做好标记,在带橡皮塞和导管的燃烧匙内装足量的红磷,用弹簧夹夹紧乳胶管,点燃燃烧匙内的红磷,立即伸入集气瓶内,塞紧橡皮塞(如右图1)。待红磷熄灭并冷却到室温后,打开弹簧夹。
实验2:将试管的容积5等分,做好标记。在试管中加入一小块(足量)白磷,用橡皮塞塞紧管口,将试管放入热水中,使白磷燃烧。等白磷熄灭并冷却到室温后,将试管倒立于盛有室温下水的水槽中(如右图2所示)并在水中将橡皮塞取下。(1)写出红磷燃烧的化学方程式:________________________________(2)实验2中,在水中而不在空气中取下橡皮塞的原因是_______________________________(3)从测定结果分析,上述实验中效果较好的是哪一个?写出另一个实验的两点不足。
40、某活动小组从工厂收集到了一些含有硝酸银的废液中,以及废铁屑、废锌屑的混合物。在回收银时,他们将一定量的上述金属混合物加入到含硝酸银的废液中,充分反应后过滤,得到固体和浅绿色滤液(所含其他杂质不考虑)。为了探究滤液中溶质的组成,他们做出下列猜想:(1)溶质为硝酸亚铁(2)溶质为硝酸亚铁和硝酸银(3)溶质为硝酸锌和硝酸来铁(4)溶质为硝酸锌、硝酸亚铁和硝酸银。
(1)上述猜想中,错误的是(填序号)________________,其原因是____________
(2)有的同学认为滤液中溶质有硝酸锌,你认为是否正确?________其原因是_____________(2)某同学将一铜片放入滤液中,目的是___________________________________,一段时间后铜片没有发生变化,上述猜想中可以排除的是(填序号)_____________________________.
五、计算题(本题共2小题,共13分)
41、无土栽培的某种营养液中,含硝酸钾(化学式为KNO3)的质量分数为7.1%.
(1)某蔬菜生产基地欲配制该营养液
(2)这些硝酸钾中含氮元素的质量是多少?(精确到
42、为了测定某些磁铁矿中四氧化三铁的质量分数,甲、乙两组同学根据磁铁矿与一氧化碳反应的原理,分别利用两种方法测定了磁铁矿样品中四氧化三铁的质量分数。已知磁铁矿与一氧化碳的化学方程式如下(磁铁矿中的杂质不参加反应):
Fe3O4+4CO 3Fe+4CO2
3Fe+4CO2
(1)甲组同学取该磁铁矿样品
(2)乙组同学取该磁铁矿样品