2007年中考模拟考试理科综合试题化学部分
注意事项:
1.答题前请考生务必在答题卡及试卷的规定位置将自己的姓名、考试号、考试科目、座号(第Ⅱ卷)等内容填写(涂)准确。
2.本试题分第Ⅰ卷和第Ⅱ卷两部分。第Ⅰ卷(1-4页)为选择题,60分;第Ⅱ卷(5-12页)为非选择题,110分。共170分。考试时间为150分钟,考生不能使用计算器。
3.第Ⅰ卷每小题选出答案后,必须用2B铅笔把答题卡上对应题目的答案标号(A、B、C、D)涂黑。第Ⅱ卷须用蓝黑钢笔或圆珠笔直接答在试卷上。
4.考试结束后,由监考教师把第Ⅱ卷和答题卡一并收回。
5.相对原子质量:H:
第Ⅰ卷(选择题 共60分)
本题共30小题,每小题给出的四个选项中只有一个是正确的,请把正确的选项涂在答题卡的相应位置上。每小题2分,错选、不选、多选均不得分
11.有关“物质――性质――用途”的叙述中,用途与性质不相关的是
A.氢气――还原性――冶炼金属
B.氯化铵――含氮元素――化学肥料
C.盐酸――能跟许多物质反应并放出热量――除去铁锈
D.干冰――蒸发时吸收热量――制冷剂
12.在实验的过程中多次重复实验的主要原因是
A.得到较多的数据 B.得出不同的结论
C.实验失败后重新再做 D.避免偶然现象,使结果更真实
13.目前最甜的甜味剂是纽甜,化学式为C20H30N2O5?H2O,其甜度是蔗糖的7000~13000倍。它是一种低熔点、无吸附性、结晶性化合物,安全无毒,稳定性好,能量值很低,是一种非营养型甜味剂。下列有关纽甜的说法中错误的是
A.纽甜是一种有机物
B.纽甜只适用食品生产,不能应用于饮料生产中
C.用纽甜作甜味剂的食品非常适宜糖尿病人、肥胖症病人等食用
D.纽甜在人体中也会发生化学反应
 14.可用如右图模型来表示的化学反应是
14.可用如右图模型来表示的化学反应是
A.2HgO△ 2Hg+O2↑ B.2H2O通电 2H2↑+O2↑
C.2HClO△ 2HCl+O2↑ D.CaCO3高温 CaO+CO2↑
15.把一根洁净的铁钉放入稀硫酸中,下列叙述:① 铁钉表面产生气泡 ② 液体由无色变为浅绿色 ③ 铁钉的质量减轻 ④ 液体的质量减轻。其中正确的是
A.①②③ B.①②④ C.②③ D.①②③④
16.下列做法不会对人体健康造成危害的是
A.用硫酸铜对饮用水进行消毒 B.牛奶经工业发酵后得到的酸奶
C.用甲醛溶液保鲜海产品 D.用工业用盐腌制的泡菜
 17.右图是某同学设计的一个可燃气体安全点燃装置,对此装置的评价和使用错误的是
17.右图是某同学设计的一个可燃气体安全点燃装置,对此装置的评价和使用错误的是
A.未经检验纯度的气体通过此装置后可安全点燃,不会发生爆炸
B.要达到安全点燃效果,烧杯内的水可不没过倒置漏斗的边缘
C.此装置防止点燃不纯气体爆炸的原理是使不纯的气体不与燃着气体直接接触
D.此装置适用于难溶于水的可燃性气体
18.化学影响着社会的发展和我们的生活质量,根据你已有的生活经验和化学知识判断,下列说法或作法不正确的是
A.瓶装啤酒应放在阴凉处 B.煤、石油、天然气是不可再生的能源
C.用氢氧化钠改良酸性土壤 D.过量使用化肥、农药会造成环境污染
19.同学们在做实验时发现,将镁条放入某CuCl2溶液中,镁条表面有气泡产生。对于这一异常现象产生的原因,同学们设计了以下探究方案进行讨论,其中没有意义的是
A.甲同学用镁粉与该CuCl2溶液反应,观察产生气泡的快慢
B.乙同学推测该气体可能是H2,并收集气体用点燃法检验
C.丙同学用锌粒与该CuCl2溶液反应,观察是否有气泡产生
D.丁同学猜想该CuCl2溶液呈酸性,并用pH试纸检测
20.检验某可燃烧的化合物是否含有氢、碳、氧3种元素,在该物质完全燃烧后还必须进行的实验是:①用带火星的木条检验;②用无水硫酸铜检验;③用澄清石灰水检验;④对反应物、生成物进行称量。以下选项中正确的是
A.①②③④ B.②③④ C.①②③ D.②③
第Ⅱ卷(非选择题 共110分)
化学部分(30分)
一、理解与应用,本大题 包括4个小题 ,共13分
1.(3分)我国制碱工业的先驱侯德榜发明了侯氏制碱法,为我国制碱工业的发展做出了极大的贡献。纯碱(化学式为Na2CO3)是常见的工业用碱,也是许多化工产品的生产原料,在生活和生产中得到广泛应用。
⑴纯碱不是碱,在化学物质分类中属于________类物质;
⑵石灰石、大理石的主要成分是碳酸钙,在组成上与纯碱具有相同的组成部分,因而,它们都能与盐酸反应产生(填具体物质)__________气体;
⑶纯碱溶液与石灰水反应可制得少量NaOH溶液,在反应基本类型中,该反应属于_____________反应。
2.(3分)苯甲酸是一种食品防腐剂,它是一种片状晶体,在水中的溶解度如下表:
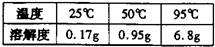
某同学为了提纯某一苯甲酸样品(其中含泥沙等难溶于水的杂质),进行了如下实验:
⑴取样品约
⑵将烧杯放在石棉网上加热,将样品充分溶解后,在加入少量蒸馏水,然后趁热过滤。趁热过滤的目的是 。
⑶将所得滤液 ,使苯甲酸以晶体形式析出,然后过滤得到较纯净的苯甲酸晶体。
3.(3分)人体所需的元素从食物中摄取不足时,可通过食品添加剂和保健药剂以补充。如制成补钙、补锌的保健药剂或制成加碘食盐等,来增加对这些元素的摄入量。
⑴氟是人体必需的一种微量元素,在牙釉质表面有一层坚硬的氟磷灰石,它的化学式为 Ca5(PO4)
⑵为了提高补钙效果,服用补钙剂时常需配合服用维生素D,据此可推知维生素D的功能是_____________。维生素D属于六大类营养素中的_____________。
4.(4分)A、B、C、D是常见的化合物,A中含有钾元素。它们之间反应关系如下:
①
根据以上信息,推断A、B两物质化学式:
A: B: 写出反应②的化学方程式: 。
二、实验与探究,本大题包括2个小题 ,共12分
5.(5分)小明在学习金属活动性顺序时,对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”这句话产生了好奇。为什么用“一般”这个词呢?难道还有例外吗?
[查阅资料]Na性质活泼,常温下,与氧气反应,也可以与水反应放出氢气。
[实验与分析]①在实验室中,金属钠保存在煤油中;②用镊子从煤油中取出金属钠,放在滤纸上,用小刀切下一小块,投人蒸馏水中,发现钠块立刻熔化成银白色小球,在水面上到处游动,滴入酚酞试液后溶液变成红色;③往硫酸铜溶液中,投入一小块钠,又出现蓝色沉淀,但没有红色物质析出。
⑴金属钠保存在煤油中的原因_________________________。
⑵从实验②中,你能得出哪些信息?(任写二条)。 、
。
⑶写出钠与硫酸铜溶液反应的化学方程式________________________________、
。
[结论]活动性较强的金属不一定将位于其后面的金属从它们的盐溶液中置换出来。
6.(7分)甲同学为了探究铝、铁和铜三种金属的活动性,他用铜丝、铁丝、铝丝和稀盐酸四种试剂,设计了以下只用一支试管,取一次盐酸的探究方案。
⑴请你帮助甲同学完善下表中的探究方案
实验步骤
观察到的现象
①在试管中取少量盐酸,插入铁丝,充分作用
________________
②在①所得溶液中,插入________,充分作用
无明显现象
③在②所得溶液中,插入________,充分作用
________________
结论:金属活动性Al>Fe>Cu
将铝丝插入溶液前应进行的操作是_________________________________________。
⑵乙同学看到甲同学的方案后,认为只要再补充一个实验,还能得出活动性Al>Fe>H>Cu的结论,乙同学要补充的实验是____________。
⑶丙同学认为要得到活动性Al>Fe>H>Cu的结论,不必补做实验,只需将甲同学方案中插入金属的顺序调整即可,调整后的金属插入顺序为____________________。
三、分析与计算,本大题包括1个小题 ,共5分
7.(5分)有关诚信食品的调查:某些不法商贩,为牟取暴利,常在味精中掺入大量食盐,以次充好,欺骗顾客。我们综合实践活动小组进行“诚信食品”研究,借助大学化学实验室,运用所学知识,探究标签所列成分含量与实际是否相符。我随机取出某种“骏马味精”(成分说明见下图),准确称取
骏马味精
配料:
谷氨酸钠(C5H7NO4Na2)80%
氯化钠(NaCl)<20%
净重: