2007届黄冈中学 启黄初三上学期期末三校联考
理科综合能力测试试题
考试时间:120分钟 分值:160分
命题人:理综备课组
说明:本试卷中用到的g值一律取10N/kg
可能用到的相对原子质量:H:1 C:12 O:16 S:32 Cu:64 Zn:65
第Ⅰ卷(选择题,共53分)
一、选择题(本题包括32小题,其中1~20小题,每小题1分,21~23小题,每小题2分,24~32小题,每小题3分,共53分。其中21~23小题有1~2个选项符合题意,其它均只有一个选项符合题意。)
11.下列变化中,都包含化学变化的一组是 ( C )
A.活性炭除去冰箱中的异味,铁锅生锈 B.米酿成醋,酒精挥发
C.动物的呼吸作用,蔬菜腐烂 D.开水沸腾,CO2用于灭火
12.下列实验装置或操作错误的是( C )
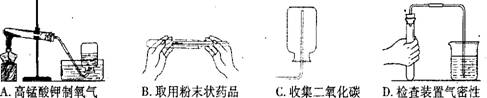
13.能够说明“分子间存在间隔”的事实是
A.空气被压缩后体积缩小
B.
C.走近花园,闻到花香 D.
14.生活中处处有化学,以下做法不合理的是
A.室内起火时,不要急于打开所有门窗
B.火灾中所处烟雾较浓时,应用湿毛巾捂住口鼻,并尽量贴近地面逃离
C.将燃气热水器安装在浴室里
D.用汽油擦洗衣服上的油污
15.下列说法不正确的是( C )
A.氢气是比天然气更理想的燃料
B.酸雨能酸化土壤,污染水体,腐蚀建筑及文物古迹,加速金属制品的锈蚀
C.使用化肥、农药不会造成水污染
D.煤、石油、天然气是不可再生能源
16.下列微粒符号中,对“
A.2Cu中的“
B.Fe2+中的“
C.Al3+ 中的“
D.Al2 (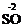 4)3 中化学式上方的“
4)3 中化学式上方的“
17.为测定铁、铜和银的金属活动性顺序,下列不能达到目的的试剂组是( b )
A.Ag,Fe,CuSO4溶液 B.Ag,FeSO4溶液,CuSO4溶液
C.Fe,Cu,AgNO3溶液 D.Cu,FeSO4溶液,AgNO3溶液
18.A、B、C三种物质各
A.5:3
B.5:
19.钨是熔点最高的金属,广泛应用于拉制灯丝,有“光明使者”的美誉。冶炼金属钨常用到白钨矿石,其主要成分是钨酸钙(CaWO4),钨酸钙中钨(W)的化合价为( )
A.-6
B.+
20.我们食用的白糖(蔗糖)的化学式为C12H22O11,以下有关它的描述错误的是( D )
A. 它是由碳、氢、氧三种元素组成
B. 它的一个分子中含有45个原子
C. 蔗糖中碳、氢、氧三种元素的质量比为72:11:88
D. 蔗糖中碳元素的质量分数为38%
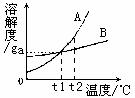 21.右图是A、B两种固体物质的溶解度曲线,下列说法正确的是(
21.右图是A、B两种固体物质的溶解度曲线,下列说法正确的是(
A.A物质的溶液,从t
B.t
C.t
D.t
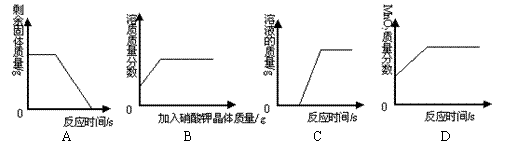
22.下列图像能正确反映所对应叙述关系的是( D )
①图A表示一定量的木炭还原氧化铜,剩余固体质量与反应时间的关系
②图B表示t℃时,向饱和硝酸钾溶液中加入硝酸钾晶体,溶质质量分数与加入量的关系
③图C表示一定量的稀硫酸与锌粒反应,溶液的质量与反应时间的关系
④图D表示一定量的KClO3和MnO2混合物加热制O2,MnO2的质量分数与时间的关系
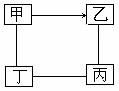
 23.下图中,“―”表示相连的物质间在一定条件下可以发生反应,“→”表示甲在一定条件下可与某种物质反应生成乙。下表四组选项中,不符合右下图要求的是
23.下图中,“―”表示相连的物质间在一定条件下可以发生反应,“→”表示甲在一定条件下可与某种物质反应生成乙。下表四组选项中,不符合右下图要求的是
 |
甲
乙
丙
丁
A
O2
CO
Fe2O3
C
B
Cu
Cu(NO3)2
Fe
O2
C
C2H5OH
CO2
Ca(OH)2
H2O
D
Fe
Fe3O4
H2
O2
第Ⅱ卷(非选择题,共107分)
化学部分
六.填空题(本题包括4小题,共22分)
45.(5分)写出符合要求的化学方程式。
(1)碳酸分解_________________________________________________________;
(2)用赤铁矿炼铁_____________________________________________________;
(3)置换反应_________________________________________________________;
(4)有氧化物生成的化合反应 __________________________________________;
(5)有碳、氢两种元素组成的燃料燃烧___________________________________.
46.(5分)能源是当今世界日益关注的热点之一。
(1)化石燃料是人类获得能量的主要来源,煤是一种化石燃料,煤的主要成分是碳,另外还含有少量硫、氮等元素,煤燃烧的产物中会造成温室效应的气体是______,会形成酸雨的主要气体是_____,易使人中毒的无色无味的气体是_______。从环保角度看,汽油和乙醇相比,较理想的燃料是______ 。乙醇可由富含淀粉的谷物发酵产生。科学家预言,未来最理想的燃料来源于绿色植物。
①绿色植物光合作用中发生的能量转化是 (填写选项序号);
A.将太阳能转化为化学能 B.将光能转化为电能
C.将化学能转化为太阳能 D.将化学能转化为热能
②使用乙醇汽油的优点有 (答出一点即可)。
(2)下列是目前正在利用和正在开发的部分能源:煤、石油、天然气、太阳能、风能、潮汐能、氢气、“可燃冰”等。回答下列问题:
①属于不可再生的能源是 ;
②通过非化学反应产生能量的能源是 ;
(3)科学家们不断研发新能源。“神舟六号”载人飞船的运载火箭所用的高能燃料是偏二甲肼(化学式为C2H8N2),在点燃的条件下,它与N2O4反应生成氮气、水和二氧化碳。该反应的化学方程式为______________________________________________________。
47.(7分)对知识的比较与归纳是学习化学的重要方法。某同学总结了O2、CO2、H2三种气体的实验室制法的化学方程式如下:
①实验室制取O2的方法之一:2KMnO4 加热 K2MnO4 + MnO2 + O2↑
②实验室制取H2的化学方程式:Zn + H2SO4 ==ZnSO4 + H2↑
③实验室制取CO2的化学方程式:_________________________
(1)通过比较这三个化学方程式发现:
①它们有许多不同之处,请指出其中一个化学方程式与另外两个的不同之处:
; ________________(答两条即可)。
②它们也有一些相似之处,请写出其中的一条: 。
(2)将实验室制取CO2和实验室用高锰酸钾制取O2进行比较,下列说法正确的是_______;实验室用高锰酸钾制取O2和实验室制取H2进行比较,下列说法正确的是_______。
A.气体发生装置可能相同 B.反应条件相同
C.气体收集方法可能相同 D.反应的基本反应类型相同
(3)该同学总结了这三种气体的制法和性质后觉得:如果有三瓶已经制得的这样的三种气体,他可以很快的、正确的鉴别出来,老师和同学对他的学习方法和精神给予了高度的赞赏,你觉得他鉴别这三种气体的方法可能是___________________________________________。
48.(5分) A、B、C、D、E是初中化学中常见的5种无色气体,其中2种是单质,3种是化合物, E是一种化石燃料
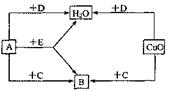 的主要成分。它们之间的转化关系如右图所示。
的主要成分。它们之间的转化关系如右图所示。
(1)写出下列物质的化学式: C _ ,D 。
实验室检验B的化学方程式为________________________
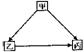 (2)已知甲、乙、丙转化关系如右下图所示(部分反应物及条件省略):
(2)已知甲、乙、丙转化关系如右下图所示(部分反应物及条件省略):
①若甲、乙组成元素相同,丙是上图中的A,则甲为(填化学式) ;
②若乙是上图中的C,甲是一种固体单质,则丙是(填化学式)____。
七.探究与实验题(本题包括1小题,共7分)
49.(7分)郭新连同学为了比较铁和银的活泼性大小,向一定量的硝酸银溶液中加入一定量的铁粉,发现溶液由无色变成了浅绿色,通过分析他得出:此实验反应的化学方程式为__________________________,且金属的活泼性是Fe?Ag。同时,他还认为反应后剩余的金属就是银。李创造同学经过分析认为剩余的金属有两种可能:①可能是银;②可能是 _________ 。李创造同学认为还可能是②的理由是______________________。于是他们将反应后的物质过滤,然后对滤出的固体进行了探究。
实验步骤
实验现象
实验结论
金属不溶解,溶液仍为无色。
猜想____正确
猜想____正确
郭新连同学还想探究Mg、Zn、Fe、Cu的活泼性大小,他通过活泼金属将不活泼金属从其化合物的溶液中置换出来的方法做了一系列的实验,得出了这四种金属的活泼性大小。李创造同学认为只需要向这四种金属中加入某种试剂,就可以比较这四种金属的活泼性大小,李创造同学认为向这四种金属中分别加入的这种试剂可能是________。
他们通过探究可以得出金属活动性顺序,而且还发现锰(Mn)也可排入金属活动性顺序中,锰(Mn)应排在Al和Zn之间,他们查资料又发现锰元素在化合物中一般显+2价,那么证明锰比银活泼的化学方程式为________ ____________ _________.
八.计算题(本题包括1小题,共5分)
50.(5分)某同学为了测定Cu-Zn合金中铜的质量分数,该同学取合金粉末
(1)该合金中铜的质量分数。 (2)反应后溶液中溶质的质量分数。