2005年青岛市中等学校招生考试
一、 选择题
1.下列是日常生活中的一些变化,其中属于物理变化的是[ ]
A.榨取果汁 B.米酿成醋
C.消化食物 D.剩饭变馊
2.在生产生活中常用到下列物质,其中属于纯净物的是[ ]
A.碘酒 B.不锈钢 C.干冰
D.牙膏
3.加油站应张贴的标志是[ ] 
4.下列物质与水混合,不能形成溶液的是[
]
A.食盐 B.植物油 C.二氧化碳
D.酒精
5.实验室常用的下列仪器中,不能用于加热的是[
]
A.试管 B.烧杯 C.量筒 D.蒸发皿
6.为了加大环保力度,许多城市的地方法规规定,不准销售和使用的物质是[ ]
A.合成纤维 B.含磷洗衣粉 C.合成橡胶
D.玻璃钢
7.目前人类所使用的能量主要来自于化学反应。下列变化中实现了由化学能转化成电能的是[ ]
A.家庭烧型煤取暖
B.在家用电器中使用干电池
C.利用海洋潮汐发电
D.电解水生成氢气和氧气
8.下列说法中,错误的是[
]
A.水是由氢元素和氧元素组成的
B.原子是构成物质的一种基本微粒
C.由同种元素组成的纯净物叫做单质
D.含有氧元素的化合物就是氧化物
9.目前从海水中提取食盐的方法主要是利用海水晒盐,它所利用的物质分离方法是[ ]
A.溶解法
B.过滤法
C.结晶法 D.蒸馏法
10.某种饮料由纯净水、蔗糖、苹果汁、维生素C、维生素A、乳酸钙等配制而成。此饮料不含有的营养素是[ ]
A.糖类
B.维生素 C.水
D.油脂
11.下列关于实验现象的描述中,错误的是[
]
A.红磷在氧气中燃烧,产生白色浓烟
B.氢气在氧气中燃烧,发出淡蓝色火焰
C.向淀粉中滴加碘水,淀粉变蓝
D.向硫酸铜溶液中滴加氢氧化钠溶液,产生白色沉淀
12.下列各组物质中,都由分子构成的是[
]
A.水、二氧化碳
B.氧气、金刚石
C.铜、食盐
D.氢气、氢氧化钠
13.现有稀硫酸、石灰水、食盐水三瓶无色溶液,只用一种试剂就能将它们一次鉴别开来的是[ ]
A.石蕊试液 B.二氧化碳 C.酚酞试液 D.氯化钡溶液
14.向盛有10mL氢氧化钠溶液的烧杯中逐滴滴加稀盐酸,下列图像能体现溶液的pH变化情况的是[ ]
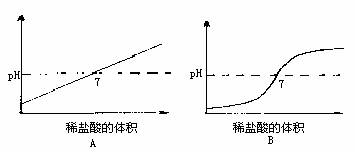
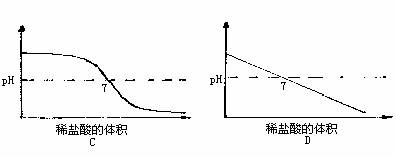
15.生产、生活实际中的下列做法,不科学的是[ ]
A.为防止自行车生锈,经常用湿抹布擦拭
B.为提高粮食产量,大量使用化肥
C.海底矿物(如可燃冰、锰结核等)虽储量丰富,也应科学规划、合理开采
D.新装修的房屋,经充分通风后再入住
16.下列物质能大量共存于水溶液中的是[ ]
A.硝酸、氢氧化钙、氯化钠
B.硝酸钾、氯化铜、硫酸铵
C.氢氧化钠、硫酸镁、氯化钡 D.盐酸、碳酸钠、硝酸钙
17.某温度下有一杯饱和的硝酸钾溶液,欲使其溶质的质量分数发生改变,下列操作可行的是[
]
A.加入一定质量的硝酸钾晶体 B.加入少量的水
C.降低温度
D.恒温蒸发溶剂
18.有关机构于
A.它是一种氧化物
B.其组成中含有氮分子
C.它的分子里C、H、N、O四种元素的原子个数比是8 : 6
: 1 : 1
D.“苏丹红一号”中C、H、N、O四种元素的质量比是48 : 3 : 7: 4
19.下表是各物质所含的少量杂质以及除去这些杂质所选用的试剂或操作方法,其中正确的是[
]
选项
物质
杂质
除杂试剂或操作方法
A
氯化钠溶液
氯化镁
加入适量烧碱溶液,再过滤
B
硝酸钠溶液
硫酸钠
加入适量氯化钡溶液,再过滤
C
熟石灰
石灰石
高温煅烧
D
二氧化碳
一氧化碳
通过澄清石灰水
20.在学习化学的过程中,及时对所学知识进行整理,是一种好的学习方法。以下归纳中,有错误的是[ ]
A.化学知识中有许多的“相等”:
原子核中质子数与中子数相等
化合物中元素化合价的正价总数与负价总数的数值相等
稀释前后溶液中溶质的质量相等
B.相似物质(或微粒)之间的区别:
氯原子和氯离子
含碳量不同
二氧化硫和三氧化硫
分子构成不同
生 铁 和 钢
最外层电子数不同
C.选择实验室制取气体装置与净化方法的依据:
发生装置
气体及所含杂质的化学性质
收集装置
反应物的状态和反应条件
净化方法
气体的密度和溶解性
D.环境问题 ―――― 主要原因 ―――――― 解决对策:
温室效应
二氧化碳
开发使用可降解塑料
水质恶化
塑 料
减少化石燃料的使用
白色污染
污水排放
先处理后排放
21.某金属加工厂生产过程中的废液含有少量硝酸银和硝酸铜,为回收利用资源和防止污染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤出的固体中加入少量稀盐酸,无气体产生。则下列有关说法中,正确的是[ ]
A.滤出的固体中一定含有银和铜,一定不含铁
B.滤出的固体中一定含有银,可能含有铜和铁
C.滤液中一定有硝酸亚铁,可能有硝酸银和硝酸铜
D.滤液中一定有硝酸亚铁,一定没有硝酸银和硝酸铜
22.实验室用食盐制纯碱的操作步骤是:(1)向浓氨水中加入足量食盐晶体制取饱和氨盐水;(2)向饱和氨盐水中通入足量的二氧化碳气体至有大量晶体析出;(3)将操作(2)中产生的晶体过滤出来;(4)将滤纸上的晶体转移至坩埚中,加热至不再有水蒸气产生,所得固体即为碳酸钠。对上述信息的有关理解中,正确的是[ ]
A.用食盐制纯碱还需要含碳元素的物质
B.食盐水比氨盐水更易吸收二氧化碳
C.室温下碳酸氢钠的溶解度比氯化铵的溶解度小,所以先结晶析出
D.在氨盐水中如果没有未溶解的食盐晶体存在,说明溶液一定不饱和
23.具备基本的化学实验技能是进行科学探究活动的基础和保证。下列有关实验操作错误的是[ ]
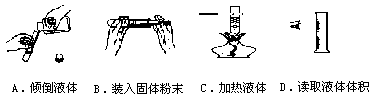
24.化学实验室通常将药品分类后存放在不同的药品柜里,现存放的部分药品如下:
药品柜
甲
乙
丙
丁
药品
硫酸、
硝酸
氢氧化钠、
氢氧化钾
汽油、
酒精
氯酸钾、金属、
高锰酸钾
实验室新购进一些盐酸,应将它存入在药品柜[
]
A.甲
B.乙
C.丙
D.丁
二、 填空题
1. 许多物质在人类的生存、日常生活和工农业生产中,有着极其广泛的用途。现有石灰石、稀硫酸、氢气、氧气、二氧化碳、天然气,请从中选出与下列用途相对应的物质,将其化学式(或主要成分的化学式)填在空白处:
(1)可供给人类呼吸的是
(2)理想的高能燃料是
(3)可用于灭火的是
(4)可用作建筑材料的是
(5)工业上可用于金属表面除锈的是
(6)我市正在推广使用、比较清洁高效的化石燃料是
2. 判断下列关于化学反应的说法是否正确,在正确说法后的横线上划“√”,在错误说法后的横线上用化学方程式举出一个否定的例子:
(1)分解反应的反应物仅有一种物质。
(2)氧化反应一定属于化合反应。
(3)生成盐和水的反应一定是中和反应。
3.现有两瓶失去标签的无色溶液,分别是硫酸钠溶液和氯化铵溶液。请你用两种不同类别的试剂鉴别它们,写出所用试剂的化学式: 、 。
4.已知A、B、C、D四种物质都含有同一种元素,其中A是单质,B是黑色固体,C是红色固体。它们之间存在着如下转化关系:
(1)A在不同条件下能够转化成B或C;
(2)A和稀硫酸反应有D生成;
(3)在高温条件下,B、C分别和无色气体E反应,都能生成A和另一种无色气体。
根据上述信息,写出下列物质的化学式:
A
; C
; D
; E
。
三 简答题
1.下表摘录了饮用天然矿泉水国家标准的部分内容:
项 目
锂
锶
锌
硒
溴化物
碘化物
硅 酸
溶解性
固体
指 标
(mg/L)
≥0.20
≥0.20
≥0.20
≥0.01
≥1.0
≥0.20
≥25.0
≥1000
请分析表中信息,回答以下问题:
(1)表中的锂、锶、锌、硒在这里是指
(填“元素”、“分子”或“原子”)。
(2)饮用天然矿泉水对人体健康有益,原因之一是矿泉水的pH与人体血液的pH相似。已知某种矿泉水的pH为7.2~7.5,该矿泉水的酸碱性为[ ]。
A.强酸性 B.弱酸性 C.强碱性
D.弱碱性
(3)有人说:“矿泉水中微量元素的含量越多越好”,你认为这种说法对吗?谈谈你的看法。
四、实验与探究题
1.请填写下列有关实验操作中的空格:
(1)点燃可燃性气体时,都要先
,再点燃。
(2)用向上排空气法收集二氧化碳时,导气管要伸到
。
(3)做铁丝在氧气中燃烧的实验时,集气瓶中应预先
。
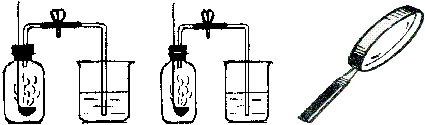
2.用来测定空气成分的方法很多,
图中所示的是用红磷在空气中燃烧的测定方法。实验过程是:
第一步:将集气瓶容积划分为五等份,并做好标记。
第二步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧。
第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸
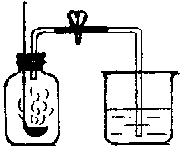
入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的1/5。
请回答下列问题:
(1)集气瓶中剩余的气体主要是 。
(2)实验完毕,若进入集气瓶中水的体积不到总容积的1/5,你认为导致这一
结果的原因可能是 、 。
(3)某同学对实验进行反思后,提出了改进方法(如图所示 ),你认为改进后的优点是: 太阳光
3.某化学活动小组以“酸碱盐的性质”为主题,进行探究学习,请你做为该小组成员来解决下列问题:
(1)小刚同学说:“酸溶液呈酸性,碱溶液呈碱性,则盐溶液一定呈中性”。你认为这种推理
(填“正确”或“不正确”),你的例证是
(2)小丽同学从某一欠收农田里取回一份土壤样品,请你用两种不同的方法帮小丽测出该土壤样品浸出液的酸碱性(只写出所用试剂的名称即可):
①
;②
。
如果检测的结果呈酸性,那么要改良此土壤,应该向农田里施加
。
(3)请你设计一个实验,能通过清晰可见的现象,除去氯化钙溶液中的少量稀盐酸。你的实验方案是(写出实验操作、现象和结论):
4.小侯同学在学习了燃烧与燃料的有关知识后,观察到家庭用的燃煤通常加工成蜂窝状,这样会燃烧得更充分。由此她联想到细铁丝在空气中不能燃烧,而在氧气中能剧烈燃烧。于是引发了思考:哪些因素能影响可燃物燃烧的剧烈程度呢?她做出两种猜想并进行了实验探究。请你回答有关问题:
(1)她提出的两种猜想是:① ;② 。
(2)请选择其中的一种猜想,设计实验加以探究(你所选择的猜想序号是 ):
实验操作
实验现象
实验结论
(3)为了使燃料能够得到充分利用,节约能源,请你结合燃料使用的实际,提出一条具体建议:
五、计算题
1.实验室中要配制
水 g。
2.某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%。为测定该产品中含碳酸钠的质量分数,进行了以下实验:取
所加盐酸的次数
第一次
第二次
第三次
第四次
烧杯及所盛物质总质量/g
181.2
204.4
228.6
253.6
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是
g。
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)