2006年山东省淄博市中考模拟试题一(理科综合)
第Ⅰ卷(选择题 共60分)
相对原子质量:H:1 C:12 N:14 O:16 Cl:35.5 Ca:40 Na:23
一、选择题:(本题共30小题,每小题给出的四个选项中只有一个是正确的,请把正确的选项涂在答题卡的相应位置上。每小题2分,错选、不选、多选均不得分)
11.铜锌合金的颜色酷似金的颜色,所以近年来用铜锌合金制成的假金元宝,欺骗行人的事件屡有发生。下列不易区别其真伪的方法是
A.测定密度 B.放入盐酸中 C.观察外观 D.在火焰上灼烧
12.空气中二氧化碳含量的增加是产生温室效应的主要原因。为了减少大气中二氧化碳的含量,下列措施不可行的是
A.提高能源的利用率 B.大量使用化石燃料
C.改进能源结构 D.提倡植树种草
13.食盐是家庭必备的调味品,它溶于水后生成Na+和Cl-。下列示意图中,能够正确表示Cl-结构的是
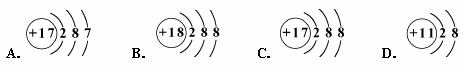
14.下表列出了不同温度下每立方厘米活性炭所能吸附的常见气体的体积,分析表中数据与气体组成、性质等的关系,你认为下列结论正确的是
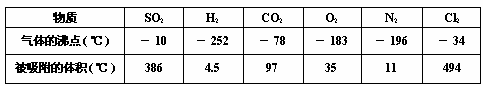
A.沸点越低的气体,越易被吸附
B.气体所含的原子数越多时,越易被吸附
C.气体是化合物时,容易被吸附
D.气体的相对分子质量越大,越易被吸附
15.2005年春季,国家质检局查出一些辣椒酱、番茄酱等食品中含有工业染色剂“苏丹红一号”,人食用后可能改癌。“苏丹红一号”的化学式为C16H12N2O,下列有关“苏丹红一号”的说法中错误的
A.“苏丹红一号”由四种元素组成
B.“苏丹红一号”一个分子由31种原子构成
C.“苏丹红一号”属于有机化合物
D.“苏丹红一号”的相对分子质量为248
16.享受生活离不开化学知识,下列有关生活常识的说法错误的是
A.用甲醛水溶液浸泡的水产品不宜食用
B.不能用工业用盐亚硝酸钠作为调味品来烹饪食品
C.冬天用煤火取暖时,要注意室内通风
D.人体缺少必需微量元素硒时,应大量食用含硒元素的营养剂
17.一定量的单质某气体其体积随压强和温度变化的原因是
A.气体分子的个数发生变化
B.气体分子本身大小发生变化
C.构成分子的原子个数发生变化
D.分子间的间隔发生变化
18.常温下,将盛有饱和KNO3溶液的试管插入盛冰水混合物的烧杯中,下列说法正确的是
A.试管中水的质量不变
B.试管内溶液的质量不变
C.硝酸钾的溶解度不变
D.试管内溶液中溶质的质量
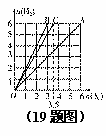
19.已知H2能在O2、Cl2中燃烧,右图中横坐标表示完全燃烧时消耗气体x(x=O2、Cl2)的分子数n(X),纵坐标表示消耗H2的分子数n(H2)。已知A、B是纯净物,C是由A和B组成的混合物,则C中n(A):n(B)为
A.2:1 B.2:3 C.2:5 D.1:1
20.已知某种食物中蛋白质的含氮量为15%,某成年人仅从该食物中摄取蛋白质,经身体内的新陈代谢后,氮元素又完全变成尿素CO(NH2)2,若测得每天排出尿素25g,则该成年人每天需从该食物中摄取蛋白质至少有
A.106g B.90.7g C.77.8g D.66.9g
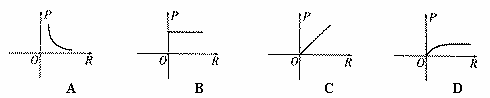
第二卷
三、本大题 包括5个小题,共28分
35.(4分)
图A的两圆分别代表酸和碱的有关信息,两圆重叠的区域表示它们的共同特征(相似点),重叠区域以外的部分表示它们的独有特征(不同点)。请你参照图A,在图下的空格内填写图B、图C中的(1)、(2)、(3)、(4)区域对应的适当内容(每处只要求填一点。)
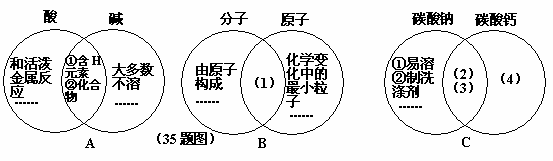
(1)_________________________(2)_________________________
(3)_________________________(4)_________________________
36.(6分)葛洪是我国晋代著名炼丹家。据史书记载:有一次葛洪之妻用铁勺盛“曾青”(硫酸铜溶液),几天后,葛洪发现了一个奇妙的现象,铁勺变成了“铜勺”,葛洪的徒弟高兴得跳起来:“点石成金啦!”葛洪把“铜勺”放在火上一烤,“铜勺”逐渐变黑。
(1)请你写出“点石成金”的化学方程式:_________________________
(2)“铜勺”逐渐变黑的原因是:_________________________
(3)葛洪的炼丹过程中常用一种名叫“黄丹”的物质。如果“黄丹”与硝酸反应的化学方程式为:黄丹+4HNO3=PbO2+2Pb(NO3)2+2H2O,请你推测“黄丹”的化学式是_________________________。
37.(7分)用天然气和水煤气(主要成分是CO和H2)代替蜂窝煤作燃料可明显改善城市空气质量,工业上用水蒸气通过赤热的碳来制取水煤气,回答下列问题:
(1)工业上制取水煤气的化学方程式为:_________________________,反应类型:___________
(2)空气质量日报中常列出的主要污染物有:①二氧化硫;②二氧化氮;③一氧化碳;④可吸入颗粒物等。用天然气或水煤气代替蜂窝煤后,上述污染物中明显降低的是________(填序号)。
(3)送入居民家中的天然气,水煤气中常加入一种有臭味的物质(硫醇),其作用是_________________________.
(4)用天然气、水煤气代替蜂窝煤作燃料,除明显改善空气质量外,还具有的优点是_________________________
38.(6分)在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸,反应中溶液的温度与加入盐酸的体积变化如下:

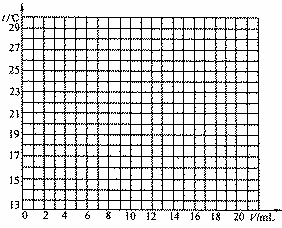
(1)试绘出溶液的温度与加入盐酸的体积之间的变化关系曲线。
(2)根据曲线讨论溶液温度变化的原因。
①加入盐酸的量在2-10mL之间时:_________________________;
②加入盐酸的量在10-20mL之间时:_________________________。
(3)若某同学提出“将氢氧化钠固体直接与10%盐酸反应,以探究中和反应是否放热”,此提议是否合理,为什么?
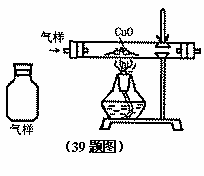
39.(5分)
接报警,某厨房的煤气管道可能有CO泄漏,一化学兴趣小组成员受命采取该厨房的气体,并检测该气样中有否含有CO气体。小组中一成员戴上防毒面具,进入厨房收集到一瓶厨房气体,他们欲用右图装置来作检测。
请回答下列问题:
(1)检测时出现_________________________现象可证明厨房气样中含有CO。
(2)小组中有成员提出该装置产生的尾气仍有可能造成环境污染,请你提出处理尾气的方法_________________________。
(3)采集气样时未携带抽气工具(如注射器等),如何用最简便的方法采到该瓶气体?
_________________________
(4)如何在检测时将瓶中的气样导入玻璃管内,请在原图中画出示意图,并用文字作必要说明。
_________________________
六、实验计算题(共14分)
45.(8分)
某学生为了测定实验室中一瓶因保存不善而部分变质的氢氧化钠中碳酸钠的质量分数,设计了如右图所示的装置(图中铁架台已略去),实验在27℃,101kPa下进行,实验步骤如下:
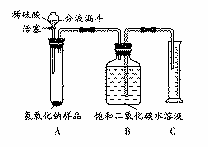
①按图连接好装置;
②用天平准确称取氢氧化钠样品2g,放入A中试管内,向B中集气瓶内倒入饱和二氧化碳水溶液至瓶颈处;
③向分液漏斗中倒入稀硫酸,打开活塞,让稀硫酸滴入试管中至过量,关闭活塞。反应结束后,量筒中收集到饱和二氧化碳水溶液220mL。
请回答下列问题:
(1)判断氢氧化钠发生变质的实验现象是_________________________;氢氧化钠变质的原因是_________________________;因此,实验室中氢氧化钠必须_________________保存。
(2)在实验步骤①和②之间,还缺少一实验步骤,该实验步骤是_________________________。
(3)B中盛装的饱和二氧化碳水溶液不能用水代替,其理由是_________________________。
(4)判断实验步骤③中滴入的稀硫酸已过量的标志是_________________________。
(5)用上述装置不能测定已部分变质的氢氧化钠样品中氢氧化钠的质量分数,理由是_________________________。
46.(6分)
将15gCaCl2溶液逐滴加入到20gNa2CO3溶液中,并测得生成沉淀的质量与滴入CaCl2溶液的质量,其关系如图所示。
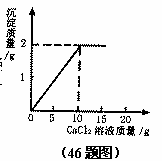
请根据题意计算:
(1)CaCl2溶液与Na2CO3溶液中溶质的质量分数之比。
(2)将反应后的物质过滤,蒸干滤液后得到固体的质量。