2006年5月北京市西城区抽样测试初三化学试卷
第Ⅰ卷(选择题 共35分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Mg-24 S-32 Cl-35.5 K-39
Ca-40 Mn-55 Fe-56 Cu-64 Zn-65 Ba-137 Hg-201
一、选择题(共35分,每小题1分。每小题只有一个选项符合题意)
1.生活中常见的下列变化,属于化学变化的是
2.某化工厂发生氯气爆炸事故后,抢险人员在疏散群众的同时,用喷雾水枪对现场喷射
稀氢氧化钠溶液,隔日现场已闻不到氯气的气味、看不到氯气的黄绿色了。下列不属
于氯气物理性质的是
A.能与氢氧化钠溶液反应 B.有刺激性气味
C.黄绿色 D.通常状况下是气体
日常生活中,我们经常饮用矿泉水。右图是某饮用天然水部分商标图,图中列出了理化指标。据此回答3~4题:

3.这里的钙、镁、钾、钠指的是
A.单质 B.原子 C.分子 D.元素
4.这种饮用天然水呈
A.酸性 B.碱性 C.中性 D.无法确定
5.下图中的事例能说明分子间的间隙变小的是

6.北京市关于限放烟花爆竹的规定为2006年春节营造了更加喜庆的节日气氛。但燃放烟花爆竹仍然会造成一些危害。以下不是燃放烟花爆竹造成的危害是
A.空气污染 B.噪音污染 C.人员炸伤 D.河流污染
7.为迎接2008奥运会,北京的空气质量备受关注。下列一组气体都是空气污染物的是
A.N2、O2、CO2 B.CO2、CO、N2 C.SO2、CO、NO2 D.CO、O2、SO2
8.厄尔尼诺现象产生的原因之一是大气中二氧化碳的含量增大,为减缓此现象,人们将选用的最理想的燃料是
A.一氧化碳 B.木炭 C.无烟煤 D.氢气
9.《科学》杂志评出2004年十大科技突破,其中“火星上‘找’到水的影子”名列第一位。这一科技突破与下列关于水的说法联系最密切的是
A.生命的孕育和维系需要水
B.水属于化合物
C.在通电条件下水能分解
D.有固、液、气三态变化
10.如果人体内的CO2不能顺利排出体外,人体血液的pH会
A.变大 B.变小
C.不变
D.先变大后变小
11.某粒子的结构示意图为 ,下列说法不正确的是
,下列说法不正确的是
A.该元素的原子核外有2个电子层
B.该元素是一种金属元素
C.该粒子是阳离子
D.该粒子具有稳定结构
12.除去一氧化碳中混有少量二氧化碳的方法是
A.将一氧化碳倒出
B.将气体点燃
C.将气体通过足量石灰水中 D.将气体通过灼热的氧化铜
13.下列物质的溶液中,能与氢氧化钠溶液反应生成蓝色沉淀的是
A.HCl B.MgCl2 C.KNO3 D.CuSO4
14.葡萄含有丰富的非金属元素硒(Se),人体如果缺硒可能会引起皮肤病变。在硒酸(化学式为H2SeO4)中,Se元素的化合价是
A.+2价 B.+3价 C.+4价 D.+6价
15.同一种元素往往能形成不同种单质,这些单质互称为同素异形体。下列各组物质互称为“同素异形体”的是
A.红磷和白磷 B.CO和CO2 C.液氧和氧气 D.石灰石和大理石
16.下列实验操作正确的是
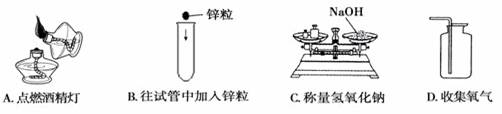
17.下列化学实验的现象正确的是
A.水在通电的条件下分解为氢气和氧气
B.白磷在空气中燃烧生成白色气体
C.铁丝在氧气中燃烧生成黑色固体
D.氢气在空气中燃烧发出耀眼白光
18.下列各组物质在溶液中能大量共存的是
A.NaOH、NaCl、HNO3
B.FeCl3、Na2SO4、HCl
C.MgSO4、NaNO3、KOH
D.Na2CO3、KNO3、HCl
19.粗盐提纯的主要操作步骤中,操作顺序正确的是
A.溶解、过滤、蒸发 B.过滤、蒸发、溶解
C.过滤、溶解、蒸发 D.溶解、蒸发、过滤
20.下列叙述正确的是
①原子由质子和中子构成 ②原子不显电性 ③原子不能再分
④原子的质子数决定元素的种类
⑤原子中质子数决定元素的化学性质
A.①⑤ B.②④ C.③④ D.①②③
21.实验室制取O2、H2、CO2这三种气体的化学反应中,不包含的基本反应类型是
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
22.下列各组物质中,按氧化物、酸、碱、盐顺序排列的是
A.干冰、碳酸、纯碱、氯化钾
B.水、硫酸、熟石灰、蓝矾
C.氧化铁、硝酸、火碱、乙醇
D.熟石灰、醋酸、氢氧化钠、食盐
23.吸毒严重危害人体健康和社会稳定,下列关于冰毒(化学式为C10H15N)的叙述正确
的是
A.完全燃烧的产物只有两种氧化物
B.C、H、N元素的质量比为10∶15∶1
C.由C、H、N三种元素组成
D.H元素的质量分数最高
24.下列物质能与盐酸反应,生成另一种酸的是
A.NaOH B.AgNO3 C.BaCl2 D.Zn
25.白色固体A由①KCl、②K2SO4、③Na2CO3、④BaCl2四种物质中的两种混合而成。将A加水搅拌,有白色不溶物,过滤后,滤液中的溶质只有KCl。则A的组成是
A.①② B.②③ C.②④ D.③④
26.t℃时,向NaCl饱和溶液中加入一定量的NaCl晶体,有关溶液变化的叙述错误的是
A.溶液仍为饱和溶液 B.溶质的质量变大
C.溶质的溶解度不变 D.溶质的质量分数不变
27.欲使稀硫酸溶液导电性实验的结果呈现右图所示的变化趋势,应在稀硫酸中加入的物质是

A.Zn B.BaCl2 C.NaOH D.Ba(OH)2
28.用以下三组物质做实验,比较锌和铜的金属活动性:
①Zn、Cu、稀硫酸;②Zn、Cu、MgSO4溶液;③Zn、Cu、AgCl。能够达到目的的是
A.① B.②③ C.①③ D.①②③
29.下列叙述不正确的是
A.铝合金比铁制品耐腐蚀的原理是:铁的化学性质比铝活泼
B.用汽油洗涤衣服上的油渍的原理是:油渍易溶于汽油
C.用含Al(OH)3的药物治疗胃酸过多的原理是:胃酸能和Al(OH)3发生中和反应
D.食醋除水垢的原理:食醋中的醋酸和水垢发生化学反应,生成可溶于水的物质
30.在化学反应A+B=C中,8 gA和20 gB充分反应,生成C的质量不可能是
A.28 g B.20 g C.12 g D.8 g
31.在一定质量的硫酸溶液中,加入氯化钡溶液,直到完全反应,生成沉淀的质量与原硫酸溶液的质量相等,则原硫酸溶液中溶质的质量分数约为
A.50% B.42.1% C.36.2% D.24.5%
32.区分下列各组物质的方法不正确的是
选项
需区分的物质
操作方法或所加试剂
A
白酒与白醋
闻气味
B
纯净水和矿泉水
观察颜色
C
火碱和纯碱
滴加稀盐酸
D
洗涤灵和洁厕灵(含盐酸)
加入石灰石
33.某混合气体可能含有N2、HCl、CO中的一种或几种。将该混合气体先通过NaOH溶液,气体体积减小;继续通过灼热的CuO粉末,产生红色物质;再将燃着的木条伸入剩余气体中,木条熄灭。假设每步反应都是完全的,下列说法正确的是
A.一定有HCl和CO,肯定无N2
B.一定有HCl和CO,可能有N2
C.一定有HCl,可能有N2和CO
D.一定有CO和N2,肯定无HCl
34.有X、Y、Z三种金属,把Y投入XCl2溶液中,Y溶解后溶液的质量增加;把X投入Z(NO3)2溶液中,X溶解后溶液的质量减少。下列判断正确的是
A. 金属活动性顺序是Y>X>Z;相对原子质量大小顺序是Y>Z>X
B. 金属活动性顺序是X>Y>Z;相对原子质量大小顺序是Y>X>Z
C.三种金属X、Y、Z可能依次是Cu、Zn、Hg
D.三种金属X、Y、Z可能依次是Hg、Zn、Cu
35.右下图中的“-”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可直接转化为戊。下面选项符合要求的是


第Ⅱ卷(非选择题 共45分)
二、填空题(36~40小题,共22分)
36.(4分)
在氧气、二氧化碳、稀硫酸、氯化钠四种物质中,
①用于抢救危重病人的一种气体单质是__________;②用于金属表面除锈的是_________;③可作为肥料施于温室中的一种气态氧化物是______;④用作食品调味剂的是__________。
37.(4分)
(1)同学都知道“木糖醇口香糖”吧?研究表明木糖醇的甜度高,溶解性好,防龋齿,一种理想的蔗糖替代品,适合糖尿病患者食用。一个木糖醇(化学式为C5H12O5)分子中含______个原子,相对分子质量为_______。
(2)下图是两种物质的溶解度曲线(m4>m3>m2>m1),请根据曲线回答下列问题:

40℃时,两种物质溶解度比较大的是_______。
30℃时,两种物质的饱和溶液中溶质的质量分数(填“相等”或“不相等”) ______。
38.(4分)
大气中的臭氧层可以阻止阳光中的紫外线对地球生物的过度照射。但是人类发明并使用氟里昂(主要用作致冷剂)若干年后,科学家发现氟里昂在紫外线照射下分解得到的氯原子能破坏臭氧层,其破坏臭氧的循环示意图如下:

(1)臭氧的化学式________,在臭氧被破坏的过程中氯原子起的是_____________作用。
(2)请写出上述循环过程中臭氧被破坏的总反应的化学方程式(1个)_________________。
(3)你从上述循环过程中你能得到哪些启示(只写一条)___________________________。
39.(5分)
A~H为初中所学的常见化合物,它们之间的相互转化关系如图所示(其中反应条件和生成物中的水已略去)。已知:A是一种建筑材料的主要成分;B是一种常见气体,H是一种含钠的化合物。
请根据上图写出:
(1) F、H的化学式:F____________、H___________。
(2) 反应A→B+C的化学方程式_________________________________________。
(3) 反应B→A的化学方程式___________________________________________。
(4)反应D→H的化学方程式___________________________________________。
40.(5分)现有A、B、C、D四种溶液,它们分别由左下表中的阴、阳离子构成,其中每一种离子只存在于一种溶液中。请根据实验记录进行推断:

(1)A是_________溶液、C是_________溶液。
(2)写出B+D→红褐色沉淀的化学方程式________________________________________。
(3)上述四种溶液的溶质,最多可以有______种在溶液中能大量共存,它们是___________
____________________________________________________________________________。
三、实验题(41~43小题,共15分)
41.(6分)
实验课上,某同学从老师提供的两瓶无标签的试剂瓶中分别取出少量固体和液体,在试管中混合,立即看到有大量无色气泡生成。大家对此实验展开一系列探究活动。
(1)请你猜想这种无色气体可能是_______,
写出生成该种气体的化学方程式_________________。
(2)按照你的猜想,请根据下列提供的实验装置回答问题:

实验室如果制取该种气体,可选的发生装置为(填序号)________,能否选用C装置收集这种无色气体(填“能”或“不能”)__________,原因是___________________________。
(3)用简便的实验方法验证你猜想的这种无色气体。(写出实验步骤、实验现象及结论)
___________________________________________________________________________。
42.(3分)
某化工厂排出的废液中含有AgNO3、Cu(NO3)2和Zn(NO3)2。为了减少废液中Ag+ 和Cu2+ 对环境的污染,并回收Ag和Cu,化学小组的同学进行了如下实验:
①向废液中加入一定量的铁粉,充分反应后过滤,得到固体和滤液;
②向滤液中滴入适量稀盐酸,有白色沉淀生成。
根据实验推断:
(1)过滤后,得到的固体是(写化学式)_____________________。
(2)滤液中的溶质是(写化学式)_____________________________________________。
(3)你认为此时同学们是否已达到实验目的,请根据你的判断请任选下表中一项填写:
能达到实验目的
理由是:
不能达到实验目的
理由是:
43.(6分)
化学实验小组的同学将一定量的Ca(OH)2溶液与Na2CO3溶液混合,充分反应后过滤,得到无色滤液,他们对滤液的成分进行了实验探究。
(1)如果滤液中只含一种溶质,则该溶质是________,请设计实验方案确认该滤液中只含一种溶质,填写实验报告。
实验步骤
实验现象
实验结论
(2)如果滤液中含有两种溶质,则溶质的组成可能有(写化学式,可不填满,也可补充)。
①___________________;②_____________________;③____________________。
选择你填的第①种组成,将其中一种溶质除去,可加入适量的试剂是_____________。
四、计算题(44~45小题,共8分,要求计算过程要规范,最后结果保留一位小数)
44.(3分)
2005年5月22日,我国测量队员完成了对珠穆朗玛峰高度的重新测定工作。测量队员冲顶时每人每分钟约消耗氧气12.8 g。若在实验室中用高锰酸钾制取相同质量的氧气,请计算需要高锰酸钾的质量。
45.(5分)
向一定量含有KCl和CaCl2的混合溶液中,逐滴加入溶质质量分数为27.6%的K2CO3溶液,所加入K2CO3溶液的质量与生成沉淀质量的关系如图所示。
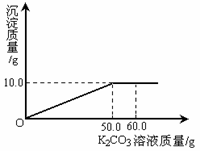
(1)恰好反应时,需K2CO3溶液的质量为_____g ;
(2)计算原混合溶液中含氯化钙的质量;
(3)若用溶质的质量分数相同的Na2CO3溶液代替上述的K2CO3溶液进行实验,计算恰好完全反应时,所消耗的Na2CO3溶液与K2CO3溶液的质量比。