2008~2009学年上学期期末安徽省怀宁中学高二化学试题
1.答题前将自己的姓名、班级、考号填写或涂在答题卡和答题卷所要求的位置上。
2.第Ⅰ卷为选择题,第Ⅱ卷为书面表达题。试卷满分100分。
3.可能用到的相对原子质量:
H
第Ⅰ卷(共60分)
一、选择题(本题包括20小题,每小题3分,共60分,每小题有1个正确答案)
1.
化二氮和偏二甲肼,C2H8N2遇N2O4后能自燃:C2H8N2+N2O4=3N2+4H2O+2CO2 。但使用这种
材料的火箭发射中对环境会产生诸多污染,下面对它可能造成的污染的分析中不正确的是
A.可能是剩余的燃料或氧化剂有毒而污染大气
B.可能是排出的NO2会破坏臭氧层w w w.ks 5u.c o m
C.不完全燃烧时会产生CO
D.可能是燃烧产生的CO2会引起温室效应
2.化学反应中通常伴随着能量变化,下列说法中错误的是
A.煤燃烧时将部分化学能转化为热能
B.电解熔融Al2O3时将部分化学能转化为电能
C.TNT爆炸时将部分化学能转化为动能
D.镁条燃烧时将部分化学能转化为光能
3.糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质。以下叙述不正确的是
A.油脂水解的产物是水和CO2 B.油脂水解可得到丙三醇
C.淀粉水解的最终产物是葡萄糖 D.蛋白质水解的最终产物是氨基酸
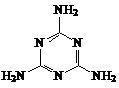 4.三聚氰胺俗称蜜胺,主要用于生产三聚氰胺一甲醛树脂。三聚氰胺微溶于冷水,易结晶,可溶于热水,低毒。在一般情况下较稳定,但在高温下可能会分解放出氰化物。其结构式如右图,下列有关说法不正确的是
4.三聚氰胺俗称蜜胺,主要用于生产三聚氰胺一甲醛树脂。三聚氰胺微溶于冷水,易结晶,可溶于热水,低毒。在一般情况下较稳定,但在高温下可能会分解放出氰化物。其结构式如右图,下列有关说法不正确的是
A.用三聚氰胺制造的餐具不可以放进微波炉中加热使用
B.该化合物属于芳香烃
C.长期摄入三聚氰胺会造成生殖、泌尿系统的损害,使膀胱、肾部结石
D.三聚氰胺呈弱碱性,可与盐酸、硫酸等酸反应形成三聚氰胺盐
5. 用铂电极电解下列溶液时,阴极和阳极上的主要产物分别是H2和O2的是
A、稀NaOH溶液 B、HCl溶液
C、饱和NaCl溶液 D、酸性AgNO3溶液
6.某烯烃与H2加成后得到2,2-二甲基丁烷,该烯烃的名称是
A.2,2-二甲基-3-丁烯 B.2,2-二甲基-2-丁烯
C.2,2-二甲基-1-丁烯 D.3,3-二甲基-1-丁烯
7.下列关于实验现象的描述不正确的是
A、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡
B、用锌片作阳极,铁片作阴极,电解氯化锌溶液,铁片表面出现一层锌
C、把铜片插入三氯化铁溶液中,在铜片表面出现一层铁
D、把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气体放出速率加快
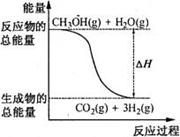 8. 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
8. 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ?mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H=-192.9kJ?mol-1
下列说法正确的是
A.CH3OH的燃烧热为192.9kJ?mol-1
B.反应①中的能量变化如右图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的△H>―192.9kJ?mol-1
9.下列关于有机物的说法正确的是
A.将甲烷通入溴水中能发生取代反应
B.乙烯双键中的一个键可以断裂,容易发生加成反应
C.乙酸是一种重要的有机酸,是一种无色无味的液体
D.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
10.下图容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是
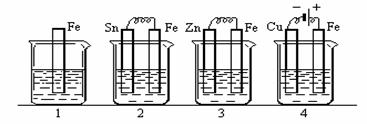
A.4>2>1>3 B.2>1>3>
11.在盛有水的电解槽中加入等物质量的Ag+,Pb2+,K+,SO42-,NO3-,Br-,然后用惰性
电极电解,通电片刻后,氧化产物和还原产物的物质的量之比为
A.1:2 B. 8:
12. 下列除去杂质的方法正确的是
① 除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离;
② 除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液、干燥、蒸馏;
③ 除去苯中混有的少量苯酚:加入浓溴水后过滤取滤液;
④ 除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
A.① ② B.② ④ C.③ ④ D.② ③
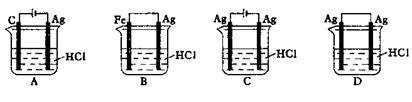
13.某同学为了使反应2HCl+2Ag
2AgCl+H2↑能进行,设计了如下图示的四个实验,
你认为可行的方案是
|
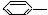 CH=CH2 推测它不可能具有下列哪种性质
CH=CH2 推测它不可能具有下列哪种性质
 气体时,电解池阴极有
气体时,电解池阴极有 不变,且溶液中有晶体析出
不变,且溶液中有晶体析出 不变;电解池中溶液
不变;电解池中溶液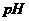 变大
变大 Fe(OH)2+Ni(OH)2
Fe(OH)2+Ni(OH)2  H= +2165 kJ/mol
H= +2165 kJ/mol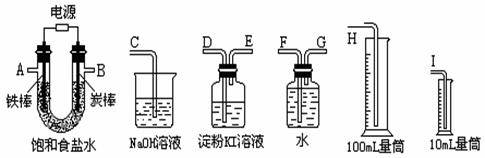 25.(8分)现需设计一套实验装置来电解饱和食盐水,并测量电解产生的氢气的体积约
25.(8分)现需设计一套实验装置来电解饱和食盐水,并测量电解产生的氢气的体积约
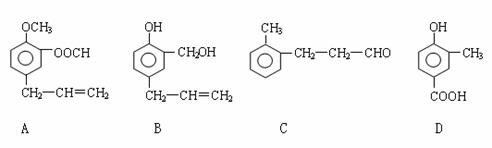

 (2)是。
(2)是。

