如何应用讨论法解题
文/杨基鄂
??一、讨论法的涵义
??讨论法是化学计算中的一种常用方法。这种方法多用于计算题在缺乏条件,求解时一个方程中出现几个未知数以及一些用字母表示的过量计算,不能得到定解时需要在分析推理的基础上通过某些假设条件,加以讨论才有定解。
??二、讨论法解题的一般思路
??用讨论法解计算题,先要分析条件与求解问题之间的联系,建立讨论模型,然后形成解题的方法。如列出二元一次方程或写出并列的各个化学方程式(或离子方程式)等,按顺序分析排查,确定答案。现举例加以说明。
??三、讨论法的解题方法
??例1.某金属氧化物的式量为M,该金属同种价态的氯化物的式量为N,则该金属元素的化合价为( )。
??A.(2N-M)/55 B.[2(N-M)]/55
??C.(2M-N)/55 D.[2(M-N)]/55
??解:设该金属相对原子质量为A,化合价为x。
??(1)当x为奇数时,有R2Ox,RClx。
则有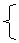
2a+16x=M
①
a+35.5x=N
②
??解得?55x=2N-M,
x=(2N-M)/55
??(2)当x为偶数时,有RO(x/2),RClx。
则有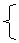
a+8x=M
①
a+35.5x=N
②
??解得 27.5x=N-M
??x=(N-M)/27.5=[2(N-M)]/55
??故选A、B。
??例2.已知2A+3B=6C+D式中A是含X、Y两种元素的化合物,B是只含Z元素的单质,C和D均是双原子分子。试确定A、B、C、D的化学式。
??解:设A的化学式为XaYb,B的化学式为Ze,则原式可改写为:2YaYb+3Ze=6C+D,按原子守恒定律:2(a+b)+3e=2×6+2=14
??整理后得:a+b+(3/2)e=7,a、b、e为正整数,e=2。
??若e=2,得a=4-b。
??讨论:(1)当b=1,a=3?则:
??2X3Y+3Z2=6XZ+Y2
??即A为X3Y,B为Z2,C为XZ,D为Y2符合题意。
??(2)当b=2,a=2,则2X2Y2中X、Y两元素都只有4个原子,不能形成C分子,不合题意,故舍去。
??(3)当b=3,a=1,则:
??2XY3+3Z2=6YZ+X2
??即A为XY3,B为Z2,C为YZ,D为X2符合题意。
??答:略
??例3.在
??解:设气态烯烃分子式为CNH2N,体积分数为x。
? CNH2N+(3/2)NO2 NCO2+NH2O ?ΔV增加
NCO2+NH2O ?ΔV增加
?? x ?? 1.5nx ? 2nx? 0.5nx-x
?? 2CO+O2 2CO2 ? ?ΔV减少
2CO2 ? ?ΔV减少
?? 1-x ?? ?? ??(1-x)/2
??概括反应前后体积不变,即体积守恒:
??则有?0.5nx-x=(1-x)/2,nx-x=1,x=1/(N-1)。
??讨论:(1)当N=2时,x=1。乙烯C2H4占100%,CO为0。
??(2)当N=3时,x=(1/2)。C3H6和CO各占50%。
??(3)当N=4时,x=(1/3)。C4H8占33.3%,CO占66.7%。
??答:该烯烃可能的分子式及体积分数分别为:
??C2H4占100%,C3H6占50%,C4H8占33.3%。?
??例4.某气态烃与O2的混合气体,在一密闭容器中完全燃烧(设反应前后温度相同且高于
??解:据阿伏加德罗定律的推论:(p1/p2)=(N1/N2)
??设该烃为CxHy,本题为等压,故N1=N2。
?? CxHy+[x+(y/4)]O2 xCO2+(y/2)H2O
xCO2+(y/2)H2O
?? 1mol [x+(y/4)]mol xmol (y/2)mol
??依题意 1+x+(y/4)=x+(y/2),解得:y=4。
??讨论:(1)当x=1、y=4为甲烷CH4
??(2)当x=2、y=4为乙烯C2H4
??(3)当x=3、y=4为丙炔或丙二烯C3H4
??(4)当x=4、y=4为乙烯基乙炔C4H4
??答:该气态烃可能为CH4、C2H4、C3H4、C4H4。
??此类型的题在高考和竞赛题中可经常碰到,解题过程对训练学生的思维能力、想像能力和知识的运用能力都很有帮助,因而在教学中应予以足够的重视。