2009年息县九年级化学第一次调研试题
注意事项:
1、 本试卷4页,满分50分,考试时间50分钟。
2可能用到的相对原子质量:H: 1 O:
题号
一
二
三
四
总分
得分
得分
评卷人
一、选择题:(每小题只有一个正确答案,请将正确答案的序号填入题后括号内。每小题1分,共计12分)
1、下列现象中有一种变化与其他变化不同的是 ( )
A、蜡烛照明 B、电灯照明 C、干冰升华 D、铁块拉成铁丝
2、食品安全与人体健康密切相关。下列做法不会 损坏人体健康的是 ( )
A、用甲醛水溶液浸泡水产品 B、用含碳酸氢钠的发酵粉焙制糕点
C、用霉变花生制成压榨花生油 D、用含NaNO2的工业用盐腌制食品
3、物质的用途与性质密切相关。下列说法中正确的是 ( )
A、洗涤剂常用来洗涤油污,是因为洗涤剂具有乳化作用
B、浓硫酸在实验室中常作干燥剂,是因为它具有腐蚀性
C、固体NaOH在实验室里常作气体干燥剂,所以它可以干燥二氧化碳和氯化氢气体
D、在铁制品表面涂抹“银粉”(实际上是铝粉)可以防止它生锈,是因为铝的活动性没有铁的活动性强。
4、下列实验操作不正确的是 ( )
A、将烧碱放在已知质量的烧杯里用托盘天平称量
B、将试管夹从试管底部往上套,夹在试管的中上部
C、滴加液体时,胶头滴管的尖端不能触及已加过其他试剂的试管内壁
D、为了避免酒精洒出,酒精灯内的酒精越少越好
5、下列说法或做法音正确的是 ( )
A、将废弃的塑料集中到野外焚烧
B、为了提高农作物的产量,施用的化肥越多越好
C、合金的很多性能一般比组成它们的纯金属更好
D、所有物质的溶解度都是随着温度的升高而增大
6、被蚂蚁、蚊虫叮咬后人会感觉痛痒,这是由于昆虫分泌出的酸性物质有刺激作用,该酸性物质的主要成分是甲酸(CH2O2)。下列有关说法正确的是 ( )
A、甲酸溶液能使酚酞试液变红色
B、甲酸中碳、氢、氧三种元素的质量比为6:
C、甲酸由1个碳原子、2个氢原子和2氧原子构成
D、可选用浓氢氧化钠溶液等碱性物质来涂抹患处
7、手电筒中使用的锌―锰干电池,在工作时反应的化学方程式为:Zn + 2NH4Cl + 2MnO2
==== ZnCl2 + 2NH3 + X + H2O, 则X的化学式为 ( )
A、MnO B、Mn3O
8、下列的说法或做法正确,且化学方程式书写正确的是 ( )
A、用稀盐酸除去铁铁制品表面的铁锈: FeO + 2HCl ==== FeCl2 + H2O
B、用稀硫酸除去试管内壁上附着的铜: Cu + H2SO4 ==== CuSO4 + H2↑
C、配制硝酸银溶液不能使用铜制容器: Cu + 2AgNO3 ==== Cu(NO3) + 2Ag
D、实验室里用碳酸钠与稀盐酸反应制二氧化碳:NaCO3 + HCl === NaCl + CO2↑+H2O
9、下列鉴别物质的方法中,切实可行的是 ( )
A、用水鉴别NaOH固体和CaCO3固体 B、用燃烧的木条鉴别CO2和N2
C、用酚酞溶液鉴别NaCl和稀盐酸 D、用石蕊溶液鉴别稀盐酸和稀硫酸
10、现有Fe、NaOH溶液、CuSO4溶液、稀H2SO4四种物质,两两混合后能发生的反应共有 ( )
A.5个 B.4个 C.3个 D.2个
11、逻辑推理是化学学习中常用的思维方法。下列推理正确的是 ( )
A、化合物都是由不同种元素组成的,不同元素组成的纯净物一定是化合物
B、酸与碱反应生成盐和水,所以生成盐和水的反应一定是酸与碱的反应
C、置换反应中有单质生成,有单质生成的反应一定属于置换反应
D、有机物都含有碳元素,所以含有碳元素的化合物都是有机物
12、下列各组中的物质完全反应后,形成溶液的质量跟反应前溶液的总质量相等的是( )
A、碳酸氢钠溶液和稀硫酸 B、碳酸钠溶液和氯化钡溶液
C、铁锈和稀盐酸 D、氢氧化钾溶液和稀硫酸
得分
评卷人
二、填空题(本题包括6个小题,每空1分,共计16分)
13、人体缺少常量元素和必需微量元素都能引起疾病。请你各举出一例,人体缺少某种常量元素引起的疾病有 ,人体缺少某种微量元素引起的疾病有 。
14通过近一年的化学学习,我们认识了酸、碱、盐三类物质。请你写出一种铵盐的化学式 ,用化学方程式表示检验该铵盐的化学方法 。
15、学完溶液知识后,小明同学回家用蔗糖、洗洁精、花生油、大理石和水相互混合做了几个家庭小实验。
(1)、在同一条件下,蔗糖易溶于水,难溶于花生油;大理石不溶于水,也不溶于花生油,由此说明物质的溶解能力与 有关。
(2)、除(1)中的因素外,你认为固体物质的溶解能力还与 有关。请你举出一个生活中常见的例子,如 。
16、现有H、C、S、O、K五种元素,请你选择适当的元素组成物质完成下列问题。
(1)、写出一种酸和一种碱反应的化学方程式: 。
(2)、写出一种金属氧化物和酸反应的化学方程式: 。
(3)、写出一种非金属氧化物和碱反应的化学方程式: 。
17、实验是进行科学探究的重要手段。请根据图示回答:
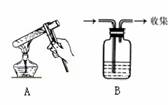 (1)图A中的错误是___________________________。
(1)图A中的错误是___________________________。
(2)若用图B装置除去CO2中混有的水蒸气,则应盛放的液体是____________。
(3)若用图B的装置来收集CH4 气体,则CH4应从左导管进还是从右导管进 。
18、欲除去下列物质中的杂质(括号中的物质为杂质),请将所选用试剂的化学式填写在横线上。
(1)Cu (Fe) __________; (2)NaOH [Ca(OH)2]______ ;
(3)NaNO3 (NaCl)_____________;
得分
评卷人
三、简答题(本题包括4个小题,共计12分)
19、(3分)牙膏的主要成份中含有精制的碳酸钙粉未,它是由石灰石经分解、化合等方法制得的,试写出生产过程中依次发生反应的化学方法式
20、(3分)取标有A、B、C、D标签的四支试管,分别加4ml、3ml、2ml、1ml的水,再分别滴加2滴盐酸,振荡后,测定它们的pH 。
(1)、推测这四种溶液的pH从大到小的顺序是。
(2)、请你简述用pH试纸测定溶液pH的方法。
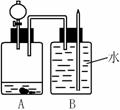
21、(3分)右图是某同学设计的趣味实验装置,其气密性良好。
(1)若B中尖嘴导管处有“喷泉”(即B中玻璃管有水向上喷)产生,请推测A中的固体物质和液体物质可能是什么?(要求:写出两组不类别物质组合即可)
(2)若要使B中的水倒流入A中,A中的分液漏斗和集气瓶中可分别盛放相应的物质才能发生,请用化学程式表示其原因。
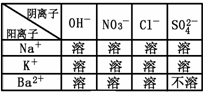 22、(3分)下表是部分物质的溶解性表(
22、(3分)下表是部分物质的溶解性表(
(1)NaOH和Ba(NO3)2两种溶液混合后能否发生反应?理由是什么?
(2)写出一个有BaSO4生成的复分解反应的化学方程式。
得分
评卷人
四、综合应用题(10分)
23、李明同学设计了两种以铁、氧化铜、稀硫酸为原料制取金属铜的方法。(已知:H2 + CuO ==== Cu +H2O)
(1)、第一种方法的实验过程中有蓝色溶液产生,你认为李明同学应选用下述装置中的(填装置的的序号____________。
(2)、第一种方法的实验过程中,为了缩短反应的时间,必需加快化学反应速率。你认为李明同学采取加快反应速率的措施是: 。
(3)、写出第一种方法中有关的反应化学方程式
。
(4)用这两种方法制得铜中都可能含有杂质。则第二种方法制得的铜中,可能含有的杂质是: 。
(5)若用这两种方法制取铜的质量相等,下列叙述符合实际实验结果的是 。
A、消耗氧化铜的质量相等 B、消耗铁的质量相等
C、消耗硫酸的质量相等 D、生成硫酸亚铁的质量不相等
(6)、取用第二种方法制得的铜样品(含杂质)
一、选择题(每小题1分,共计12分)
题号
1
2
3
4
5
6
7
8
9
10
11
12
答案
A
B
A
D
C
B
C
C
A
B
A
D
二、填空题(每空1分,共计16分)
13、缺钙会得佝偻病、骨质疏松;缺铁会引起贫血(其他合理答案均可)
14、NH4Cl或(NH4)2SO4或NH4HCO3等;
NH4Cl + NaOH ==== NaCl + NH3↑+ H2O (其他合理答案均可)
15、(1)、溶剂和溶质的性质
(2)、温度;蔗糖在热水中比在冷水中溶解的多(其他合理答案均可)
16、(1)、2KOH + H2SO4 ==== K2SO4 + 2H2O
(2)、K2O + H2SO4 ==== K2SO4 + H2O
(3)、CO2 + 2KOH ==== K2CO3 + H2O (其他合理答案均可)
17、(1)试管所盛液体超过其容积的1/3(或手握试管夹位置不对等)
(2)浓硫酸
(3)、从右导致管进。
18、(1)、稀HCl或稀H2SO4 等(2)、Na2CO3或NaHCO3
(3)、AgNO3 (其他合理答案均可)
三、简答题(本题包括4个小题,共计12分)
19、(1)、CaCO3 ==== CaO + CO2 ↑;(2)、CaO + H2O ==== 、Ca(OH)2 ;
(3)、Ca(OH)2 + CO2 ==== CaCO3↓+ H2O;(每个方程式1分,按中招要求评判)
20、(1)、A?B?C?D (1分)
(2)、用玻璃棒分别蘸取四种溶液,滴在pH试纸上(1分);然后将显示的颜色与标准比色对比(1分)。
21、(1)、锌和稀盐酸;双氧水和二氧化锰等(其他合理答案均可)(每组1分)
(2)、CO2 + 2NaOH ==== Na2CO3 + H2O (其他合理答案均可)(1分,评判标准同上)
22、(1)、不能(1分) ; 没有沉淀、气体或水生成(或不符合复分解反应发生的条件)(1分)
(2)、Na2SO4+Ba(OH)2=BaSO4↓+2NaOH(其他合理答案均可)(1分)
四、综合应用题(10分)
23、(1)B、C ;(2)加热反应物;(3) CuO + H2SO4 ==== CuSO4 + H2O ; CuSO4 + Fe ====FeSO4 + Cu ; (4)氧化铜 ;(5) A、D ;(每空1分)
(6)设
.CuO + H2SO4 ==== CuSO4 + H2O
80 98

X =
所以稀硫酸中溶质的质量分数为: (1分)
(1分)
答:略