题目内容
一个半径为0.1 cm的气泡,从18 m深的湖底上升,如果湖底水的温度是8 ℃,湖面的温度是24 ℃,湖面的大气压强是76 cmHg,那么气泡升至湖面时体积是多少?
0.012 cm3.
气泡从湖底上升过程中气泡的温度随上升而升高,可认为是水的温度.另外,气泡的压强和体积也发生变化.先确定初、末状态,再应用理想气体状态方程进行计算.此题的关键是确定气泡内气体的压强.
由题意可知
V1= πr3=4.19×10-3 cm3
πr3=4.19×10-3 cm3
p1=p0+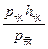 =76+
=76+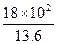 cmHg="208" cmHg
cmHg="208" cmHg
T1="273+8" K="281" K
p2="76" cmHg
T2="273+24" K="297" K
根据理想气体的状态方程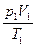 =
=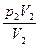 得
得
V2=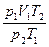 =
=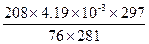 cm3="0.012" cm3.
cm3="0.012" cm3.
由题意可知
V1=
 πr3=4.19×10-3 cm3
πr3=4.19×10-3 cm3p1=p0+
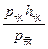 =76+
=76+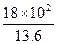 cmHg="208" cmHg
cmHg="208" cmHgT1="273+8" K="281" K
p2="76" cmHg
T2="273+24" K="297" K
根据理想气体的状态方程
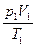 =
=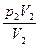 得
得V2=
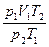 =
=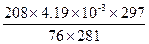 cm3="0.012" cm3.
cm3="0.012" cm3.
练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
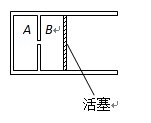
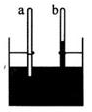


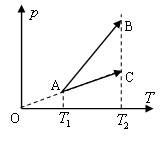
 .当阀门
.当阀门 闭锁时,三个恒温箱内气体状态分别如图所示,大气压强恒为P0.今将阀门
闭锁时,三个恒温箱内气体状态分别如图所示,大气压强恒为P0.今将阀门