题目内容
一定质量的理想气体,在经过等压膨胀、等容降温、等压压缩、等容升温四个过程后回到初始状态,它是吸热还是放热?
吸热
解法一:由于一定质量的理想气体的内能是否变化决定于温度是否发生了变化,所以经过一个循环后回到初始状态,内能不变,即ΔU=0。由热力学第一定律ΔU=W+Q可知,它是吸热还是放热,取决于外界对它的做功情况。以下对在每个过程中外界对气体做功W的情况逐个分析:
等压膨胀:气体压强为p1,体积增大了ΔV1,则W1=-p1ΔV1;
等容降温:体积不变,所以W2=0。
等压压缩:气体压强为p2,体积减小了ΔV2,则W3=p2ΔV2。
等容升温:体积不变,所以W4=0。
外界对气体做的总功为W=W1+W2+W3+W4=-p1ΔV1+p2ΔV2
由于p1>p2,ΔV1=ΔV2,所以W<0,代入
ΔU=W+Q得Q>0,即气体吸热。
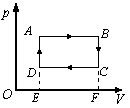
解法二:用图线直观地反应气体的状态变化。对本题作p-V图线如图所示,气体从A状态经过一个循环回到状态A。由p-V图线可以看出,在等温膨胀过程A-B中,气体对外做的功等于矩形ABFE的面积;在等压压缩过程C-D中,外界对气体所做的功等于矩形CDEF的面积。整个循环气体对外做的功等于矩形ABCD的面积。气体内能不变,对外做功,必然吸热。而且气体所吸收的热量也等于矩形ABCD的面积。
等压膨胀:气体压强为p1,体积增大了ΔV1,则W1=-p1ΔV1;
等容降温:体积不变,所以W2=0。
等压压缩:气体压强为p2,体积减小了ΔV2,则W3=p2ΔV2。
等容升温:体积不变,所以W4=0。
外界对气体做的总功为W=W1+W2+W3+W4=-p1ΔV1+p2ΔV2
由于p1>p2,ΔV1=ΔV2,所以W<0,代入
ΔU=W+Q得Q>0,即气体吸热。
解法二:用图线直观地反应气体的状态变化。对本题作p-V图线如图所示,气体从A状态经过一个循环回到状态A。由p-V图线可以看出,在等温膨胀过程A-B中,气体对外做的功等于矩形ABFE的面积;在等压压缩过程C-D中,外界对气体所做的功等于矩形CDEF的面积。整个循环气体对外做的功等于矩形ABCD的面积。气体内能不变,对外做功,必然吸热。而且气体所吸收的热量也等于矩形ABCD的面积。


练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
