题目内容
(2009?山东)一定质量的理想气体由状态A经状态B变为状态C,其中A→B过程为等压变化,B→C过程为等容变化.已知VA=0.3m3,TA=TC=300K、TB=400K.
(1)求气体在状态B时的体积.
(2)说明B→C过程压强变化的微观原因
(3)设A→B过程气体吸收热量为Q,B→C过程气体放出热量为Q2,比较Q1、Q2的大小说明原因.
(1)求气体在状态B时的体积.
(2)说明B→C过程压强变化的微观原因
(3)设A→B过程气体吸收热量为Q,B→C过程气体放出热量为Q2,比较Q1、Q2的大小说明原因.
分析:(1)A→B过程为等压变化,根据盖--吕萨克定律可求出气体在状态B时的体积.
(2)气体的压强在微观上来看,与气体分子的密集程度和气体分子的平均动能有关.所以要解释气体压强变化,只要分析出在等容变化过程中气体分子的密集程度和气体分子的平均动能的变化.
(3)根据热力学第一定律△U=W+Q,气体内能变化与温度有关,A、C两状态的温度相同,可知A→B增加的内能与B→C减小的内能相同,然后通过做功的情况比较出吸热与放热的大小.
(2)气体的压强在微观上来看,与气体分子的密集程度和气体分子的平均动能有关.所以要解释气体压强变化,只要分析出在等容变化过程中气体分子的密集程度和气体分子的平均动能的变化.
(3)根据热力学第一定律△U=W+Q,气体内能变化与温度有关,A、C两状态的温度相同,可知A→B增加的内能与B→C减小的内能相同,然后通过做功的情况比较出吸热与放热的大小.
解答:解:(1)设气体在B状态时的体积为VB,由盖--吕萨克定律得,
=
,代入数据得VB=0.4m3.
(2)微观原因:气体体积不变,分子密集程度不变,温度变小,气体分子平均动能减小,导致气体压强减小.
(3)Q1大于Q2;因为TA=Tc,故A→B增加的内能与B→C减小的内能相同,而A→B过程气体对外做正功,B→C过程气体不做功,由热力学第一定律可知Q1大于Q2
| VA |
| TA |
| VB |
| TB |
(2)微观原因:气体体积不变,分子密集程度不变,温度变小,气体分子平均动能减小,导致气体压强减小.
(3)Q1大于Q2;因为TA=Tc,故A→B增加的内能与B→C减小的内能相同,而A→B过程气体对外做正功,B→C过程气体不做功,由热力学第一定律可知Q1大于Q2
点评:解决本题的关键是熟练运用气体定律和热力学第一定律.

练习册系列答案
相关题目
 (2009?山东)如图所示,一导线弯成半径为a的半圆形闭合回路.虚线MN右侧有磁感应强度为B的匀强磁场.方向垂直于回路所在的平面.回路以速度v向右匀速进入磁场,直径CD始终与MN垂直.从D点到达边界开始到C点进入磁场为止,下列结论正确的是( )
(2009?山东)如图所示,一导线弯成半径为a的半圆形闭合回路.虚线MN右侧有磁感应强度为B的匀强磁场.方向垂直于回路所在的平面.回路以速度v向右匀速进入磁场,直径CD始终与MN垂直.从D点到达边界开始到C点进入磁场为止,下列结论正确的是( )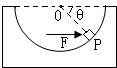 (2009?山东)如图所示,光滑半球形容器固定在水平面上,O为球心,一质量为m的小滑块,在水平力F的作用下静止P点.设滑块所受支持力为FN.OF与水平方向的夹角为θ.下列关系正确的是( )
(2009?山东)如图所示,光滑半球形容器固定在水平面上,O为球心,一质量为m的小滑块,在水平力F的作用下静止P点.设滑块所受支持力为FN.OF与水平方向的夹角为θ.下列关系正确的是( ) (2009?山东)如图所示,某货场而将质量为m1=100kg的货物(可视为质点)从高处运送至地面,为避免货物与地面发生撞击,现利用固定于地面的光滑四分之一圆轨道,使货物中轨道顶端无初速滑下,轨道半径R=1.8m.地面上紧靠轨道次排放两个完全相同的木板A、B,长度均为L=2m,质量均为m2=100kg,木板上表面与轨道末端相切.货物与木板间的动摩擦因数为μ1,木板与地面间的动摩擦因数μ=0.2.(最大静摩擦力与滑动摩擦力大小相等,取g=10m/s2)求:
(2009?山东)如图所示,某货场而将质量为m1=100kg的货物(可视为质点)从高处运送至地面,为避免货物与地面发生撞击,现利用固定于地面的光滑四分之一圆轨道,使货物中轨道顶端无初速滑下,轨道半径R=1.8m.地面上紧靠轨道次排放两个完全相同的木板A、B,长度均为L=2m,质量均为m2=100kg,木板上表面与轨道末端相切.货物与木板间的动摩擦因数为μ1,木板与地面间的动摩擦因数μ=0.2.(最大静摩擦力与滑动摩擦力大小相等,取g=10m/s2)求: (2009?山东)(1)历史中在利用加速器实现的核反应,是用加速后动能为0.5MeV的质子11H轰击静止的X,生成两个动能均为8.9MeV的24He.(1MeV=1.6×-13J)
(2009?山东)(1)历史中在利用加速器实现的核反应,是用加速后动能为0.5MeV的质子11H轰击静止的X,生成两个动能均为8.9MeV的24He.(1MeV=1.6×-13J)