题目内容
根据玻尔理论,氢原子的电子由外层轨道跃迁到内层轨道后
A.原子的能量增加,电子的动能减少
B.原子的能量增加,电子的动能增加
C.原子的能量减少,电子的动能减少
D.原子的能量减少,电子的动能增加
D
解析:
根据玻尔理论原子的能级公式为En=![]() ,从外层轨道跃迁到内层轨道,量子数由大变小,所以原子的能量减少.原子减少的能量以光子的形式辐射出去.
,从外层轨道跃迁到内层轨道,量子数由大变小,所以原子的能量减少.原子减少的能量以光子的形式辐射出去.
由于原子核对电子的库仑力为电子绕核做匀速做圆周运动的向心力.根据牛顿第二运动定律、库仑定律和向心加速度公式,有: ![]() ,
,
又根据玻尔理论的轨道公式: rn=n2 r1.
综合上述公式可知,电子在轨道上运动时的动能为:![]() .
.
当轨道量子数减少时,电子的动能增加.
此题涉及原子能量、电子动能和势能两方面问题.玻尔应用量子化假设很好地解释了氢原子能级(能量)问题.氢原子只能处于一些不连续的能量状态,这些能量状态与核外电子沿不同的圆形轨道绕核运转(动能+势能)相对应.量子数为n(对应电子在第n条轨道上)的氢原子能量为![]() .氢原子由于吸收或辐射光子而使能量改变时,能量的改变不能是任意的,只能为两个能级之差.当氢原子核外电子从高能级向低能级(从n较大的高轨道向n较小的低轨道)跃迁时,氢原子辐射光子能量后
.氢原子由于吸收或辐射光子而使能量改变时,能量的改变不能是任意的,只能为两个能级之差.当氢原子核外电子从高能级向低能级(从n较大的高轨道向n较小的低轨道)跃迁时,氢原子辐射光子能量后![]() 减少;电子动能
减少;电子动能![]() (速度)增加;电场力对电子做正功,电子的电势能减少.
(速度)增加;电场力对电子做正功,电子的电势能减少.
在分析核外电子动能变化时,一些考生把电子绕氢原子核运转与行星运转规律相类比,以为电子跃迁到不同轨道上绕氢原子核运转过程中能量守恒,电子从较高轨道跃迁到较低轨道过程中,总能量不变,动能则增加,这样理解是不对的.还有的同学死套公式最容易出现以下的错误:从外层轨道跃迁到内层轨道,量子数由大变小,n2减小,根据En=![]() ,原子的能量增加.这样做错误的直接原因是忘记了原子能量的规定:设电子距离原子核无限远处时为原子的能量零点,在各层轨道上原子的能量均为负值.
,原子的能量增加.这样做错误的直接原因是忘记了原子能量的规定:设电子距离原子核无限远处时为原子的能量零点,在各层轨道上原子的能量均为负值.

| A、根据玻尔理论,氢原子在辐射光子的同时,轨道也在连续地减小 | B、放射性物质的温度升高,则半衰期减小 | C、用能量等于氘核结合能的光子照射静止氘核,不可能使氘核分解为一个质子和一个中子 | D、某放射性原子核经过2次α衰变和一次β衰变,核内质子数减少3个 | E、根据玻尔理论,氢原子的核外电子由较高能级跃迁到较低能级时,要释放一定频率的光子,同时电子的动能增大,电势能减小. |
 ”形的光滑长直导轨槽,槽口向上(图为俯视图).槽内放置一个木质滑块,滑块的左半部是半径为R的半圆柱形光滑凹槽,木质滑块的宽度为2R,比“
”形的光滑长直导轨槽,槽口向上(图为俯视图).槽内放置一个木质滑块,滑块的左半部是半径为R的半圆柱形光滑凹槽,木质滑块的宽度为2R,比“ ”形槽的内侧宽度略小.现有一半径为r(r<<R)的金属小球以水平初速度v0冲向滑块,从滑块的一侧半圆形槽口边缘进入.已知金属小球的质量为m,木质滑块的质量为5m,整个运动过程中无机械能损失.求:
”形槽的内侧宽度略小.现有一半径为r(r<<R)的金属小球以水平初速度v0冲向滑块,从滑块的一侧半圆形槽口边缘进入.已知金属小球的质量为m,木质滑块的质量为5m,整个运动过程中无机械能损失.求: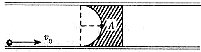
 (2011?黄冈模拟)根据玻尔理论,氢原子核外电子绕原子核的运动与卫星绕地球的匀速圆周运动极为相似,运动图景如图所示.图中,涂黑的圆表示氢原子核或地球,圆a,b表示的是氢原子的核外电子或地球卫星的可能轨道.下列对比中正确的是( )
(2011?黄冈模拟)根据玻尔理论,氢原子核外电子绕原子核的运动与卫星绕地球的匀速圆周运动极为相似,运动图景如图所示.图中,涂黑的圆表示氢原子核或地球,圆a,b表示的是氢原子的核外电子或地球卫星的可能轨道.下列对比中正确的是( )