题目内容
【题目】下图是某水库生态系统的食物网,图中A、B、C和D代表四个不同物种的鱼。回答下列问题。
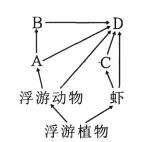
(1)B和D的种间关系是____。作为一个完整的生态系统,图中缺少的生物成分是____,该成分在生态系统中的作用是____。
(2)调查发现,小个体的D主要以虾、浮游动物为食,大个体的D主要以A、B和C为食,这在一定程度上缓解了____的剧烈程度,有利于D的生存。
(3)研究发现,在蓝藻浓度较高时,D更多地以鱼类为食,从而能抑制水华发生。水华发生被抑制的原因是____。
【答案】捕食、竟争 分解者 将动植物遗体和动物的排遗物分解成无机物 种内斗争 D 更多地以鱼类为食会使得浮游动物、虾增加,从而增加了对浮游植物的摄食,由此抑制水华
【解析】
生态系统的结构包括生态系统的组成成分和营养结构;由某水库生态系统的食物网简图可知,A、B、C、D均为鱼类,为不同级别的消费者,图中只列出了生产者和各级消费者,未列出的该生态系统的成分是非生物的物质和能量、分解者。
(1)据图可知,B和D均以A为食物,两者之间存在竞争关系,同时D捕食B,两者之间也有捕食关系;一个完整的生态系统中生物成分包括生产者、消费者和分解者,图中缺少分解者;分解者在生态系统中的作用是将动植物遗体和动物的排遗物分解成无机物。
(2)调查发现,D鱼的大小个体捕食对象不同,可以更为充分的利用资源,这在一定程度上可以缓解D种内斗争的剧烈程度,有利于D的生存。
(3)据图示食物网关系可知:若D 更多地以鱼类为食,鱼类数目减少会使得浮游动物、虾的数量增加增加,从而增加了对浮游植物的摄食,由此可以抑制水华。

【题目】为研究低温胁迫对水稻生长的影响,科研人员进行相关研究,结果如下表所示。
光合色素(mg/L) | 气孔导度(μmol m 2 s-1) | 光合速率(μmol m 2 s-1) | 胞间CO2浓度(μL/L) | |
3°C处理 | 8.9 | 0.13 | -0.35 | 454.5 |
正常培养 | 26 | 0.3 | 0.5 | 316 |
注:气孔导度指气孔的开放程度
(1)低温下光合色素的含量降低,影响了光合作用的进行,叶片中光合色素吸收的光能的用途是_____;此外,低温胁迫下水稻光合速率降低的原因还有_________。
(2)低温胁迫下水稻叶片胞间CO2浓度比正常培养条件下高,原因是_____。
(3)植物抵抗低温胁迫的能力与膜透性的变化有关,可用电导法测定,相对电导值与植物抵抗低温胁迫的能力呈反比。为了提高水稻抵抗低温胁迫的能力,科研人员对水稻进 抗寒驯化,结果如下图所示:
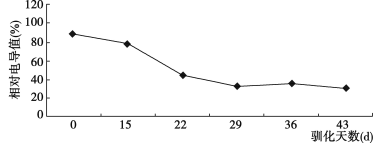
①据图分析可知,抗寒驯化对水稻抵抗低温胁迫能力的影响是_____。
②植物体内脱落酸通常在环境不佳时产生,故又称为“逆境激素”,为探究脱落酸能否代替低温进行水稻的抗寒驯化,实验思路是_____。
【题目】随着大量生活污水、工业污染物流入海洋,使海水中Cu2+、Zn2+、Cd2+等重金属离子的量不断增加,这些离子陆陆续续进入单细胞藻类体内,最终进入人体内,影响人类的生命健康。某科研小组以扁藻和盐藻为实验材料,研究三种金属离子对单细胞藻类生长的影响,三种离子的浓度如表所示,实验结果如图所示:
Cu2+、Cd2+、Zn2+的浓度梯度(g/mL)
T0 | T1 | T2 | T3 | T4 | T5 | T6 | T7 | |
Cu2+ | 0 | 10 | 20 | 30 | 100 | 200 | 300 | 500 |
Cd2+ | 0 | 40 | 80 | 100 | 300 | 500 | 600 | 700 |
Zn2+ | 0 | 40 | 80 | 100 | 300 | 500 | 600 | 700 |
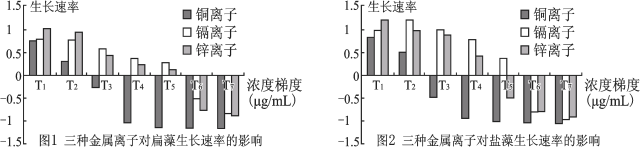
(1)大量生活污水、工业污染物进入海洋,导致水体富营养化,说明了生态系统_____________。大量重金属离子进入单细胞藻类,通过_____________途径最终进入人体体内,因为重金属离子在生物体内不易降解且不易排出,所以营养级越高的生物体内重金属离子浓度越_______(填“高”或“低”)。
(2)该实验中同浓度的三种离子中,_____________对扁藻和盐藻的生长影响大;同密度的两种单细胞藻类中,_____________对Zn2+敏感。结合图1和图2可得出的结论是①_____________,②____________。