题目内容
【题目】I.实验室用下图所示的装置制取乙酸乙酯。
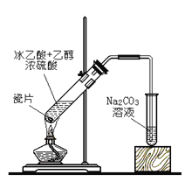
(1)在大试管中配制一定比例的乙醇、乙酸和浓硫酸的混合液,操作步骤如下:__________,然后轻振荡使其混合均匀。
(2)浓硫酸的作用是:① _______________;② ______________。
(3)右边装置中通蒸气的导管要插在液面上而不能插入溶液中,目的是防止溶液的倒吸。造成倒吸的原因是___________________。
(4)分离得到乙酸乙酯的方法是________________,分离需要的玻璃仪器是___________。
(5)若加的是C2H518OH写出制乙酸乙酯的方程式_________________。
II.某实验小组用下列装置进行乙醇催化氧化的实验。
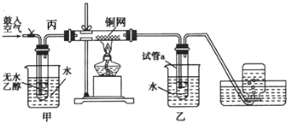
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式_____________________、____________________。在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是_________________反应。
(2)甲和乙两个水浴作用不相同。甲的作用是______________;乙的作用是____________。
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是________________。集气瓶中收集到的气体的主要成分是____________。
(4)图中丙处导管应倾斜的原因是______________________________。
(5)本实验中若不鼓入空气,其他操作不变,乙处试管内也得到了乙醛,则发生的化学方程式为_______________________________。
【答案】向大试管中注入适量乙醇,将浓硫酸加入乙醇中,边加边振荡,最后加入乙酸 催化剂 吸水剂 挥发出的乙醇和乙酸易溶于水,溶于水后导管内压强减少引起倒吸 分液 分液漏斗,烧杯 CH3COOH+CH3CH218OH![]() CH3CO18OCH2CH3+H2O 2Cu+O2
CH3CO18OCH2CH3+H2O 2Cu+O2![]() 2CuO CH3CH2OH+CuO
2CuO CH3CH2OH+CuO![]() CH3CHO+Cu+H2O 放热 加热 冷却 乙醛、乙醇、水 氮气 使冷凝的乙醇蒸汽易于回流 CH3CH2OH
CH3CHO+Cu+H2O 放热 加热 冷却 乙醛、乙醇、水 氮气 使冷凝的乙醇蒸汽易于回流 CH3CH2OH![]() CH3CHO+H2
CH3CHO+H2
【解析】
I.(1)浓硫酸在混合过程中放出大量热,浓硫酸密度大于乙醇,所以应该将浓硫酸加入到乙醇中;
(2)浓硫酸在反应中作催化剂和吸水剂,使生成乙酸乙酯的反应速率加快,并减少水的量,平衡向着正向移动,增加乙酸乙酯的产率;
(3)根据挥发出来的乙醇和乙酸易溶于水,容易产生压强差进行解答;
(4)乙酸乙酯不溶于饱和碳酸钠溶液,可以通过分液方法分离;分液操作使用的仪器有分液漏斗、烧杯等;
(5)酯化反应的原理为“酸脱羟基醇脱氢”,据此写出反应的化学方程式;
II.甲中鼓入空气,且在水浴加热条件下,氧气和乙醇在铜催化下,加热发生氧化还原反应生成乙醛和水,进入乙中的为乙醇、乙醛,在冷却下可收集到乙醛,集气瓶收集的为氮气。
(1)铜与氧气反应生成氧化铜,氧化铜与乙醇反应生成乙醛、Cu与水;反应需要加热进行,停止加热反应仍继续进行,说明乙醇的氧化反应是放热反应;
(2)甲是水浴加热可以让乙醇在一定的温度下成为蒸气,乙是将生成的乙醛冷却;
(3)乙醇被氧化为乙醛,同时生成水,反应过程中乙醇不能完全反应,故a中冷却收集的物质有乙醛、乙醇与水;空气中氧气反应,集气瓶中收集的气体主要是氮气;
(4)乙醇易挥发,图中丙处导管应倾斜的原因是使冷凝的乙醇蒸汽易于回流;
(5)若不鼓入空气,其他操作不变,乙处试管内也得到了乙醛,则乙醇分解生成乙醛和氢气。
I.(1)制取乙醇、乙酸和浓硫酸的混合液时,正确操作方法为:向大试管中注入适量乙醇,将浓H2SO4加入乙醇中,边加边振荡,最后加入乙酸;
(2)浓硫酸在乙酸乙酯的制取反应中,能够加快反应速率,起到了催化剂作用,能够吸收反应生成的水,平衡正向移动,增加了乙酸乙酯的产率,起到了吸水剂的作用;
(3)乙醇和乙酸的沸点较低,反应过程中容易挥发,由于挥发出的乙醇和乙酸易溶于水,溶于水后导管内压强减小引起倒吸现象;
(4)乙酸乙酯不溶于饱和碳酸钠溶液,所以混合液分层,可以通过分液操作将乙酸乙酯分离出来;分液操作使用的仪器有分液漏斗、烧杯等;
(5)乙酸与乙醇生成乙酸乙酯的反应中,乙醇脱去羟基中的氢原子、乙酸脱去羧基中的羟基,所以18O反应后进入乙酸乙酯中,该反应的化学方程式为:CH3COOH+CH3CH218OH![]() CH3CO18OCH2CH3+H2O;
CH3CO18OCH2CH3+H2O;
II.(1)乙醇的催化氧化反应过程:金属铜被氧气氧化为氧化铜:2Cu+O2![]() 2CuO,氧化铜将乙醇氧化为乙醛:CH3CH2OH+CuO
2CuO,氧化铜将乙醇氧化为乙醛:CH3CH2OH+CuO![]() CH3CHO+Cu+H2O,反应需要加热进行,停止加热反应仍继续进行,说明乙醇的氧化反应是放热反应;
CH3CHO+Cu+H2O,反应需要加热进行,停止加热反应仍继续进行,说明乙醇的氧化反应是放热反应;
(2)甲和乙两个水浴作用不相同,甲是热水浴,作用是乙醇平稳气化成乙醇蒸气,乙是冷水浴,目的是将乙醛冷却下来;
(3)乙醇被氧化为乙醛,同时生成水,反应过程中乙醇不能完全反应,故a中冷却收集的物质有乙醛、乙醇与水;空气中氧气有部分参加反应,故集气瓶中收集的气体主要是氮气;
(4)乙醇的沸点较低,其易挥发也易被冷凝,图中丙处导管倾斜的目的是便于使冷凝的乙醇蒸汽易于回流;
(5)若不鼓入空气,其他操作不变,乙处试管内也得到了乙醛,则乙醇分解生成乙醛和氢气,该反应为:CH3CH2OH![]() CH3CHO+H2。
CH3CHO+H2。