题目内容
【题目】用2mL1mol/LCuSO4溶液与3mL0.5mol/LNaOH溶液混合后,加入40%的甲醛溶液0.5mL,加热至沸腾,无砖红色沉淀生成,实验失败的主要原因是( )
A.甲醛的量太少B. CuSO4的量太少C.NaOH的量太少D.加热的时间太短
【答案】C
【解析】
甲醛属于饱和一元醛,但它又相当于二元醛,在与弱氧化剂(新制的Cu(OH)2悬浊液)反应的过程中,涉及的反应方程式为:Cu2++2OH-=Cu(OH)2↓,HCHO+4Cu(OH)2![]() CO2↑+2Cu2O↓+5H2O。实验中要注意碱液需过量,反应条件为加热至沸腾。据此进行分析。
CO2↑+2Cu2O↓+5H2O。实验中要注意碱液需过量,反应条件为加热至沸腾。据此进行分析。
该反应的本质是:甲醛中的醛基具有还原性,新制的Cu(OH)2悬浊液具有弱氧化性,醛基与Cu(OH)2中的+2价的铜发生氧化还原反应。只要有醛基即可与新制的Cu(OH)2悬浊液发生反应;
根据题意可知:n(CuSO4)=![]() ,根据反应:Cu2++2OH-=Cu(OH)2↓,可知n(OH-)=
,根据反应:Cu2++2OH-=Cu(OH)2↓,可知n(OH-)=![]() ,则需要0.5mol/LNaOH溶液的体积=
,则需要0.5mol/LNaOH溶液的体积=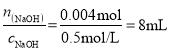 ,反应过程中要保持碱过量,则所需NaOH溶液的体积V>8mL,而题中该NaOH溶液的体积为3mL,NaOH的量不够,导致实验中未见砖红色沉淀。
,反应过程中要保持碱过量,则所需NaOH溶液的体积V>8mL,而题中该NaOH溶液的体积为3mL,NaOH的量不够,导致实验中未见砖红色沉淀。
故由以上结论可知,实验失败的主要原因是NaOH的量不够,C项正确;
答案选C。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目